Vaccination et couverture vaccinale en france

INTRODUCTION/GÉNÉRALITÉ
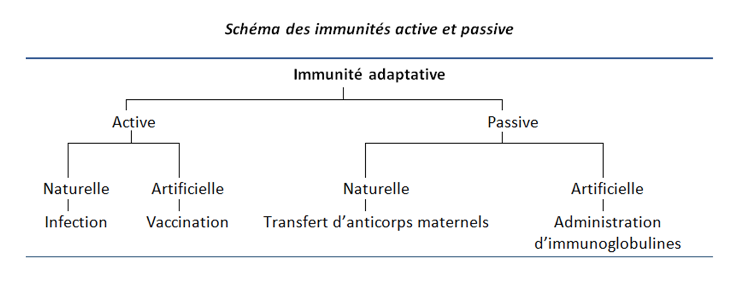
- La vaccination anti-infectieuse consiste à introduire chez un individu une préparation antigénique, le vaccin, susceptible d’induire une réponse immune apte à le protéger contre une infection naturelle ou ses conséquences. Il s’agit d’une immunoprophylaxie active à la différence de l’immunoprophylaxie passive obtenue par l’administration intra-veineuse IV ou intra-musculaire IM d’anticorps comme les gammaglobulines.
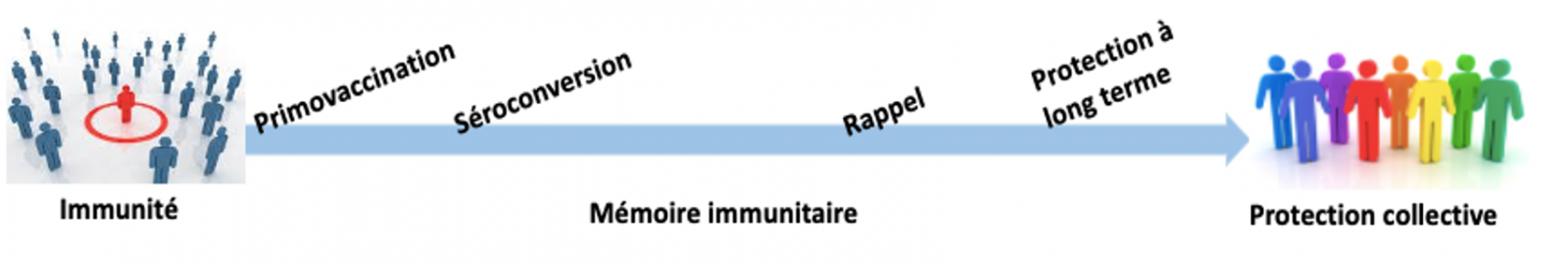
- La primovaccination concerne les premières injections successives d'un vaccin, nécessaires pour obtenir une protection contre une maladie. La primovaccination peut être constituée d’une ou plusieurs injections selon les vaccins.
- Un rappel est le renouvellement de l'administration d'un vaccin, destiné à maintenir un bon niveau de protection. Le rappel peut être unique ou répété dans le temps selon les vaccins.
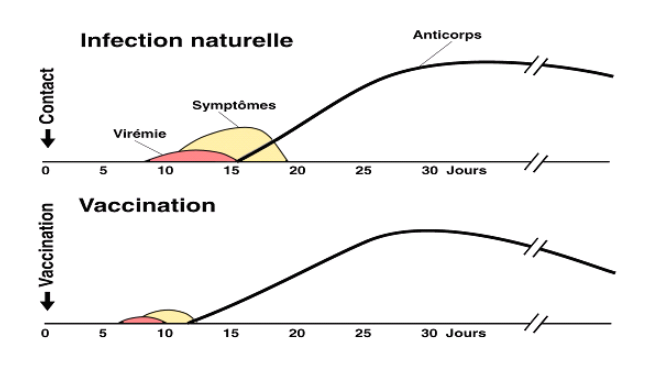
- Séroconversion : on parle de séroconversion quand on détecte dans le sérum des anticorps spécifiques. Elle apparaît avec un temps de latence, après une infection virale, bactérienne ou une vaccination. La séroconversion est progressive dans la temps, et la protection contre la maladie dépend du nombre d’injections vaccinales nécessaires. Habituellement, la protection apportée par le vaccin contre une maladie est présente entre deux et trois semaines après la vaccination. Lorsqu’une vaccination exige 2 ou 3 doses, la protection apparaît dès la 1ère dose, par contre, elle ne durera dans le temps que si toutes les doses sont administrées.
- Séroprotection : Présence, dans le sérum, d’un niveau d’anticorps considéré comme suffisant pour protéger une personne contre une maladie. L’expression titre d’anticorps protecteur est aussi utilisée pour désigner cette notion.
- Immunisations actives et passives : L’immunisation permet de procurer au corps humain les moyens de se défendre contre une agression biologique avant qu’elle ne survienne.
- Dans l’immunisation active, il s’agit de stimuler le système immunitaire par un vaccin connu et contrôlé en évitant les conséquences liées à l’infection naturelle.
- Dans l’immunisation passive, il s’agit d’un transfert d’anticorps (immunoglobulines) provenant d’un sujet immunisé à un autre qui ne l’est pas.

- La couverture vaccinale est la proportion de la population ciblée par un vaccin qui est effectivement vaccinée. 95%, c'est le taux de couverture vaccinale à atteindre pour une protection collective.
HISTORIQUE
A) Jusqu’au 17ème siècle : constats et essais
- Des écrits retrouvent l’utilisation de croûtes de vaches pour protéger de la variole – 3000 av JC.
- Dès l’Antiquité, on avait remarqué que les personnes atteintes une première fois de certaines maladies infectieuses ne tombaient pas malades une seconde fois.
- Les premiers exemples d’immunisation concernent la variole. Connue de longue date, aussi appelée « petite vérole », celle-ci refait surface au 17ème siècle sous forme d’épidémies qui font chaque fois des milliers de victimes (la mortalité de la variole selon les formes pouvaient être de 30%.)
- Dans toutes les régions du monde, on s’efforçait de déclencher une forme légère de variole en introduisant dans le corps d’une personne, par divers procédés, du pus de pustules de malades, afin de lui procurer une protection à vie.
B) 18ème siècle : Jenner et la variole des vaches
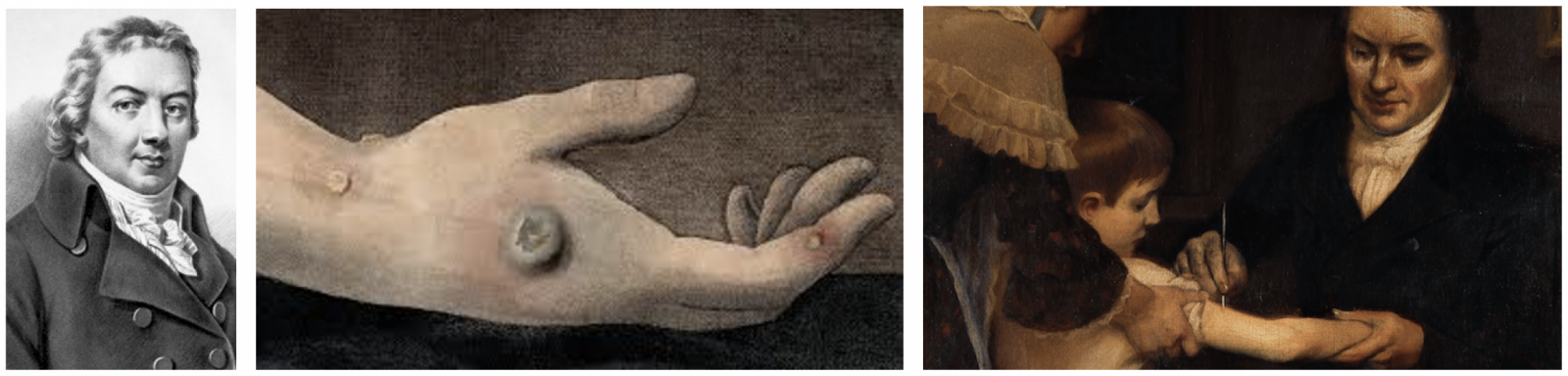
- En 1796, un médecin de campagne anglais, Edward Jenner, fait une découverte importante : une maladie bénigne des vaches, la « vaccine », ou « cowpox » ressemble à la variole. Les fermières, en contact régulier avec le virus de la vaccine, ne contractent pas la variole lors des épidémies.
- Jenner contamine une personne avec la vaccine via de petites incisions dans la peau. Puis s’efforce d’infecter son « cobaye » avec la variole, sans succès : celui-ci ne développe pas la maladie. Le nom de « vaccination » est donné à cette opération. Après de nombreuses critiques, elle connaît un succès retentissant en Europe et donne lieu à l’organisation de grandes campagnes de vaccination antivariolique.
C) 19ème siècle : Pasteur crée le premier vaccin atténué
- Dans la seconde moitié du 19ème siècle, Louis Pasteur, un docteur en sciences français, explore le rôle des microbes dans la survenue des maladies contagieuses, en travaillant sur des animaux d’élevage. Il montre que le choléra des poules est dû à une bactérie.
- Il retrouve de vieilles cultures de cette bactérie, et les administre à des volailles. Celles-ci tombent malades mais ne meurent pas, même quand on les infecte ensuite avec des germes frais et virulents. Louis Pasteur vient de créer un vaccin vivant atténué. En l’honneur de Jenner, il invente le terme « vaccin ».
- En 1881, Pasteur énonce le principe de la vaccination : (inoculer) « des virus affaiblis ayant le caractère de ne jamais tuer, de donner une maladie bénigne qui préserve de la maladie mortelle ».
- Après avoir mis au point un autre vaccin animal atténué contre la maladie du charbon qui décimait les troupeaux ovins et bovins, Pasteur oriente ses recherches vers la vaccination humaine. Il se penche sur une maladie touchant à la fois l’animal et l’homme : la rage.
- A partir de cerveaux d’animaux morts de la rage, Pasteur parvient à isoler, purifier et inactiver la souche de l’agent contagieux. En 1885, il met au point le premier vaccin humain à virus atténué. En l’occurrence, celui-ci est utilisé post-exposition (il est administré avec succès à un jeune berger mordu par un chien supposé enragé). Une commission d’enquête internationale confirme son efficacité.
- Il s’est avéré par la suite que le virus utilisé dans le vaccin contre la rage était détruit, ce qui a ouvert la voie à des vaccins à base de microbes « tués ». Louis Pasteur crée autour de lui une véritable école de pensée scientifique. Il fonde un institut, l’Institut Pasteur, et forme de nombreux chercheurs en infectiologie, immunologie, parasitologie, génétique…
D) 1880-1930 : toxines, anatoxines et bacilles tués
- Ces « pasteuriens », comme Emile Roux, Alexandre Yersin ou Gaston Ramon, poursuivent l’œuvre du maître, tandis que se développe en Allemagne une seconde grande école de la microbiologie, emmenée par des chercheurs tels Robert Koch et Emil von Behring.
- Les scientifiques démontrent que ce sont les toxines sécrétées par le bacille de la diphtérie et du tétanos qui rendent ces maladies redoutables. Ils découvrent également comment le corps se protège de la maladie : en fabriquant des anticorps. Tout cela ouvre la voie à la production de vaccins contenant des « anatoxines », des toxines modifiées pour leur faire perdre leur toxicité.
- C’est à cette période également qu’on découvre l’« effet adjuvant » de certaines substances, comme les sels d’aluminium, qui augmentent le pouvoir immunologique du vaccin en boostant la création d’anticorps.
- Parallèlement, les scientifiques concentrent leurs recherches sur des vaccins dirigés contre des maladies bactériennes qui constituent de véritables fléaux pour les populations : typhoide, tuberculose, et choléra. Les recherches s’écartent du principe d’atténuation du pathogène pour opter pour son inactivation : le vaccin contient des bacilles tués.
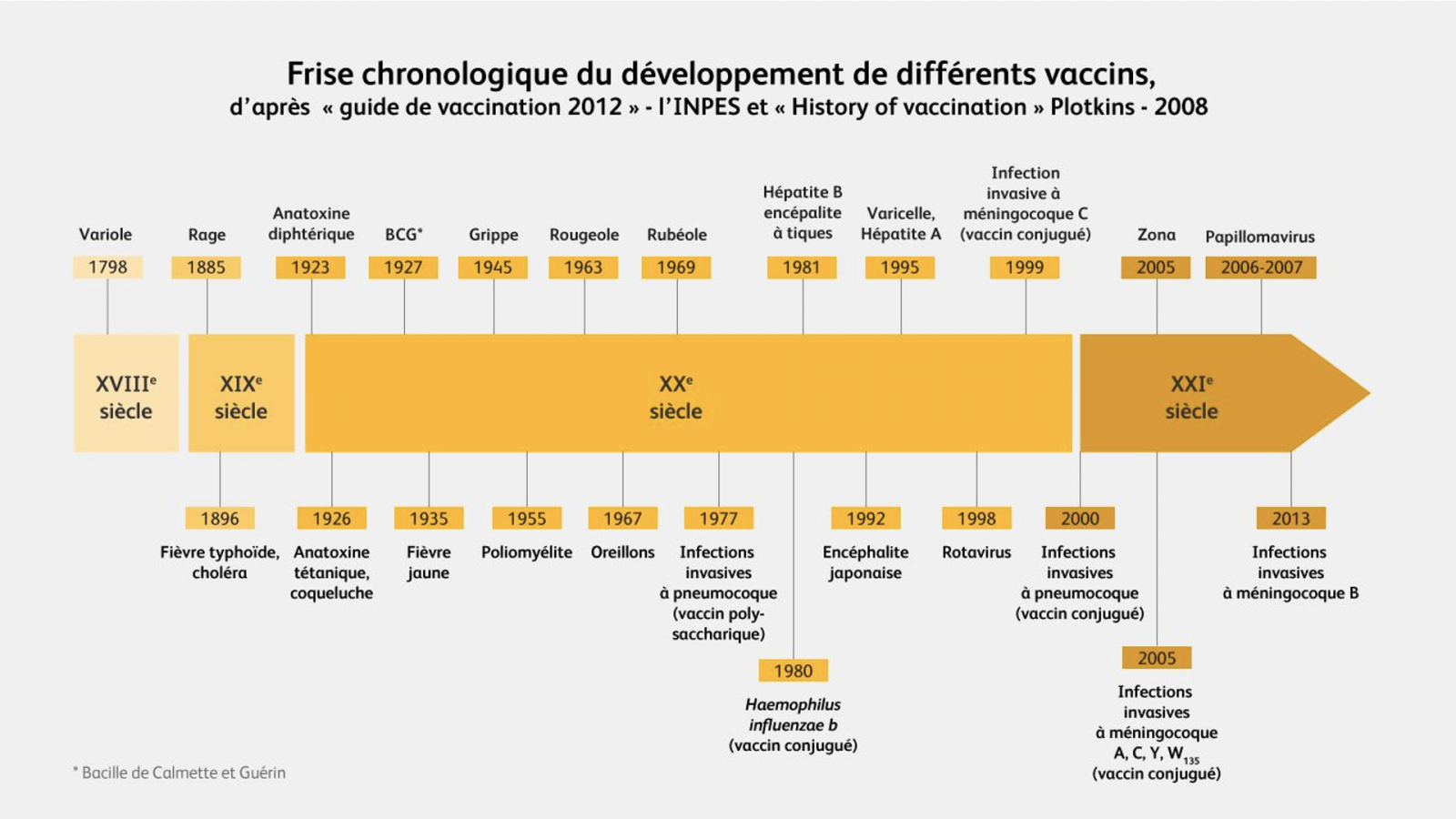
- Les vaccins contre la diphtérie, la typhoide, la tuberculose et le tétanos apparaissent dans les années 1920.
E) 1930-1960 : Nouveaux vaccins et vaccins combinés
- Des progrès dans les méthodes de culture de virus permettent l’émergence de plusieurs vaccins viraux. On passe d’une culture sur des œufs, des embryons de poulet, des tissus d’animaux vivants… à des techniques de culture cellulaire en milieu synthétique, qui seront adoptées largement en Europe et aux Etats-Unis.
- Les efforts se concentrent d’abord sur la fièvre jaune, contre laquelle un vaccin apparaît dans les années 30.
- L’américain Jonas Salk met au point le premier vaccin contre la grippe, puis, 20 ans plus tard, le premier vaccin injectable contre la poliomyélite. Quelques années après, le médecin polonais Albert Sabin en propose une forme orale.
- C’est également dans les années 50-60 que voient le jour les vaccins à plusieurs valences, offrant une protection combinée contre plusieurs maladies à la fois. C’est le cas notamment des vaccins trivalents : Diphtérie-Tétanos-Poliomyélite et Rougeole-Oreillons-Rubéole.
F) Après les années 60 : biotechnologies et génie génétique
- Après les avancées en matière de culture cellulaire, les biotechnologies et le génie génétique permettent à la vaccination de continuer à progresser.
- Des vaccins modernes peuvent par exemple s’appuyer sur la technologie de l’ADN recombinant : on insère un gène d’un virus dans une cellule (de levure, d’animal…) pour produire un antigène. Ce procédé permet le développement du vaccin contre l’hépatite B, au début des années 80.
- Les progrès en matière de synthèse artificielle et les travaux sur les capsules qui entourent les bactéries conduisent à la mise au point de vaccins contre les pneumocoques, les méningocoques A et C, et l’haemophilus influenzae de type B, responsables d’infections graves comme les méningites. Ces vaccins contiennent des substances issues de l’enveloppe bactérienne.
- En 2006 : apparaît un vaccin contre les infections à papillomavirus, permettant de réduire l’incidence des cancers du col de l’utérus.1
G) Et demain ?
- De nombreuses innovations dans le domaine de la vaccination sont en train de voir le jour. Les technologies de production des vaccins ont évolué rapidement, parallèlement aux évolutions réalisées dans d’autres domaines, tels que la biologie moléculaire, le séquençage génomique, l’immunologie…
- Jusqu’à présent, les vaccins étaient développés dans l’optique de prévenir des maladies infectieuses.
- Le développement de nouveaux vaccins et de nouvelles technologies d’administration et de stockage permettra de cibler des maladies émergentes et de protéger des populations spécifiques (femmes enceintes, nouveau-nés, personnes âgées ou immunodéprimées…). L’extension de la vaccination à la prévention de maladies telles que les cancers, les allergies ou les maladies auto-immunes. renforcera encore l’importance de cette pratique de santé publique.
PHYSIOPATHOLOGIE
A) Système et mémoire immunitaire
- Le système immunitaire permet à l’organisme de se défendre contre les agents infectieux.
- La mémoire immunitaire est la capacité des lymphocytes B et T, après un 1er contact avec un antigène, à le reconnaître, à réagir de façon plus rapide et plus marquée.
- Anticorps : Protéine, aussi appelée immunoglobuline, produite par un organisme en réponse à une stimulation par un antigène et ayant la propriété de réagir spécifiquement à cet antigène.
- Antigène : Substance capable, lorsqu’elle est introduite dans un organisme, de provoquer une réponse du système immunitaire. Les virus, les bactéries et tout autre agent infectieux ont à leur surface ou sécrètent des molécules considérées comme étrangères qu’on appelle antigènes.
-
La valence d’un vaccin, correspond soit au nombre de bactéries ou virus visés, soit au nombre de souches d’un même germe.
-
Exemple 1 : Vaccin 13-valent ou 23-valent contre le pneumocoque.
-
Exemple 2 : Vaccin trivalent combiné ROR.
-
B) Mécanisme d'action des vaccins
- L’objectif des vaccins est de déclencher une réponse immunitaire contre un antigène, de sorte que lorsque la personne est de nouveau exposée à cet antigène, une réponse immunitaire secondaire nettement plus forte soit déclenchée. Les vaccins contiennent les mêmes antigènes que ceux présents sur les agents pathogènes qui provoquent la maladie en question, mais l’exposition aux antigènes dans les vaccins est contrôlée. La vaccination permet d’activer le système immunitaire qui, lorsque la personne vaccinée est exposée aux agents pathogènes dans l’environnement, peut les détruire avant qu’ils ne provoquent la maladie.
- Il existe donc deux moyens d’acquérir une immunité contre un agent pathogène : par une infection naturelle et par la vaccination. Les infections naturelles et les vaccins produisent un résultat final très similaire (immunité), mais la personne qui reçoit un vaccin ne développe pas la maladie et ses complications potentiellement mortelles.1
C) Description du système immunitaire
1) Caractéristiques du système immunitaire
- Spécificité : le système immunitaire est capable de reconnaître et d’éliminer certains agents pathogènes ou certaines molécules étrangères (antigènes). Chaque antigène possède une structure moléculaire unique qui déclenche la production de cellules ou d’anticorps spécifiques dirigés contre lui.
- Diversité : le système immunitaire est capable de combattre des millions de types d’agresseurs en reconnaissant chacun d’eux à ses marqueurs antigéniques.
- Reconnaissance du soi et du non‑soi : le système immunitaire est capable de faire la distinction entre les molécules de l’hôte lui‑même (le soi) et les molécules étrangères (le non‑soi).
- Mémoire : le système immunitaire est capable de se souvenir des antigènes qu’il a rencontrés et d’y réagir rapidement et efficacement lors d’expositions ultérieures.
2) Composants du système immunitaire
- Cellules présentatrices d’antigènes : cellules spécialisées qui capturent les antigènes, les transportent et les présentent aux lymphocytes (ex. : cellules dendritiques).
- Lymphocytes : cellules qui ont à leur surface des récepteurs spécifiques d’antigènes :
- Lymphocytes B : ils sont créés dans la moelle osseuse et y poursuivent leur maturation. Ils sont les principaux responsables de l’immunité humorale.
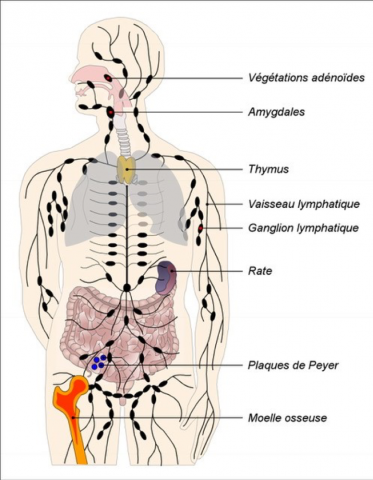
- Lymphocytes T : ils sont créés dans la moelle osseuse et migrent dans le thymus. Ils sont les principaux responsables de l’immunité cellulaire.
- Cellules effectrices : types de cellules qui servent à éliminer les agents pathogènes par divers mécanismes (ex. : macrophages).
- Moelle osseuse : lieu principal de fabrication des lymphocytes.
- Rate : organe lymphoïde important où ont lieu la présentation d’antigènes aux lymphocytes T et la différenciation des cellules mémoire. La rate assume plusieurs fonctions :
- Elle filtre les bactéries et les complexes antigène-anticorps pour les éliminer.
- Elle produit une quantité considérable d’IgM.
- Ganglions et autres tissus lymphatiques (ex. : amygdales) : organes lymphoïdes dans lesquels les cellules du système immunitaire interagissent avec les antigènes. Les cellules du système immunitaire et les agents pathogènes entrent dans les organes lymphoïdes par les vaisseaux sanguins et les canaux lymphatiques.1
D) Deux types de réactions immunitaires
Pour assurer sa protection, le corps humain possède 2 types de mécanismes de défense : l’immunité innée et l’immunité adaptative.
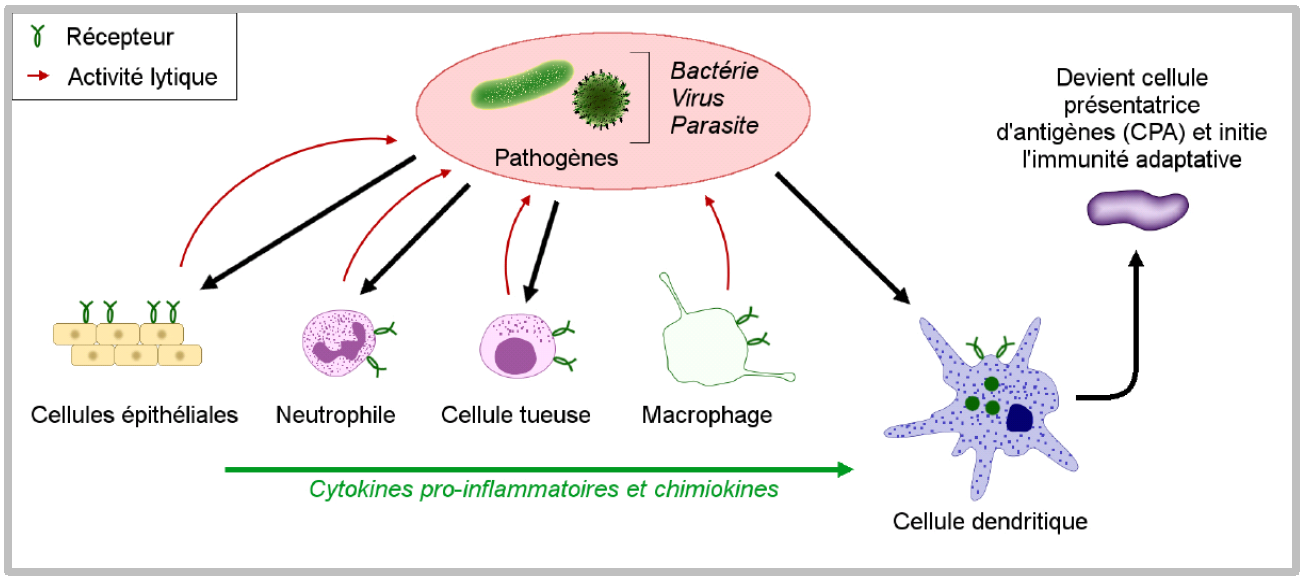
1) L’immunité innée
- L’immunité innée permet la défense de l'organisme contre les agents infectieux de façon immédiate.
L’immunité innée comprend 2 lignes de défense :
- Ligne de défense externe :
- Empêche la pénétration des agents infectieux dans l’organisme.
- Est constituée de la peau et des muqueuses (barrière physique) ainsi que des sécrétions telles que le mucus, la salive, les larmes et le suc gastrique (barrière chimique).
- Ligne de défense interne :
- Empêche la prolifération des agents infectieux qui ont réussi à pénétrer dans l’organisme.
- Est constituée de plusieurs types de cellules (ex. : macrophages, neutrophiles, monocytes, cellules dendritiques) et de plusieurs types de protéines (ex. : cytokines, interférons, complément).

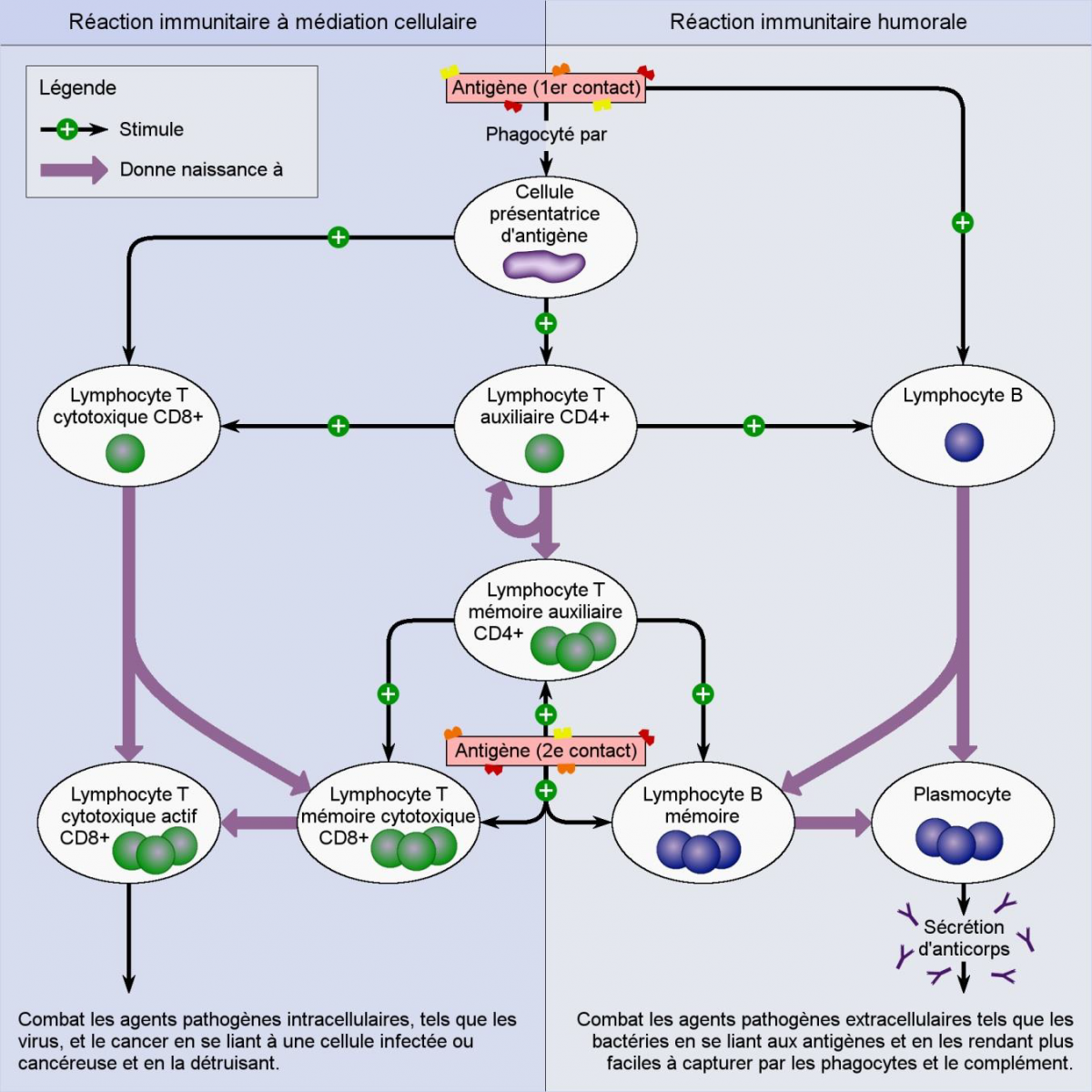
2) Immunité adaptative (acquise)
L’immunité adaptative confère une protection plus tardive, mais plus durable.
À la suite de l’interaction entre un agent infectieux et l’immunité innée, l’immunité adaptative entre en action dans les tissus lymphoïdes, surtout dans les ganglions et la rate. Plusieurs mécanismes entrent alors en jeu :
- L’antigène (agent infectieux) active directement les lymphocytes B, qui possèdent des récepteurs spécifiques. Les lymphocytes B activés deviennent alors des plasmocytes, qui vont sécréter des anticorps spécifiques pour la destruction de l’antigène (immunité humorale).
- L’antigène (agent infectieux) est présenté à des lymphocytes T par des cellules présentatrices d’antigènes (ex. : cellules dendritiques). Les cellules présentatrices d’antigènes activent les lymphocytes T, qui se différencient en :
- Lymphocytes T cytotoxiques (CD8+), qui détruisent les cellules infectées (immunité cellulaire);
- Lymphocytes T auxiliaires (CD4+), ou T helper cells, qui stimulent les lymphocytes B pour produire une plus grande quantité d’anticorps et de cellules mémoire, qui iront ensuite se loger dans la moelle.

3) Immunité humorale et cellulaire
- L’immunité adaptative entraîne 2 types de réponse immunitaire : l’immunité humorale et l’immunité cellulaire.
- Cette distinction dans la réponse immunitaire adaptative est utile pour l’évaluation de la réponse immunitaire après la vaccination.
- Toutefois, il est clairement prouvé que la plupart des antigènes et des vaccins stimulent à la fois les lymphocytes B et les lymphocytes T, et que ces 2 réponses sont intimement liées.
a) Immunité humorale
- L’immunité humorale est assurée par la production d’anticorps par les lymphocytes B et est principalement dirigée contre les agents infectieux extracellulaires tels que les bactéries.
- Les lymphocytes B se différencient en plasmocytes producteurs d’anticorps et en lymphocytes B mémoire.
- Les principaux anticorps sont :
- Les IgG : elles se trouvent dans le sang et les tissus
- Les IgM : elles sont les premières à être fabriquées
- Les IgA : elles sont dominantes dans les sécrétions extracellulaires;
- Les IgE : elles sont jouent un rôle dans les réactions allergiques;
- Les IgD : elles sont en faible quantité dans le sérum.
- La durée de vie des plasmocytes est limitée, car ils ne se divisent plus après leur différenciation. Ils disparaissent progressivement. La disparition des anticorps reflète la disparition des plasmocytes.
- La durée de la persistance des anticorps est directement liée au titre d’anticorps atteint après la vaccination.
- La mesure des anticorps sériques en laboratoire permet de connaître la réponse immunitaire humorale aux vaccins.
- La réponse humorale ne représente qu’une partie de la réponse immunitaire, l’autre partie étant l’immunité cellulaire.
b) L’immunité cellulaire
- L’immunité cellulaire est surtout assurée par les lymphocytes T et est principalement dirigée contre les agents infectieux intracellulaires tels que les virus.
- L’immunité cellulaire peut protéger la personne même en l’absence d’anticorps décelables.
- L’immunité cellulaire est plus difficile à mesurer que l’immunité humorale.
- Les cellules mémoire sont réactivées lors de nouveaux contacts avec un antigène spécifique à la suite de l’exposition à un vaccin ou à la maladie. Elles ont une survie prolongée.1
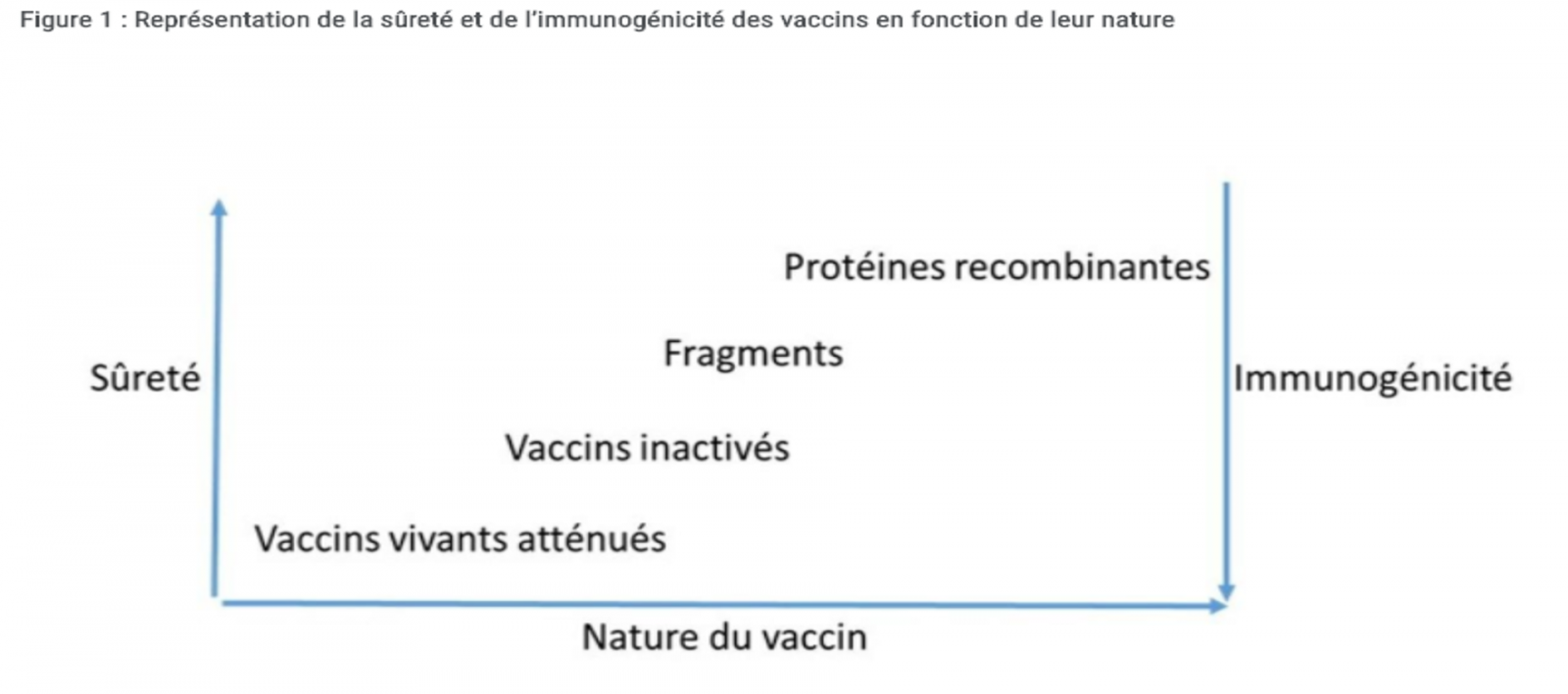
immunogénicité des vaccins
Plusieurs facteurs peuvent influencer la réponse immunitaire induite par la vaccination. La nature et l’intensité de la réponse varieront en fonction de facteurs liés au vaccin et de facteurs liés à l’hôte.
A) Facteurs liés au vaccin
1) Nature de l’antigène
a) Vaccins vivants atténués
- Les particules virales se disséminent rapidement dans l’organisme, se multiplient et activent l’immunité innée puis l’immunité adaptative, comme lors de l’infection naturelle.
- Les réactions inflammatoires locales sont rares et sont liées plus au volume injecté qu’à la composition du vaccin.
- L’infection est habituellement non apparente. Elle peut être accompagnée de symptômes systémiques atténués (ex. : fièvre, malaises, éruption) après la période nécessaire à la réplication virale (de 5 à 21 jours selon le vaccin).
- Le temps nécessaire à l’induction d’anticorps (de 2 à 3 semaines) reflète la durée de différenciation des lymphocytes B en plasmocytes dans la rate et les ganglions.
- Comparativement aux vaccins inactivés, les vaccins vivants atténués induisent une meilleure réponse immunitaire innée, une production d’anticorps plus importante et plus persistante en raison de la réplication systémique. La conséquence est l’obtention d’un taux d’anticorps plus élevé et plus durable.
b) Vaccins inactivés
- La réponse immunitaire est variable selon les antigènes des vaccins.
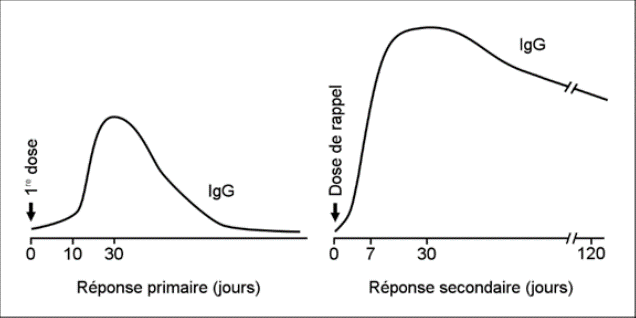
- Les Ag vaccinaux sont pris en charge par les cellules dendritiques. Celles-ci provoquent l’activation des cellules inflammatoires et déclenchent la réaction locale. Les cellules dendritiques migrent également vers les ganglions régionaux et peuvent y déclencher de l’inflammation. Cette période dure de 2 à 3 semaines, produisant un pic d’anticorps environ 1 mois après la vaccination.
- Les plasmocytes responsables de cette réponse immunitaire primaire meurent rapidement par la suite, entraînant une baisse rapide du taux d’anticorps, d’où la nécessité d’administrer 1 ou plusieurs doses additionnelles, qui entraîneront une réponse anamnestique secondaire.
- On distingue plusieurs types de vaccins inactivés :
- Inactivés polysaccharidiques;
- Inactivés polysaccharidiques conjugués à une protéine;
- Inactivés entiers ou inactivés à protéines purifiées;
- Inactivés à ARN messager;
- Inactivés à protéines recombinantes;
- Inactivés à vecteur viral.
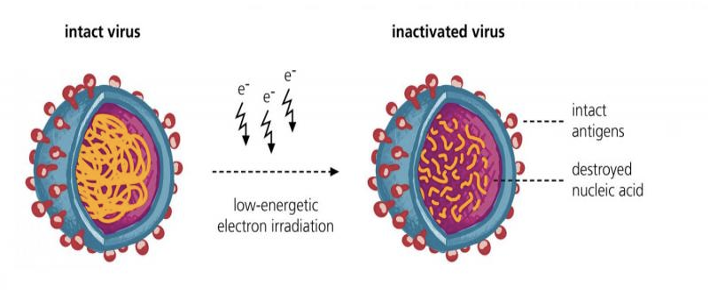
+ Vaccins entiers ou à protéines purifiées :
- Les vaccins inactivés entiers sont constitués de micro‑organismes complets, alors que les vaccins inactivés à protéines purifiées contiennent des protéines constituantes des micro-organismes
- La présence de protéines rend les substances immunogènes et induit une réponse immunitaire humorale (lymphocytes B) et cellulaire (lymphocytes T)
- Les antigènes sont dits T‑dépendants
- Ces vaccins sont immunogènes avant l’âge de 2 ans
- La production de cellules mémoire permet une réponse anamnestique lors d’une nouvelle exposition à ces vaccins
+ Vaccins polysaccharidiques :
- Les polysaccharides sont des constituants de la membrane externe de la bactérie
- La réponse immunitaire induite est humorale seulement (lymphocytes B)
- Les lymphocytes T ne sont pas stimulés
- Les antigènes sont dits T‑indépendants
- Ces vaccins sont peu ou pas immunogènes avant l’âge de 2 ans
- Il n’y a pas de production de cellules mémoire et de réponse anamnestique à la suite d’une nouvelle exposition à ces vaccins
+ Vaccins polysaccharides conjugués à une protéine :
- La conjugaison est le couplage des polysaccharides à une protéine vectrice
- La réponse immunitaire est apparentée à celle des vaccins inactivés entiers ou inactivés à protéines purifiées et elle possède les mêmes caractéristiques
- La réponse immunitaire induite est humorale (lymphocytes B) et cellulaire (lymphocytes T)
- Les principales protéines utilisées pour la conjugaison dans la fabrication des vaccins contre le pneumocoque et le méningocoque sont :
- anatoxine diphtérique
- anatoxine tétanique
- variante non toxique de la toxine diphtérique (CRM197)
- protéine OMV provenant de la capsule de Neisseria meningitidis
+ Vaccins à protéines recombinantes :
- Une protéine recombinante est produite par une cellule (comme une bactérie, une plante, une cellule de mammifère ou encore d’insecte) servant « d’usine vivante » dont le matériel génétique a été modifié avec une séquence de gènes permettant de produire cette protéine ou plusieurs protéines s’assemblant en particules pseudo-virales.
- Celles-ci sont purifiées et incluses dans le vaccin, qui permettra d’induire une immunité contre le pathogène d’origine de la séquence de gènes
+ Vaccins à vecteur viral :
- Le vecteur viral, un virus inoffensif pour l’humain, exprime une protéine à sa surface.
- La réponse immunitaire induite est humorale (lymphocytes B) et cellulaire (lymphocytes T)
+ Vaccins à ARN messager :
- Un vaccin à ARN messager est constitué de nanoparticules lipidiques contenant de l’ARN messager. Cet ARN messager contient un fragment de l’information génétique du virus
- Le vaccin à ARN messager est absorbé par les cellules. Dans le cytoplasme de la cellule, il permet de fabriquer une protéine virale qui va stimuler le système immunitaire
- La réponse immunitaire induite est humorale (lymphocytes B) et cellulaire (lymphocytes T)
- L’ARN messager est utilisé dans la production de vaccins contre la COVID-19.1
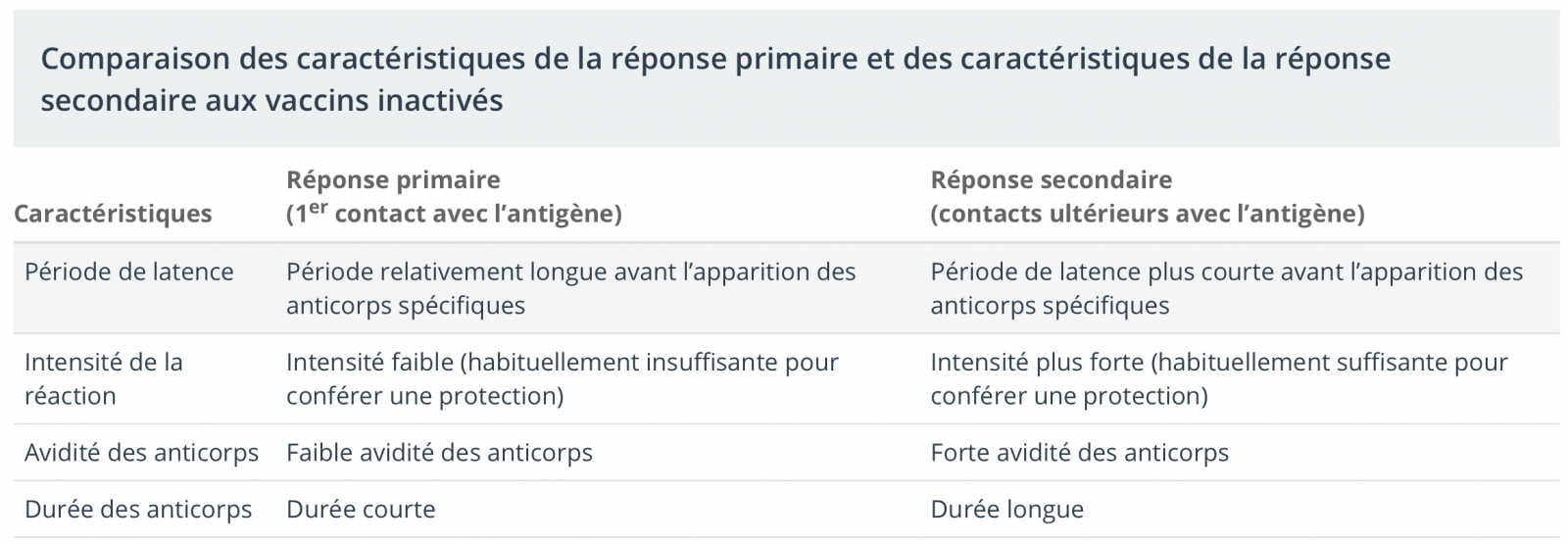
c) Implications cliniques du type d’antigène
- Les antigènes qui déclenchent une réaction humorale sans participation des lymphocytes T sont appelés Ag T indépendants.
- La réaction obtenue est plus faible et ne génère pas ou peu de mémoire immunitaire.
- Le vaccin Pneumovax®(pneumocoque 23 valences ou VPP23) est polysaccaridique non couplé à des protéines. C’est un Ag T indépendant.
Pour cette raison la réponse est plus courte (30 mois environ) et moins efficace qu’un vaccin anti pneumococcique contenant un polysaccaride et des protéines, Ag T dépendant, comme le Prévenar 13® (pneumocoque 13 valences).
2) Voie d’administration
- La voie intra-dermique est la plus immunogène en raison de la grande quantité de cellules présentatrices d’antigènes (ex. : cellules dendritiques et macrophages) présentes dans le derme.
- On observe une faible immunogénicité dans le tissu adipeux, car les cellules dendritiques y sont rares. Ainsi, la faible immunogénicité observée lorsque le vaccin est administré dans la fesse est probablement due à l’injection du vaccin dans le tissu adipeux plutôt que dans le muscle.
3) Présence d’un adjuvant
Les adjuvants peuvent être utilisés pour plusieurs raisons :
- Obtenir une meilleure réponse sérologique.
- Renforcer l’immunogénicité du vaccin en favorisant la réaction inflammatoire.
- Assurer une immunité plus durable.
- Utiliser une quantité plus faible d’antigènes.
- Administrer un plus petit nombre de doses.
L’adjuvant le plus fréquemment utilisé est le sel d’aluminium, en général sous forme de phosphate ou d’hydroxyde d’aluminium. Les autres adjuvants utilisés sont :
- Émulsion huile-eau MF59.
- AS01B (Fraction de Quillaja saponaria Molina et 3-O-désacyl-4’— monophosphoryl lipide A).
- Adjuvant AS03 (Polysorbate 80, tocophérol et squalène).
- Adjuvant AS04 (hydroxyde d’aluminium et 3‑O‑désacyl‑4’— monophosphoryl lipide A).
4) Posologie
- Généralement, lorsque la quantité d’antigènes contenus dans un vaccin est plus élevée, la quantité d’anticorps augmente.
5) Nombre de doses
- La réponse secondaire observée a tendance à augmenter avec le nombre de doses de vaccin administrées si les intervalles minimaux entre les doses de vaccin sont respectés.
6) Intervalles entre les doses
- Une 2e stimulation antigénique trop rapprochée de la 1re peut être inefficace à cause de l’élimination de l’antigène par les anticorps sériques encore présents à une forte concentration, d’où l’importance de respecter les intervalles minimaux entre les doses.
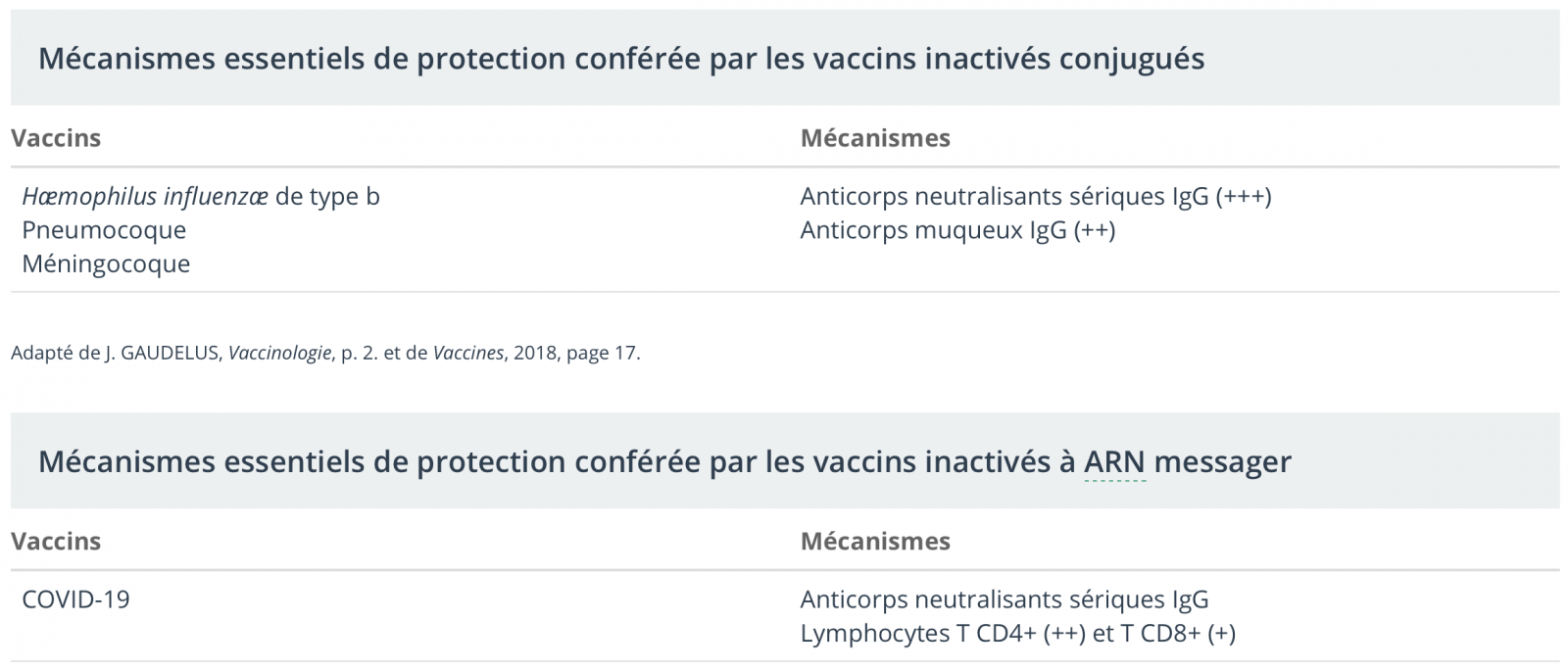
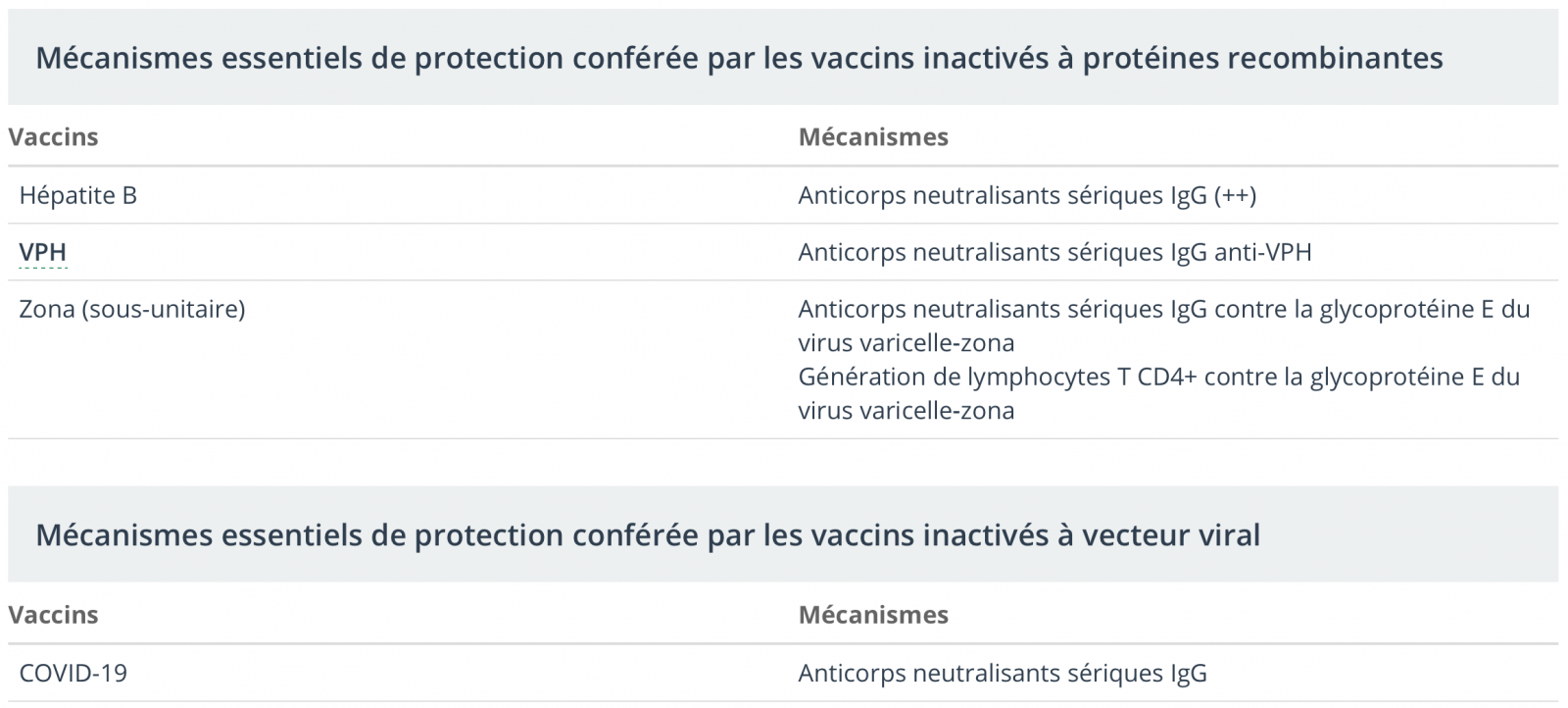
7) Mécanismes de protection conférée par certains vaccins
- Selon leur type, les vaccins peuvent induire des anticorps et des lymphocytes T, qui sont considérés comme des mécanismes essentiels de protection. Ces mécanismes sont présentés dans les tableaux qui suivent.
- Il est à noter que les lymphocytes T CD4+ participent à l’induction de toutes les réponses en anticorps, à l’exception de celles qui sont induites par les vaccins polysaccharidiques.




B) Facteurs liés à l’hôte
De nombreux facteurs liés à l’hôte peuvent moduler la réponse immunitaire.
1) Âge au moment de la vaccination
- Le système immunitaire du corps humain est fonctionnel dès la naissance et persiste tout au long de la vie.
- Des différences dans la réponse immunitaire existent selon l’âge, particulièrement chez les très jeunes enfants (immaturité immunitaire chez les nourrissons) et les personnes âgées (immunosénescence).
a) Nouveau-nés prématurés
- La réponse immunitaire dépend de l’âge après la naissance, et non de l’âge gestationnel.
- Ainsi, un bébé né à 30 semaines de grossesse recevra ses premiers vaccins quand il atteindra l’âge de 2 mois, même si cet âge correspond à un âge gestationnel de 38 semaines.
b) nouveau-nés et nourrissons âgés de moins de 2 ans
La capacité du système immunitaire des enfants âgés de moins de 2 ans est très importante :
- Nombre élevé de lymphocytes naïfs disponibles.
- Capacité de générer jusqu’à 2 millions de lymphocytes T CD4+ chaque jour.
- Capacité de répondre à 10 000 antigènes différents simultanément.
Leur système immunitaire est immature :
- Forte proportion de lymphocytes B et T immatures.
- Centres germinatifs non encore présents dans les tissus lymphoïdes.
- Présence d’une réponse immunitaire aux antigènes T‑dépendants, mais production d’anticorps moindre que chez les enfants plus âgés.
- Absence de réponse immunitaire aux antigènes T‑indépendants, d’où l’absence de réponse ou la faible réponse aux vaccins polysaccharidiques.
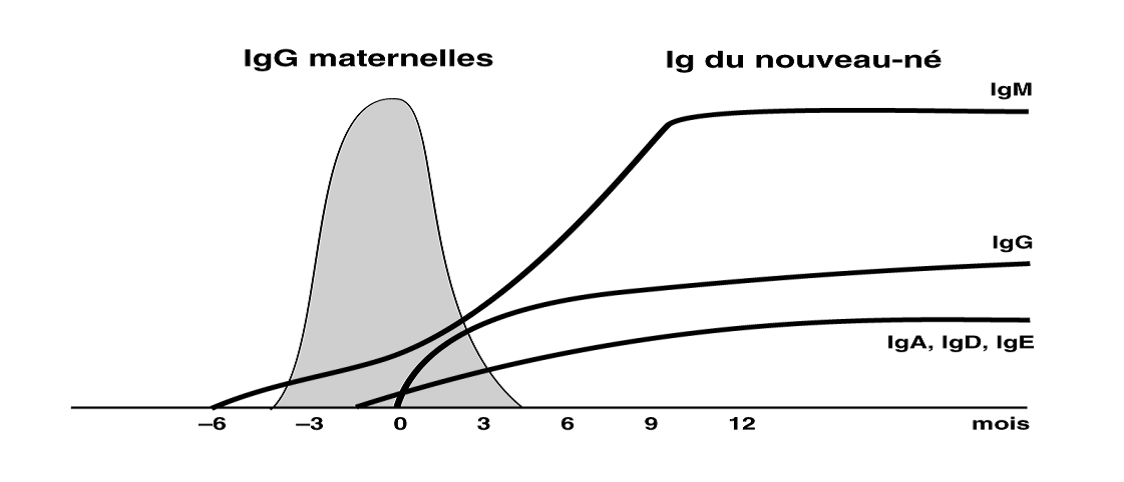
Les anticorps de la mère sont présents chez les nouveau‑nés :
- Ils sont transmis passivement in utero ou par l’allaitement.
- Ils peuvent avoir un effet inhibiteur sur la réponse immunitaire du nourrisson ; les calendriers de vaccination en tiennent compte.
- Ils protègent partiellement contre la varicelle, la poliomyélite, la rougeole, les oreillons, la rubéole, la gastroentérite à rotavirus, le tétanos, la diphtérie, la coqueluche et l’infection invasive à Hæmophilus influenzæ de type b.
c) Adolescents
- En général, cette période d’âge est celle où le système immunitaire répond le mieux.
d) Personnes âgées
- La capacité d’obtenir une bonne réponse immunitaire s’atténue au cours du vieillissement, car le pool des plasmocytes non différenciés diminue avec le temps.
2) Facteurs génétiques
- Les déterminants génétiques, tels que le système sanguin ABO et les antigènes d’histocompatibilité HLA, jouent un rôle dans l’immunité adaptative.
- Certaines personnes répondent mieux que d’autres aux vaccins.
- Par exemple, certaines personnes ne développent pas d’anticorps à la suite de la vaccination contre l’hépatite B, mais développent une réponse cellulaire qui assure leur protection.
3) Immunodépression
- Qu’elle soit acquise ou congénitale, l’immunodépression diminue généralement la réponse immunitaire humorale ou la réponse immunitaire cellulaire, ou les deux.
4) Malnutrition
- La malnutrition est associée à une altération de la fonction de la barrière intestinale et à un faible niveau des protéines du complément.
- Le tissu lymphatique, en particulier le thymus, subit une atrophie, et les réponses d'hypersensibilité de type retardé sont réduites.
- Les niveaux d'anticorps produits après la vaccination sont réduits chez les personnes gravement malnutries.
5) Obésité
- L’obésité est associée à des troubles métaboliques qui provoquent un dysfonctionnement tissulaire dans le tissu adipeux, le foie, le pancréas et les vaisseaux sanguins.
- Ces changements sont associés à un impact négatif sur l’immunité contre l’infection et sur l’efficacité vaccinale.1
Différents types de vaccins
Contrairement aux médicaments parfois synthétisés de manière artificielle, tous les vaccins contiennent au moins une partie du microbe naturel. Du microbe entier jusqu’à un simple gène pour l’hépatite B.
A) Classifications multiples
- Viral ou bactérien (parasitaire non disponible chez l’homme pour l’instant)
- Vivants ou inerte
- Inertes : entiers ou avec fraction antigénique (protéique, glucidique, anatoxine…)
- Selon le mode d’administration : intra-dermique, sous-cutanée, intra musculaire, oral, nasal.
- Selon le procédé de fabrication.
- Selon la réponse immunitaire déclenchée….
Découvertes progressives des différents types de vaccins au cours du 20ème siècle. Intérêt à connaître en pratique car on retrouve de nombreuses différences selon les types de vaccins :
- Modalités et âges d’administration
- Immunogénicité et surêté
- Mode de stockage
- Composition
- Contre-indications
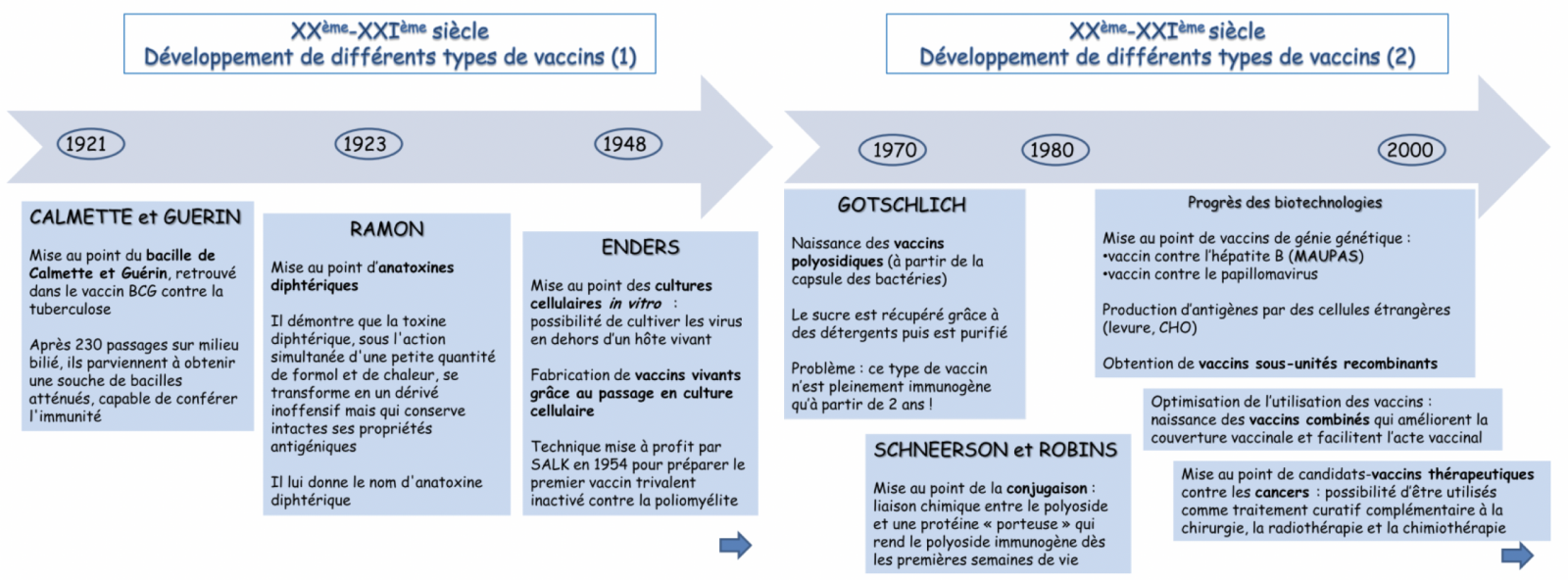
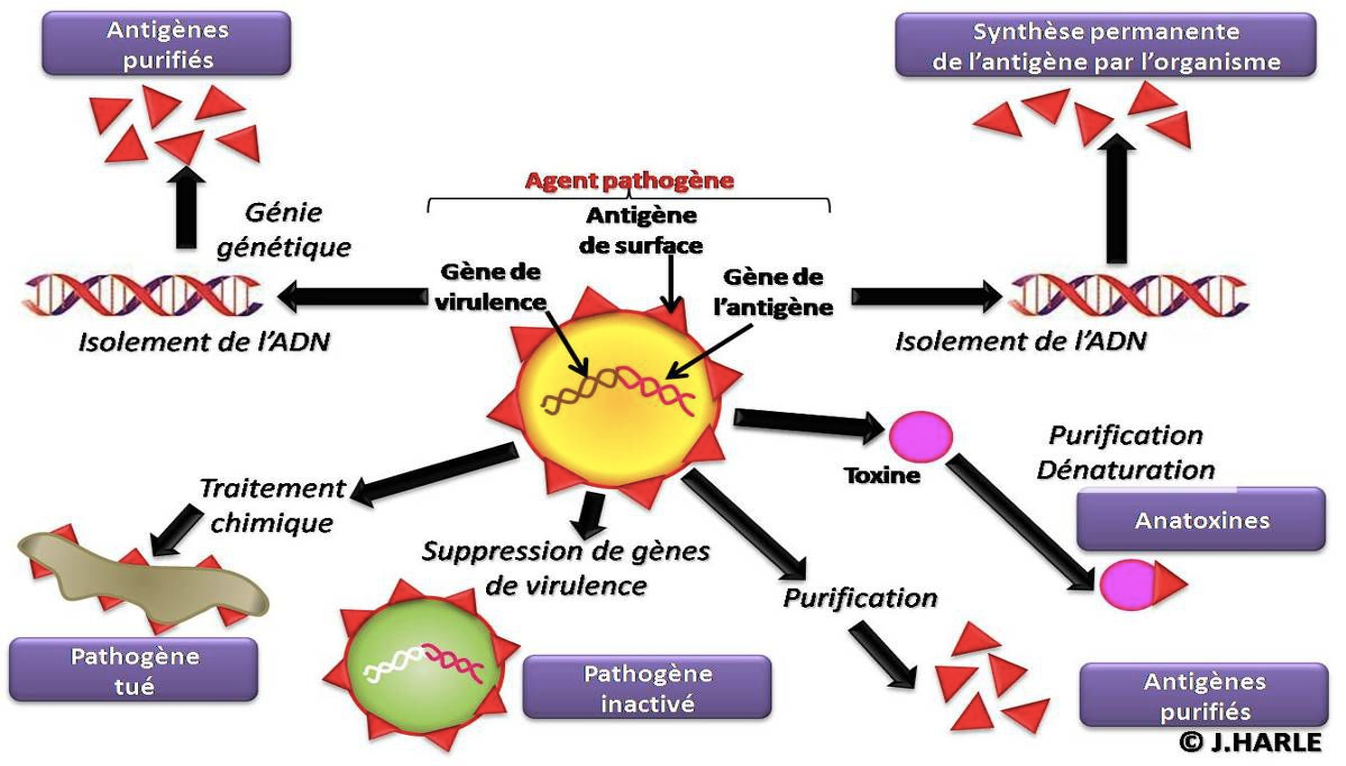
B) Vaccins vivants atténués
-
Il s'agit de souches d'agents infectieux atténuées ayant perdu tout ou partie de leur virulence par adaptation à une espèce animale nouvelle ou à la culture de cellules. Il s'agit de mutants avirulents ou peu virulents, qu'on a sélectionnés à force de passage en série chez le nouvel hôte (lapin, œufs embryonnés) ou en culture de cellules mais qui ont conservé la propriété de se multiplier chez l'hôte naturel et donc d'y induire une réponse immunitaire de longue durée. 1
- Ils entraînent une réponse à médiation humorale et cellulaire CD4+ et CD8+, proche de celle entrainée par l’infection.
- Ils miment la maladie, donc peuvent provoquent fièvre et symptômes après une période d’incubation identique (7 à 14 jours en moyenne).
- Ils n’ont jamais besoin d’adjuvants pour booster leur efficacité ou migrer vers les organes lymphoïdes.
- Ce sont les vaccins les plus efficaces et les plus durables.
- Risque très rare mais réel de retour à la virulence en cas d’immunodéficience.
- Contre-indiqués chez les femmes enceintes et les immunodéprimés.
- Vaccins à cible virale : rougeole, oreillons, rubéole, fièvre jaune, varicelle, zona, rotavirus, dengue, grippe nasale, variole.
-
Vaccin à cible bactérienne : BCG, Typhoïde
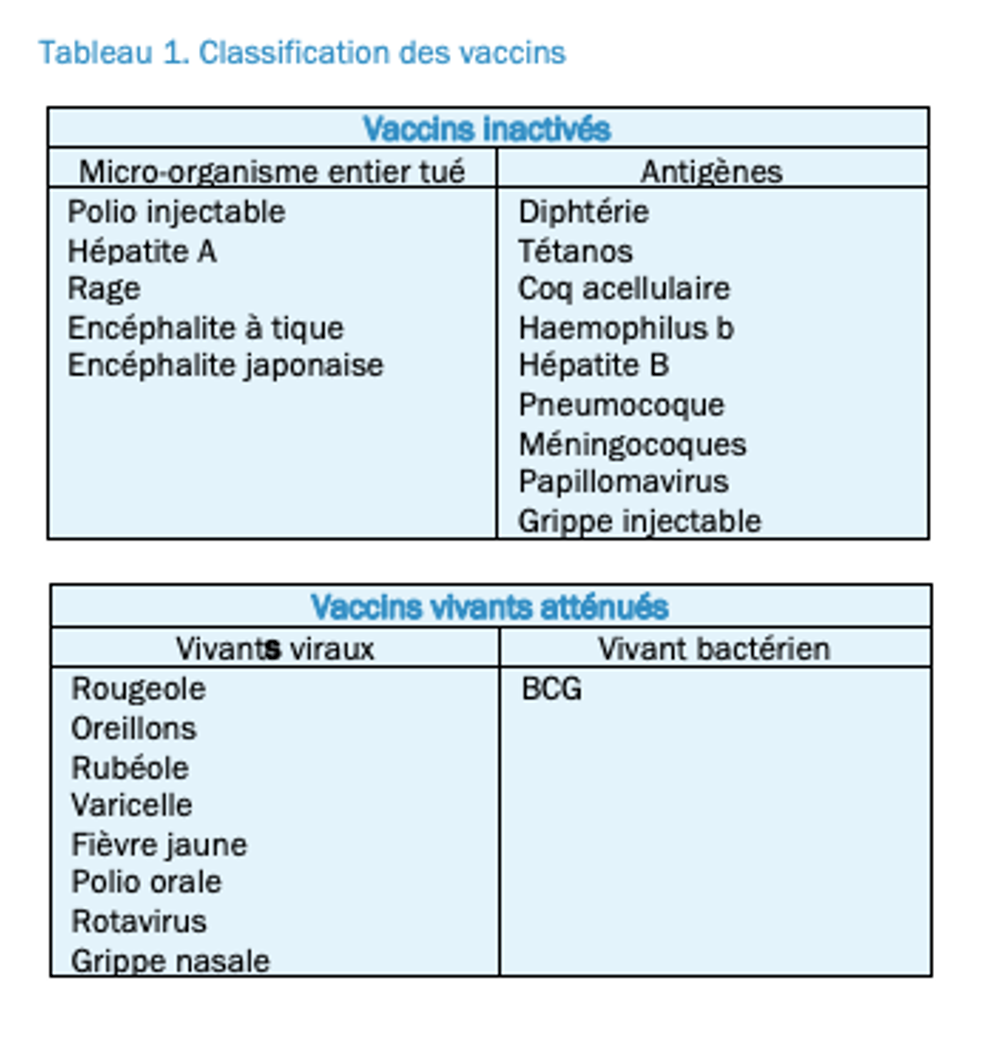
C) Vaccins inertes (inactivés) entiers
- Vaccins entiers à cible virale : Grippe, poliomyélite, hépatite A, encéphalite à tiques, encéphalite japonaise, rage.
- Vaccins entiers à cible bactérienne : un seul disponible (Leptospirose)
- Ils sont constitués d'agents infectieux dont on a supprimé toute virulence par inactivation chimique (formol, propiolactone) ou physique (rayonnements ou chaleur). Les micro-organismes inactivés ne sont plus capables de se multiplier, mais leurs protéines constitutives ont conservé leur pouvoir immunogène intact : inoculées à l'animal ou à l'Homme, elles provoquent une réponse immunitaire.
-
En général une seule administration de vaccin vivant atténué suffit pour parvenir à une immunité solide et durable, alors que les vaccins inactivés nécessitent plusieurs inoculations (rappels espacés dans le temps). De plus, il suffit d'inoculer une quantité minime de vaccin vivant (ce qui n'est pas surprenant puisque l'agent infectieux se multiplie dans l'organisme du sujet qu'on vaccine), alors qu'il faut des quantités importantes d'antigène inactivé pour conférer la même immunité.
- Les vaccins inertes viraux entrainent une réponse à médiation humorale avec participation des CD4+ (Ag T dépendant).
-
Ils ont besoin d’un adjuvant pour migrer vers les organes lymphoïdes et booster leur efficacité (augmenter leur immunogénicité).
-
Ils provoquent une réaction inflammatoire locale rapide (fièvre, douleur au point d’injection).
-
Pas de contre-indications durant la grossesse et chez les personnes immunodéprimées.
-
Le risque des vaccins inertes est plutôt d’être inefficace (puissance de l’Ag, âge, immunité).
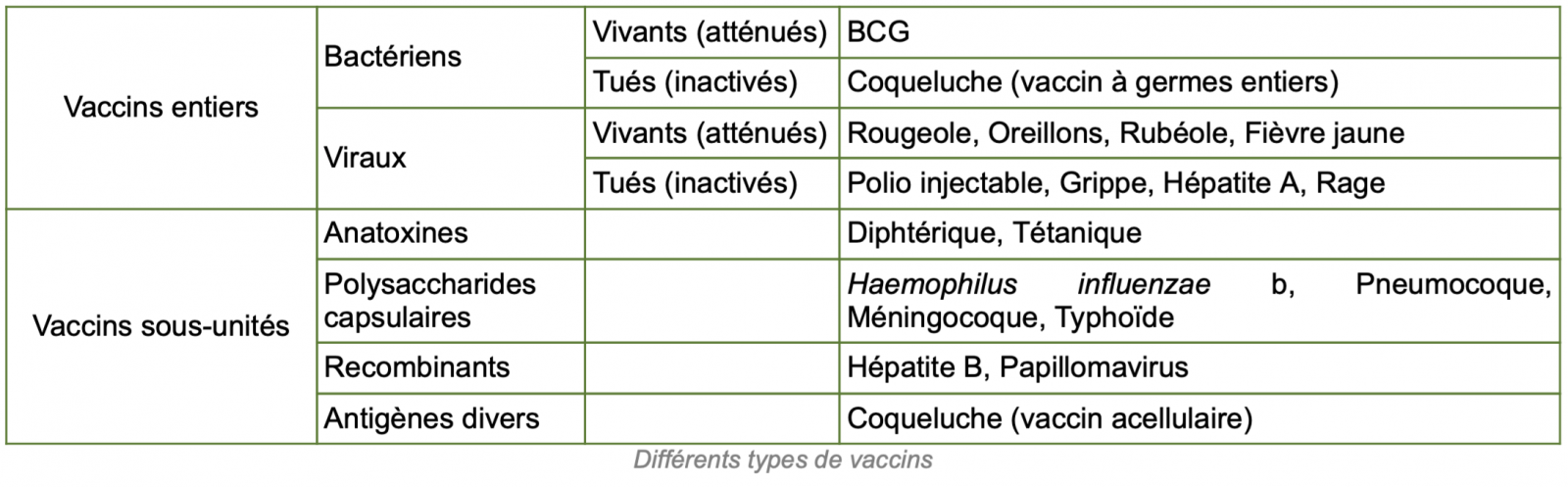
D) Vaccins sous-unitaires (fractionnés) :
- Il s'agit de vaccins contenant les antigènes spécifiques de l'agent infectieux après extraction et modification ou fabrication de novo.
- Réaction humorale Ag T dépendante sauf les polyosidiques non conjugués qui qui sont T indépendants (30 mois).
Les vaccins fractionnés peuvent être de nature :
- Protéique : extrait membranaire, anatoxine, fraction, sous-unité
- Glucidique = polyosidique : Antigène capsulaire. Les vaccins polyosidiques ont des propriétés éloignées de l’agent infectieux, en terme d’efficacité et de durée de protection. Ils sont parfois couplés à des protéines pour augmenter leur efficacité.1
1) Vaccins à cible bactérienne
- Toxine inactivée (= anatoxine) : diphtérie, tétanos. Lorsque les symptômes les plus graves de la maladie sont dus à la production de toxines par l'agent infectieux, il est possible de produire des vaccins uniquement à partir de ces toxines en les inactivant chimiquement ou par la chaleur (une toxine ainsi rendue inoffensive est alors fréquemment appelée un « toxoïde » ou plus généralement une « anatoxine »).
- Polysaccharides capsulaires non conjugués : pneumocoque 23 valences, méningocoque A-C, A-C-Y-W135, typhoïde
- Polysaccharides capsulaires conjugués à des protéines : pneumocoque 13 valences, méningocoque C, A-C-Y-W135, haemophilus influenzae de type b. Les vaccins anti-pneumocoque et la plupart des vaccins anti-méningocoque comportent plusieurs valences antigéniques du pathogène, permettant de vacciner contre plusieurs sérogroupes.
Le couplage à une protéine permet au vaccin d’avoir une immunogénicité augmentée.
- Sous-unités protéique : coqueluche acellulaire, méningocoque B. Un vaccin coquelucheux acellulaire est un vaccin qui ne contient pas de cellules bactériennes entières (contrairement à l'ancien vaccin coquelucheux dit « à germes entiers » qui entrainait de nombreux effets indésirables).
2) Vaccins à cible virale
- Protéines recombinantes : hépatite B, papillomavirus (HPV) : Ils sont obtenus par génie génétique. Le gène codant un antigène donné peut être introduit dans une bactérie, une levure ou une cellule animale, qui vont servir d' « usines biologiques » pour la synthèse de l'antigène. Ces antigènes « recombinants » sont ensuite purifiés et peuvent servir de base à des vaccins moléculaires aussi appelés vaccins sous-unités. Les vaccins contre les virus de l'hépatite B ou contre les papillomavirus sont ainsi constitués des protéines qui se trouvent naturellement à la surface de ces virus. 1 1

Fabrication et adjuvants
A) Un procédé de fabrication long et complexe - 6 à 22 mois
- Les vaccins sont composés de substances actives d'origine biologique.
- Ils sont fabriqués à partir des germes sur des milieux de culture principalement d’origine animale ou de synthèse qui apportent les nutriments nécessaires à leur développement.
-
Les vaccins se différencient des autres médicaments par l’origine biologique de leurs substances actives qui ne peuvent pas être synthétisées chimiquement.
- Les procédés de fabrication des vaccins sont souvent longs et complexes du fait de l’origine naturelle et non synthétique des substances actives.
- En effet, il faut entre six à vingt-deux mois pour produire un vaccin contre quelques semaines à six mois en général pour les médicaments chimiques.
-
De ce fait, ils présentent une variabilité de production importante, ce qui explique les difficultés rencontrées pour maîtriser la reproductibilité des procédés de fabrication.
-
70% du temps de fabrication sont consacrés aux contrôles de qualité et de sécurité qui sont effectués à chaque étape de la fabrication (Contrôle industriels ET par une autorité indépendante de l’ANSM).
B) Fabrication en deux étapes principales
Chaque type de vaccin est produit de manière spécifique mais leur fabrication suit, en général, les mêmes étape.
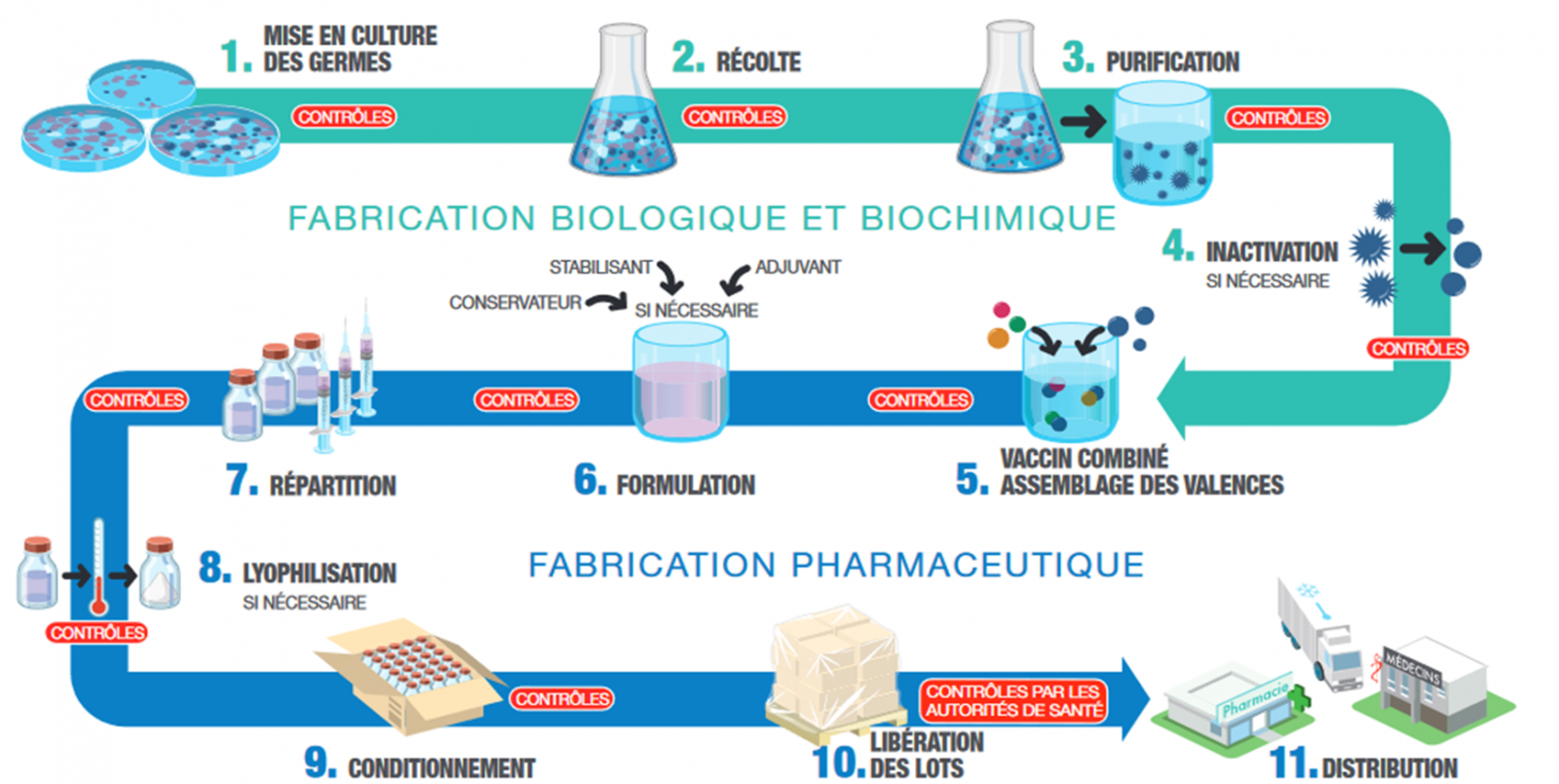
1) Fabrication biologique
- Constitution de la banque de germes.
- Production de la substance active :
- germe vivant atténué,
- germe ou fraction de germe inactivé
- Génie génétique pour obtenir antigène
- ➔ Conservation/stabilité, germes non mutants.
- Mise en culture et Amplification : sur milieux cellulaires, œufs de poule (grippe, fièvre jaune).
- Récolte de l’antigène produit. Extraction du milieu de culture.
- Purification et concentration : Supprimer toute impureté de la substance et à la concentrer grâce à des procédés physiques (centrifugation par exemple).
- Inactivation (chaleur, formaldéhyde) pour supprimer le pouvoir pathogène en gardant l’immunogénicité.
- Fabrication des valences antigéniques : cette étape consiste à rassembler les substances antigéniques actives en un seul composé.
2) Fabrication pharmaceutique
- 6. Assemblage des valences pour les vaccins combinés : exemple ROR
- 7. Formulation : ajout d’adjuvants, de stabilisateurs et de conservateurs.
- 8. Répartition aseptique : mise en flacon ou seringue en stérile.
- 9. Lyophilisation si nécessaire.
- 10. Conditionnement : étiquetage et mise en boîtes sous forme de lots homogènes (50 000 à 1 000 000 de doses selon les vaccins).
- 11. Contrôle et Libération des lots pour commercialisation. Les vaccins font l'objet d'un double contrôle, par le fabricant et par un laboratoire officiel indépendant qui est en France la Direction des contrôles de l'Agence nationale de sécurité du médicament et des produits de santé (ANSM).
- 12. Livraisons des lots dans les pharmacies/hôpitaux/centres de vaccinations.1

C) Les adjuvants
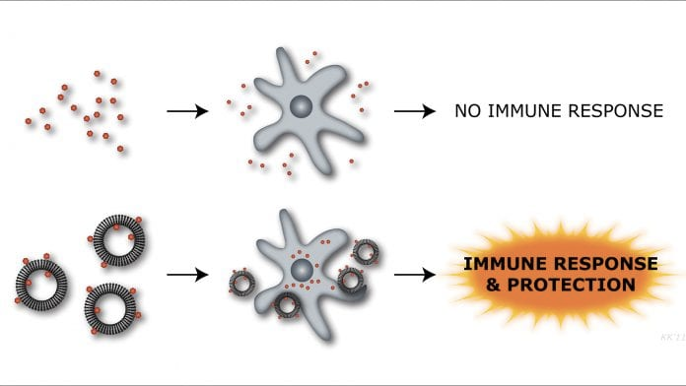
- Pour la majorité des vaccins inactivés, la présence d’adjuvants est indispensable pour permettre une réponse immunitaire entraînant une protection.
- Ils servent entre autres à donner le signal de danger à l’organisme pour que le système immunitaire soit activé.
- L’ajout d’adjuvant dans les vaccins permet, par ailleurs, de diminuer la quantité d’antigènes par dose vaccinale, et de réduire le nombre d’injections.
- Les vaccins vivants ne nécessitent pas d’adjuvants.
-
Les sels d’aluminium (phosphate et surtout hydroxyde d’aluminium) figurent parmi les adjuvants les plus utilisés dans le monde avec un recul d’utilisation de 90 ans et des centaines de millions de doses injectées.
-
Les données disponibles à ce jour issues d’études menées sur des vaccins contenant des sels d’aluminium ne remettent pas en cause leur innocuité, ni leur capacité à stimuler la réponse immunitaire induite par les vaccins.1 1
-
De nouveaux adjuvants pour de nouveaux vaccins ont été développés, notamment des émulsions et des phospholipides.D’autres sont en cours de développement. Des adjuvants à base de phosphate de calcium ont été développés dans les années 70 mais ont été abandonnés par la suite.Les données de la littérature n’avaient pas permis de conclure ni à une meilleure tolérance ni à une meilleure adjuvanticité.1

Effets secondaires
- Des centaines de millions de personnes sont vaccinées tous les ans en France et dans le monde.
- Comme pour tous les médicaments, les vaccins peuvent provoquer des effets indésirables (ou effets secondaires).
- La majorité des réactions vaccinales sont mineures et passagères, et les éventuels effets indésirables des vaccins sont très surveillés.
- Le risque de développer une maladie grave en ne se vaccinant pas est beaucoup plus important que celui de voir apparaître un effet indésirable lié à la vaccination.
A) Une histoire de sécurité
- La particularité d’un vaccin est qu’il s’adresse habituellement à des sujets en bonne santé, souvent jeunes (impliquant donc l’acceptation des parents).
- Son bénéfice individuel est différé et hypothétique, alors que son risque est le plus souvent immédiat.
- Le profil de sécurité d’emploi doit donc être excellent pour faire accepter la stratégie vaccinale.
- La population vaccinée est variée (du nourrisson à la personne âgée) et large, facilitant l’évaluation de la sécurité d’emploi à un temps donné et dans un groupe donné.
-
Avant tout commercialisation, on rappelle que durant la procédure de fabrication : 70% du temps sont réservés aux contrôles de sécurité. Puis, la commercialisation des vaccins obéit aux mêmes règles que celles qui sont appliquées aux médicaments.
-
La sécurité des médicaments et des produits biologiques est évaluée avant leur mise sur le marché, dans le cadre d’une procédure nationale ou européenne d’autorisation de mise sur le marché (AMM).1 Cette autorisation garantit que chaque patient reçoive des vaccins dont la qualité pharmaceutique, la sécurité d’emploi et l’efficacité sont démontrées et validées. L’AMM n’est délivrée qu’après une évaluation de la qualité pharmaceutique, de l’efficacité et de la tolérance (absence de danger aux doses utilisées) du vaccin.
-
Il existe quatre procédures d’autorisation des médicaments, trois procédures européennes et une procédure nationale.
B) Pharmacovigilance
- La sécurité d’emploi d’un nouveau médicament ne peut être totalement assurée par les études précliniques et les essais cliniques qui précèdent l’accord d’une AMM.
- La pharmacovigilance est donc indispensable pour assurer la sécurité d’emploi des médicaments – donc des vaccins – après leur mise sur le marché.
- Elle a pour objet la surveillance, l’évaluation, la prévention et la gestion du risque d’effet indésirable résultant de l’utilisation des médicaments et produits mentionnés à l’article L.5121-1 du Code de la santé publique.1
1) Organisation
- Le système de pharmacovigilance implique les professionnels de santé, les centres régionaux de pharmacovigilance (CRPV), les entreprises ou organismes exploitant les médicaments ainsi que les patients et associations agréées de patients.
- Il est coordonné par l’Agence nationale de sécurité du médicament et des produits de santé (ANSM).
- Plus précisément, il repose au niveau national sur le réseau des CRPV et les autres réseaux de vigilance, répartis sur l’ensemble du territoire national afin de favoriser les échanges de proximité avec les professionnels de santé ainsi que l’ensemble des déclarants, dont les patients.
- La pharmacovigilance repose notamment sur des notifications spontanées, adressées par les professionnels de santé à propos des effets indésirables médicamenteux dont ils ont connaissance, ainsi que par les patients et les associations de patients. Les notifications sont adressées soit directement au centre régional de pharmacovigilance dont il dépend géographiquement, soit via le portail de signalement des événements sanitaires indésirables du ministère chargé de la Santé.1
2) Echelon national et international
- L’ANSM recueille et centralise les informations relatives aux risques et utilisations susceptibles d’influer sur la sécurité du médicament, qu’elle qu’en soit la source. Elle examine et prend les mesures qui s’imposent afin de prévenir les risques ou de les réduire en vue d’assurer la sécurité d’emploi des médicaments dans le respect des procédures européennes et nationales.
- La pharmacovigilance s’inscrit également dans un cadre européen contraignant, visant à un large processus d’harmonisation. Elle repose sur le réseau des systèmes nationaux – dont les États-membres sont responsables –ainsi que sur les comités européens compétents.
- Une collaboration internationale est par ailleurs établie avec l’Organisation mondiale de la santé (OMS) ainsi que les autres autorités de santé (États-Unis, Japon, etc.).
C) Les effets indésirables des vaccins
- Les effets indésirables les plus fréquents sont une fièvre légère et une douleur ou une rougeur au point d’injection.
- Les effets indésirables graves sont très rares et font l’objet d’un suivi et de recherches approfondies lorsqu’ils surviennent.
- La déclaration des éventuels effets indésirables, qu’ils soient graves ou non, par les professionnels de santé et par les patients, permet de faire progresser en permanence la sécurité des vaccins.
1) Réactions locales post-vaccinales
- L’injection de matériel étranger dans les tissus et l’irritation des tissus par le processus d’injection peuvent produire une réaction inflammatoire. La réaction locale est donc un phénomène courant en vaccination.
- Les réactions locales observées sont habituellement une induration, de la douleur ou une sensibilité, une rougeur (érythème) et de la chaleur au point d’injection.
- Parfois, l’inflammation locale sera plus intense, par exemple après la 4e dose de la série vaccinale contre la diphtérie, la coqueluche et le tétanos chez les enfants. Même si la distinction peut parfois être difficile à faire cliniquement, il ne faut pas attribuer ces réactions plus fortes que ce qui était attendu, mais prévisibles et autolimitées, à une cellulite d’origine infectieuse (voir Réactions attribuables à une erreur), qui requiert l’administration d’antibiotiques. L’absence de fièvre ainsi que le bon état général contribueront à orienter le diagnostic.
- Des nodules sous-cutanés sont parfois observés durant quelques semaines ou parfois quelques mois, particulièrement à la suite de l’injection d’un vaccin contenant un adjuvant (ex. : sel d’aluminium). La maîtrise de la technique d’injection et l’utilisation de la longueur d’aiguille appropriée permettront de limiter ce genre de réactions.
2) Réactions systémiques post-vaccinales
- La plupart des manifestations systémiques sont non spécifiques, bénignes et transitoires. Elles peuvent être causées par des problèmes de santé courants au sein de la population sans être en lien avec le vaccin
- En général, après un vaccin inactivé, les réactions systémiques surviennent dans les 12 à 48 heures. Dans le cas des vaccins vivants atténués, elles peuvent survenir plusieurs jours après l’administration du vaccin en raison de la période d’incubation du micro‑organisme atténué. Par exemple, une éruption généralisée non contagieuse apparaissant dans les 5 à 12 jours chez 2 à 5 % des vaccinés avec le vaccin ROR.
- Les réactions systémiques après la vaccination varient en nature et en fréquence selon le vaccin administré : fièvre, malaise ou irritabilité, céphalée, éruptions, arthralgie ou myalgie, nausées, vomissements/diarrhée. Des convulsions fébriles surviennent rarement. D’autres symptômes du système nerveux central peuvent survenir exceptionnellement, par exemple une méningite ou une encéphalite après le vaccin vivant atténué RRO.
3) Syndrome hypotonie - hyporéactivité post vaccinale
- Diminution de l’état de veille ou perte de conscience avec pâleur et hypotonicité musculaire.
-
Peu fréquente, cette réaction a été décrite chez des enfants < 2 ans qui recevaient les vaccins entiers contre la coqueluche (et non acellulaires).
-
La réaction se produit de 1 à 12 heures après la vaccination.
-
Les enfants sont irritables au début et peuvent être fébriles.
-
Par la suite, ils deviennent pâles, hypotoniques et hyporéactifs. La respiration devient alors superficielle, et une cyanose peut être notée. En conséquence, les parents peuvent rapporter que l’enfant ne respirait pas.
-
Les épisodes sont autolimités et sont habituellement de courte durée (quelques minutes), bien qu’il puisse s’écouler jusqu’à 36 heures avant que l’enfant récupère complètement.
-
La cause de ces épisodes est inconnue, mais certains pensent qu’ils correspondent à des réactions vagales ou à des convulsions fébriles, mais atoniques.
-
Depuis l’utilisation des vaccins acellulaires contre la coqueluche, cette réaction est rarement signalée après la vaccination.1
4) Réactions d’hypersensibilité (ou réactions allergiques)
- Les réactions d’hypersensibilité, ou réactions allergiques, peuvent parfois expliquer certaines réactions locales ou systémiques observées après la vaccination.
- En dépit des limites liées à la complexité du système immunitaire, il s’est avéré utile de regrouper les réactions d’hypersensibilité selon quelques grandes familles. La classification traditionnelle de Gell et Coombs, qui propose 4 types de réactions d’hypersensibilité, demeure une référence classique en immunologie qui facilite la compréhension des réactions immunitaires, même si elle ne permet pas à elle seule d’expliquer complètement l’ensemble des phénomènes immunitaires.
a) Hypersensibilité de type I (allergie immédiate médiée par les immunoglobulines E)
Les réactions allergiques immédiates sont celles qui surviennent habituellement moins de 1 heure après la vaccination. Elles sont souvent déclenchées par des anticorps spécifiques IgE résultant d’une sensibilisation antérieure à l’un des composants du produit.
+ Anaphylaxie
- La réaction la plus grave est l’anaphylaxie, qui constitue une urgence en vaccination. L’anaphylaxie survient exceptionnellement après une vaccination, de moins de 1 sur 100 000 à 1 sur 1 million de doses distribuées. Un traitement efficace (adrénaline) est disponible.
- La personne qui a présenté une anaphylaxie dans les 24 heures suivant de l’administration d’un vaccin devrait être dirigée vers une clinique spécialisée qui déterminera si elle peut être vaccinée de nouveau avec ce vaccin ou avec un vaccin ayant un composant identique. En attendant cette évaluation, l’administration du vaccin ou de l’autre produit ayant un composant identique est contre-indiquée.
- Si une anaphylaxie survient plus de 24 heures après l’administration d’un vaccin, elle n’est pas attribuée à celui-ci, et la personne peut être revaccinée.
+ Urticaire (ou autre réaction d’hypersensibilité)
- Une urticaire généralisée, sans autres symptômes, qui survient après la vaccination est compatible avec une hypersensibilité de type I. Cependant, la probabilité que l’urticaire généralisée soit une hypersensibilité de type I est à considérer seulement si elle commence moins de 1 heure après la vaccination. L’urticaire est alors considérée comme une précaution (voir Vaccinologie pratique, Précautions).
- La personne qui a présenté une urticaire moins de 1 heure après l’administration d’un vaccin devrait être dirigée vers une clinique spécialisée qui déterminera si elle peut être vaccinée de nouveau avec ce vaccin ou avec un vaccin ayant un composant identique.
- On peut poursuivre la vaccination d’une personne qui a présenté une urticaire généralisée plus de 1 heure après un vaccin ou une urticaire localisée sans autre investigation. De même, les éruptions cutanées autres que l’urticaire ne sont généralement pas des réactions d’hypersensibilité de type I, et la vaccination peut être poursuivie.
b) Hypersensibilité de type II (ou réactions par anticorps cytotoxiques)
- Dans ces réactions, l’antigène se fixe à la membrane de certaines cellules et forme un antigène combiné. Des anticorps cytotoxiques sont produits et entraînent la destruction et la lyse de cet antigène combiné.
- Ces réactions sont surtout liées aux cytopénies médicamenteuses et aux accidents de transfusion dus à l’incompatibilité. Il n’y a pas d’exemple connu en vaccination.
c) Hypersensibilité de type III (ou réactions par complexes immuns)
- Ces réactions sont dues à la formation et à l’accumulation d’un trop grand nombre de complexes immuns, qui sont la combinaison d’un antigène et d’un anticorps. Cela provoque une réaction inflammatoire intense et des dommages tissulaires.
- En vaccination, les réactions locales importantes qui débutent de 2 à 8 heures après l’injection et qui surviennent à la suite de l’administration répétée des anatoxines diphtérique et tétanique sont des réactions par complexes immuns.
- Ces réactions n’empêchent généralement pas la poursuite de la vaccination. Toutefois, on évitera la revaccination contre la diphtérie et le tétanos plus souvent que tous les 10 ans chez les personnes ayant présenté une telle réaction.
d) Hypersensibilité de type IV (ou réactions retardées médiées par les lymphocytes)
- Ces réactions ne sont pas produites par des anticorps, mais par les lymphocytes T. Ce sont des réponses immunitaires à médiation cellulaire.
- Elles apparaissent dans un délai de 24 à 72 heures après la réintroduction de l’antigène dans l’organisme, d’où le nom de réaction retardée. Elles se manifestent par une inflammation localisée au point d’injection pouvant aller jusqu’à une nécrose locale. Les exemples classiques sont les réactions tuberculiniques, les rejets de greffe et les dermites de contact.
- Une dermite de contact survenue à la suite de l’application topique d’un médicament trouvé aussi dans un vaccin (néomycine, streptomycine, agents de conservation, dont le thimérosal) n’est pas une contre-indication de la vaccination.
5) Réactions attribuables à une erreur
Des réactions indésirables peuvent être attribuables à une erreur. Les types d’erreurs sont multiples, par exemple :
- Administration d’un produit inapproprié à l’âge de la personne.
- Administration faite sans tenir compte des précautions ou des contre-indications.
- Utilisation d’un mauvais diluant pour reconstituer un vaccin lyophilisé.
- Injection à un mauvais site d’injection (ex. : vaccin dans le muscle dorsofessier).
- Mauvaise voie d’administration (ex. : SC au lieu d’IM).
- Mauvaise posologie.
- Mauvais calendrier vaccinal.
- Contamination du produit, du point d’injection ou du matériel utilisé.
Les manifestations cliniques varient selon l’erreur d’immunisation, par exemple :
- Si la technique d’injection IM d’un vaccin adsorbé est imparfaite, une réaction inflammatoire plus importante peut survenir au point d’injection. Cette réaction est due à l’écoulement dans les tissus sous‑cutanés du sel d’aluminium contenu dans le vaccin. On a même rapporté des abcès stériles.
- Un abcès ou une cellulite d’origine infectieuse peut survenir à la suite de l’introduction de micro‑organismes lors de l’injection ou à la suite de la contamination de la fiole de vaccin.
Ces erreurs doivent être divulguées à la personne vaccinée, qu’elles entraînent des manifestations cliniques ou non (Déclaration d’incident ou d’accident).
Une MCI qui survient à la suite d’une erreur doit aussi être déclarée à la DSPublique de sa région au moyen du formulaire prévu à cet effet (Formulaire de déclaration).
L’administration d’un vaccin non indiqué fait partie des erreurs de vaccination, car une manifestation clinique indésirable peut survenir même si aucun avantage n’est retiré du vaccin. Par exemple, un voyageur ayant reçu le vaccin FJ a subi une réaction systémique grave (maladie vaccinale viscérotrope), alors qu’il se rendait à une destination où il n’y avait aucun risque de fièvre jaune.1
6) Exemple effets indésirables
a) Vaccins Hexavalents
- Dans 5 à 15 % des cas, une réaction locale (rougeur, tuméfaction, douleur au point d’injection) ou une réaction plus générale (par ex : fièvre généralement inférieure à 39°). Ces réactions se manifestent 24 à 48 heures après la vaccination et disparaissent très vite.
-
Environ un nourrisson sur 1000 pleure et reste inconsolable durant quelques heures après la vaccination.
- Des convulsions fébriles ont été rapportées essentiellement après la dose de rappel.
- Dans de très rares cas, chez des enfants prédisposés, une réaction allergique à certains composants du vaccin. Ceci se manifeste en général par une rougeur généralisée de la peau et/ou des démangeaisons.
- Une tuméfaction au point d’injection : elle disparaît en quelques jours.
- D’autres problèmes sont parfois signalés après vaccination, mais ils restent exceptionnels : 1 cas pour 100 000 ou pour 1 million. Il est donc très difficile desavoir si le vaccin est en cause ou s’il s’agit d’une coïncidence.1
b) ROR
- Les vaccins ROR ont été développés de façon à avoir la meilleure efficacité et la meilleure tolérance possible.
- Une réaction cutanée au point de la piqûre est possible, mais rare.
- Environ 1 enfant sur 10 réagit avec de la fièvre, parfois (2-4 cas sur 100) avec des plaques rouges sur la peau ou un gonflement des glandes salivaires. Lorsque ces réactions surviennent, elles apparaissent environ 7 à 12 jours après la vaccination.
- Si la fièvre est très élevée, elle peut provoquer une convulsion fébrile chez environ 1 enfant sur 3 000: il est donc important de contrôler la température de l’enfant vacciné.
- Le vaccin ROR peut provoquer une thrombopénie transitoire (environ 1 enfant sur 30 000), avec un risque de saignements (hématomes sous la peau en particulier), – mais le risque de développer cette complication suite à la vaccination est beaucoup plus rare que le risque qui existe si on attrape la rougeole ou la rubéole (1 enfant sur 1 000).
- Les effets indésirables graves sont extrêmement rares (moins de 1 par million). D’autres problèmes ont été rapportés après ces vaccinations, mais si rarement (moins de un par cent mille ou par million) qu’il est difficile de déterminer si le vaccin est en cause ou non.
- Les vaccins ROR ne surchargent pas le système immunitaire et n’augmentent pas le risque de développer des allergies, de l’autisme, des maladies inflammatoires ou autoimmunes.1
c) BCG
Peu fréquent (> 1/1000, < 1/100) :
- Réaction générale : céphalée, fièvre
- Réaction locale : ganglion lymphatique régional > 1 cm, ulcération avec suppuration au site d'injection
Rare (< 1/1000) :
- Réaction générale : complication par dissémination du BCG telle que ostéite ou ostéomyélite
- Réactions allergiques incluant des réactions anaphylactiques
- Réaction locale : lymphadénite suppurative, abcès
- Quelques cas de syncope, d'épilepsie et de convulsion ont été rapportés lors de la surveillance après la commercialisation.1
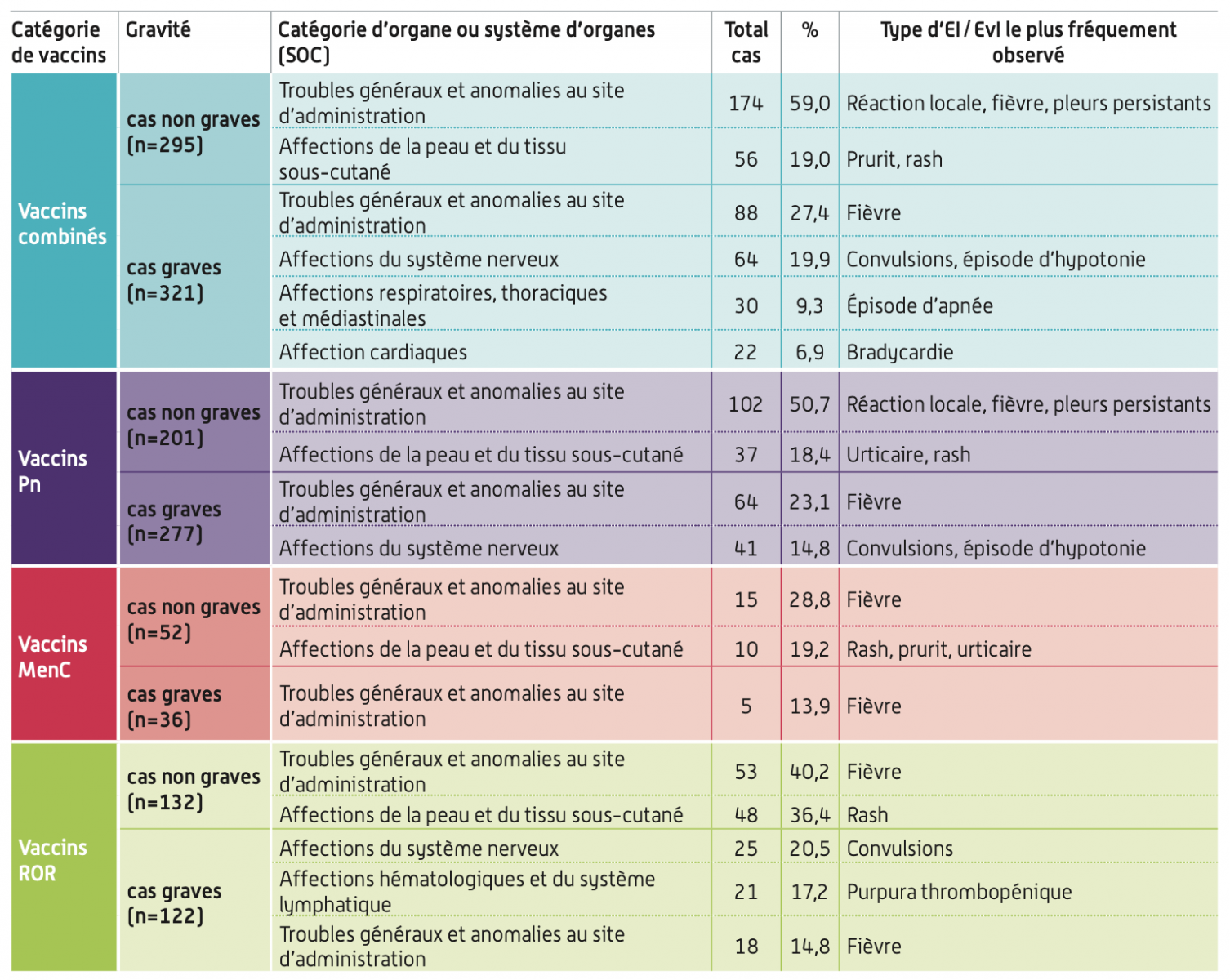

Rappels de voies d’administration des vaccins. Le vaccin doit être administré de préférence par voie sous-cutanée chez les patients présentant une thrombocytopénie ou un trouble de la coagulation.
LÉGISLATION ET RÉGLEMENTATION
A) Obligation vaccinale en france : une histoire ancienne.
- 1902 : En France, la vaccination contre la variole est rendue obligatoire chez l'enfant en 1902, et il est prévu de la répéter aux âges de 11 ans et 21 ans. Obligation suspendue en 1984 par l’OMS après éradication de la maladie.
- 1938-1940 : Diphtérie et tétanos.
- La vaccination diphtérique est obligatoire depuis la loi du 25 juin 1938, modifiée par les lois du 7 septembre 1948 et du 12 août 1966 (obligation de la primovaccination et du rappel avant l’âge de 18 mois). Les rappels ultérieurs sont recommandés.
- La vaccination tétanique est obligatoire en France pour les enfants de moins de 18 mois depuis la loi du 24 novembre 1940.
- 1950 : La vaccination BCG a été rendue obligatoire en 1950 mais suspendue en 2007 dans notre pays compte tenu de l’évolution de son épidémiologie dans notre pays. Depuis, la vaccination BCG est ciblée et recommandée pour les sujets à risque.
- 1964 : La vaccination contre la Poliomyélite elle a été rendue obligatoire en juillet 1964, avec des rappels de vaccination obligatoires qui doivent être terminés avant l'âge de 13 ans. .
- 1967 : Depuis 1967, l'entrée en Guyane est subordonnée à la présentation d'un certificat de vaccination antiamarile (fièvre jaune) à jour ou d'un certificat de contre-indication médicale à cette vaccination (article R3115-63 du code de la santé publique).
- Ainsi, jusqu’en 2017, l’obligation vaccinale en France métropolitaine portait sur trois vaccins, diphtérie, tétanos et polio (schéma comportant primovaccination et rappel avant 18 mois, les rappels polio étant obligatoires jusqu’à 13 ans)
B) Naissance de la nouvelle obligation vaccinale de 2018
C’est en 2013 et 2014, suite au rapport du Haut conseil de la santé publique sur l’obligation vaccinale que le débat va être lancé dans notre pays.

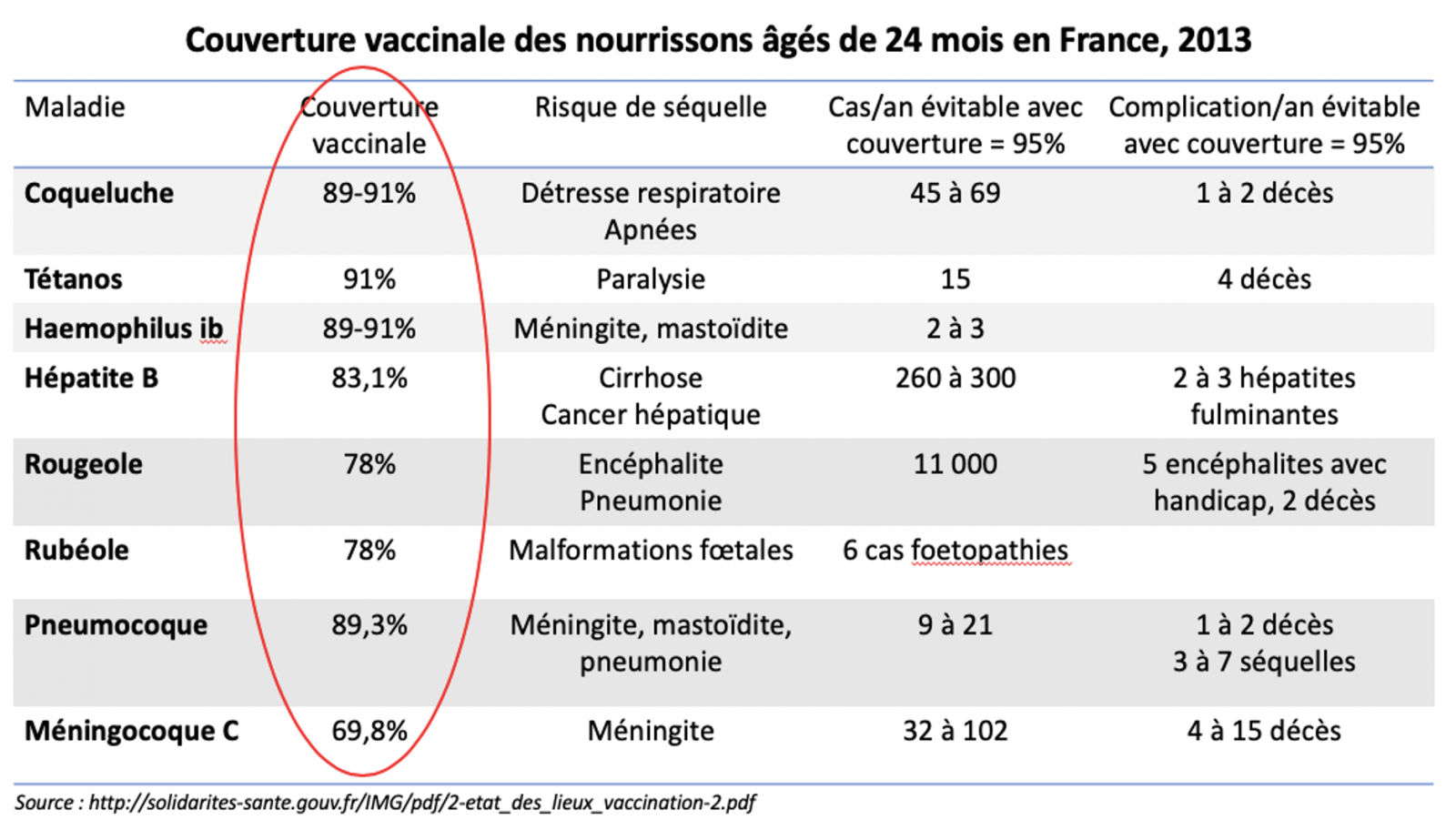
1) En 2013 et 2014 Rapport du Haut Conseil de la Santé Publique (HCSP).
Selon cet avis, l’obligation vaccinale pour DTP en France ne serait :
- Ni pertinente en terme de morbi-mortalité.
- Ni cohérente, puisque les adultes représentent désormais la quasi-totalité des cas résiduels de ces maladies et ne sont pas concernés par l’obligation.
- Ni justifiée par la couverture vaccinale de ces trois maladies qui est très bonne.
- Ni compréhensible par la population, pensant que les vaccins recommandés ne sont pas importants.
- Ni loyale depuis la disparition du vaccin DTP non adjuvé, formulation trivalente adaptée au nourrisson c’est-à-dire suffisamment dosée en anatoxines diphtérique et tétanique.
2) En 2015 : difficultés à statuer
- Il apparaissait alors que selon la législation en vigueur du code de santé publique, le caractère obligatoire était difficilement applicable dans notre pays.
- Sur le plan juridique, l’obligation vaccinale relève en effet du code de la santé publique selon les articles L.3111-2 et L.3111-3 modifiés par lois 2004 et 2007.
Selon le code de SP et ces articles, on pouvait noter :
- Indemnisation des effets secondaires de ces 3 vaccins obligatoires à 100 % par l’État sans que le patient ait à fournir la preuve de la relation causale.
- Possibilité de sanctions en cas de refus (article L.3 111-9 modifié par loi 2008).
- Mais l’article du même code sur le droit des patients (2002), jette une confusion puisque le refus de vaccination y apparaît clairement autorisé (L.1 111-2 modifié par loi 2016).
3) En 2015 : avancée du débat et prise de position du conseil constitutionnel
Ce qui a fait avancer le débat :
- Procédures juridiques entre Etat et familles refusant de vacciner leurs enfants à l’entrée en crèche.
- Le Conseil Constitutionnel stipule le 20 mars 2015 que les lois de Santé Publique relatives à l’obligation vaccinale sont conformes à la Constitution. Seuls des motifs médicaux vrais exonèrent de cette obligation.
- Selon cet avis, le droit de toute personne à refuser un traitement s’efface donc devant l’obligation vaccinale.
4) 2016 : accélération du débat
- Remise du rapport Hurel à la ministre de la santé,
- Annonce par le ministre de la santé du plan d’action pour une rénovation de la politique vaccinale,
- Nombreuses prises de position des sociétés savantes et des académies en faveur de l’obligation vaccinale,
- Grande concertation citoyenne coordonnée par le professeur Alain Fisher, dont le comité d’organisation conclura à la nécessité non pas de supprimer les obligations vaccinales mais de les élargir, temporairement, à l’ensemble du calendrier vaccinal du nourrisson.1
Le rapport hurel met en évidence:
- La différenciation entre vaccins obligatoires et recommandés est non pertinente.
- La politique vaccinale aboutit à des résultats contrastés.
- L’adhésion à la vaccination ne peut pas être considérée comme acquise d’emblée. Une information et une communication régulière sur les sujets relatifs à la vaccination sont indispensables à l’adhésion des professionnels de santé et du public concerné.
- Les obligations vaccinales de chaque pays doivent être étudiées en y intégrant les obligations relatives à l’entrée en collectivité.
- La mise en œuvre de la politique vaccinale suppose de prendre en compte la question de la disponibilité des vaccins.
- Avant tout choix entre obligation et recommandations vaccinales, un débat public et une conférence de consensus sont indispensables.
5) En 2016 et 2017
- Une concertation des sociétés savantes et citoyennes, sous l’égide du Pr Fischer, conclut à l’élargissement de l’obligation vaccinale à certains vaccins recommandés.
- Des groupes d’opposants à la vaccination demanderont alors à la ministre de la Santé de rendre disponible des vaccins correspondant uniquement aux trois obligations.
- Cette demande sera rejetée par la ministre en février 2016 et le conseil d’État sera alors saisi de la question.
- Sa décision sera publiée le 8 février 2017 et comportera plusieurs réponses.
Réponse publiée en février 2017 du conseil d’état aux opposants à la vaccination :
- Il écarte toute argumentation des requérants sur les risques allégués des vaccinations non obligatoires en jugeant qu’aucun élément sérieux n’est apporté sur l’existence d’un risque d’atteinte à l’intégrité de la personne et de la mise en danger d’autrui.
- Il stipule que les pouvoirs du ministre doivent lui permettre dans les six mois de mettre à disposition une formulation vaccinale limitée aux trois vaccins obligatoires.
6) Fin du débat : 2017
- Dans ces conditions, il apparaît donc que la seule solution possible pour nos autorités sanitaires était de faire évoluer la législation en élargissant le champ des vaccinations obligatoires ce qui revient aux mêmes conclusions que celles du comité d’orientation de la concertation citoyenne.
- La loi d’extension de l’obligation vaccinale en France est promulguée le 30 décembre 2017 et applicable pour les nourrissons nés à partir du 1er janvier 2018.
7) Naissance de la nouvelle obligation vaccinale de 2018
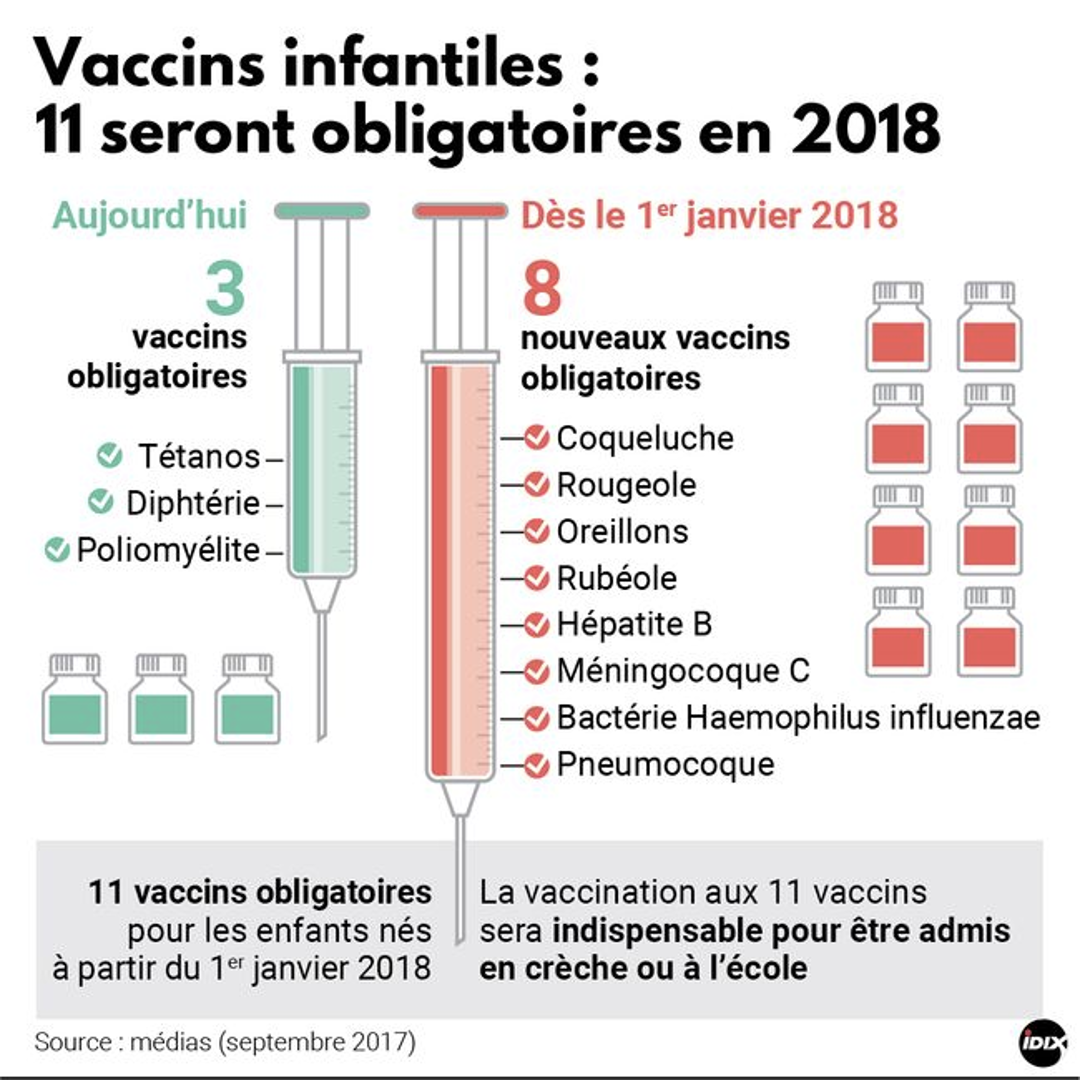
8) Quels risques pour les refus de vaccins ?
- La sanction pénale spécifique au refus de vaccination est supprimée.
- Cependant, parce que ne pas faire vacciner son enfant le met en danger et peut mettre en danger les autres, le fait de compromettre la santé de son enfant, ou celle des autres, pourront toujours faire l’objet de poursuites pénales.
- Il est conseillé aux vaccinateurs de noter, dans le dossier médical papier ou dans le logiciel de gestion du cabinet, les oppositions aux vaccinations de la part des titulaires de l’autorité parentale, l’information donnée sur l’utilité des vaccins et leur caractère obligatoire pour les enfants nés à partir du 1er janvier 2018.
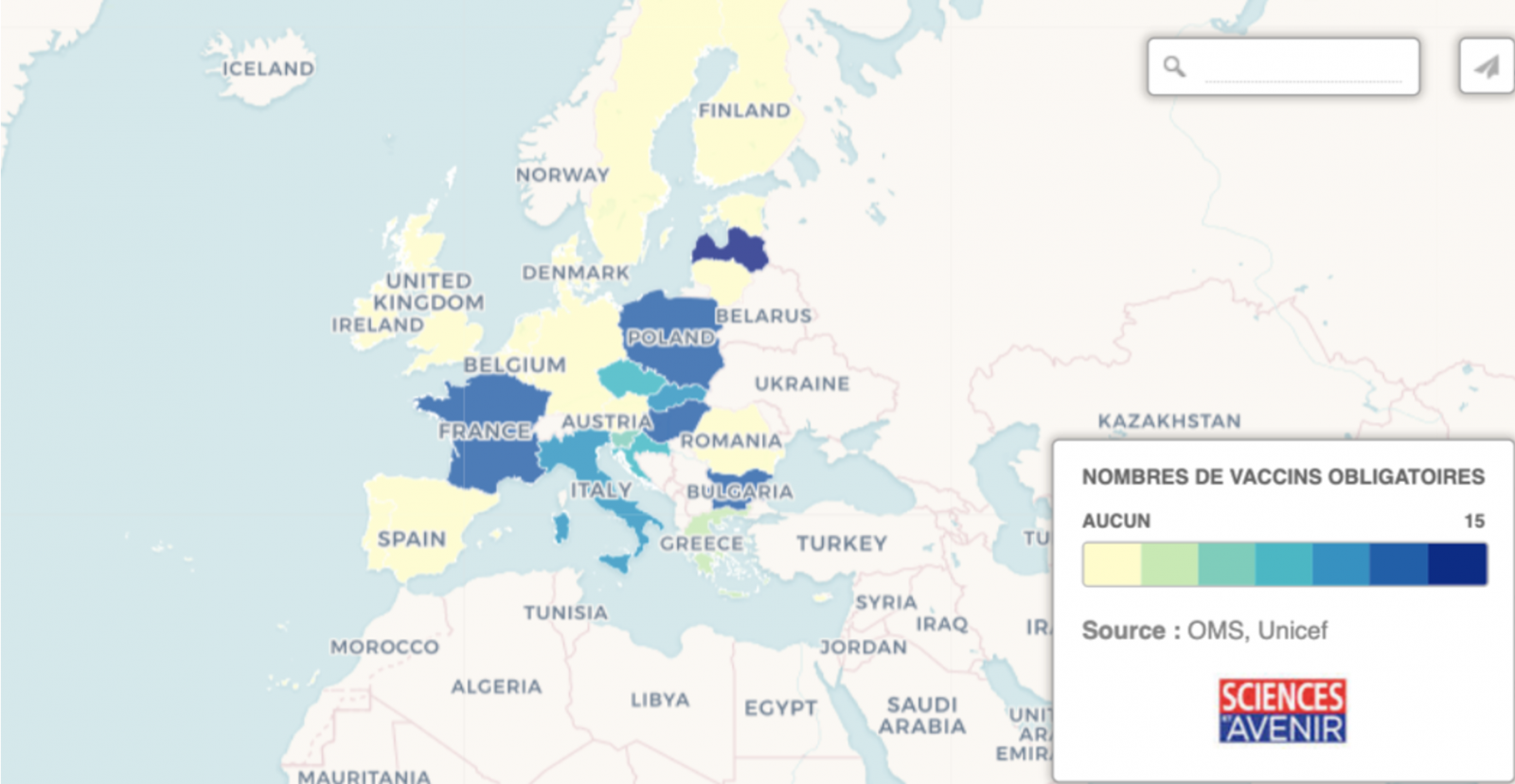
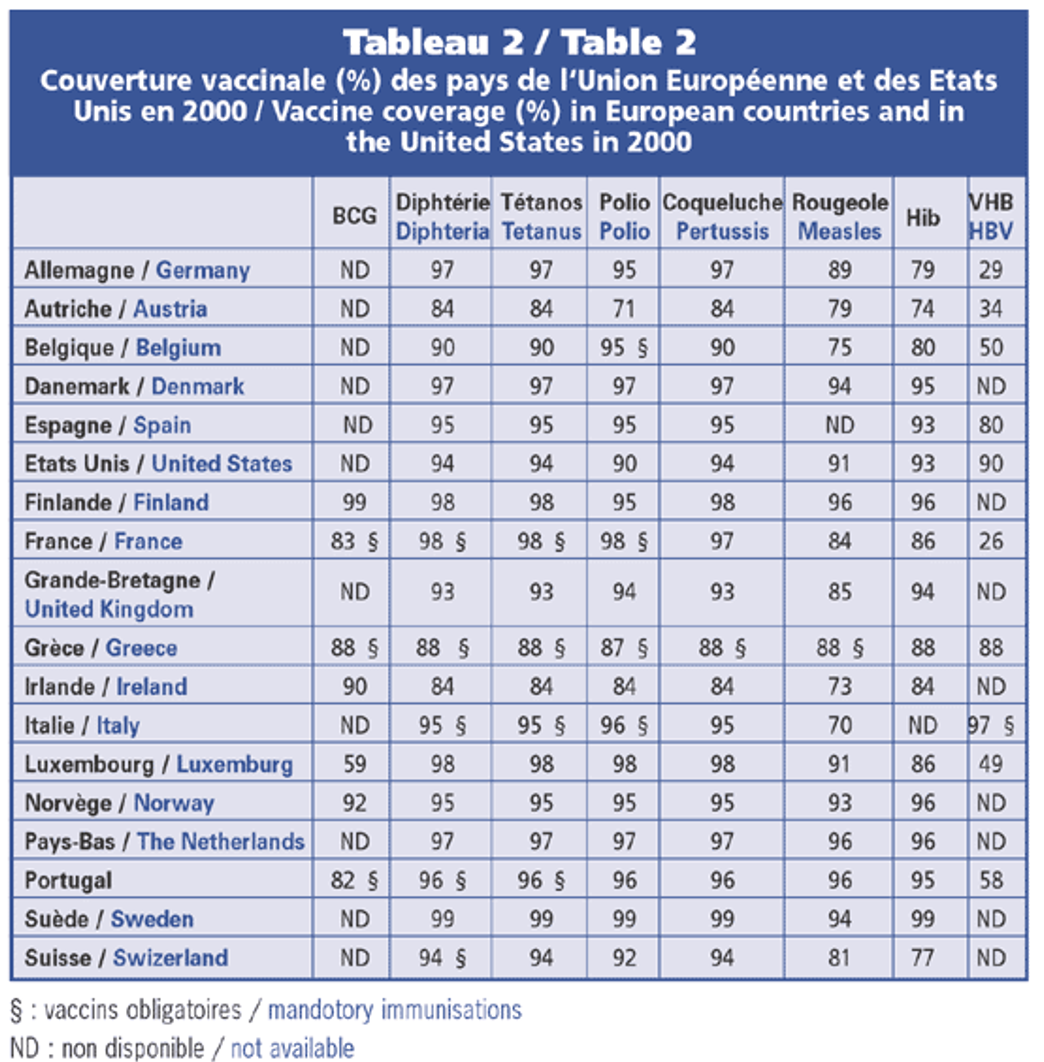
C) Obligation vaccinale en Europe 1
- En Europe, les politiques vaccinales ne sont pas homogénéisées.
- Chaque pays européen dispose de son propre calendrier vaccinal pour les enfants de moins de 2 ans.
- Certains passent par l’obligation légale pour garantir une couverture vaccinale optimale, d’autres se contentent d’une recommandation.
-
Les pays du Nord et les pays scandinaves n’ont pas d’obligation, mais les couvertures vaccinales sont excellentes. La seule exception est la Belgique qui a maintenu l’obligation vaccinale uniquement pour la polio.
-
Les pays du sud et de l’est de l’Europe ont quant à eux des obligations vaccinales, à l’exception de l’Espagne. Les couvertures vaccinales sont faibles pour les vaccins seulement recommandés.1
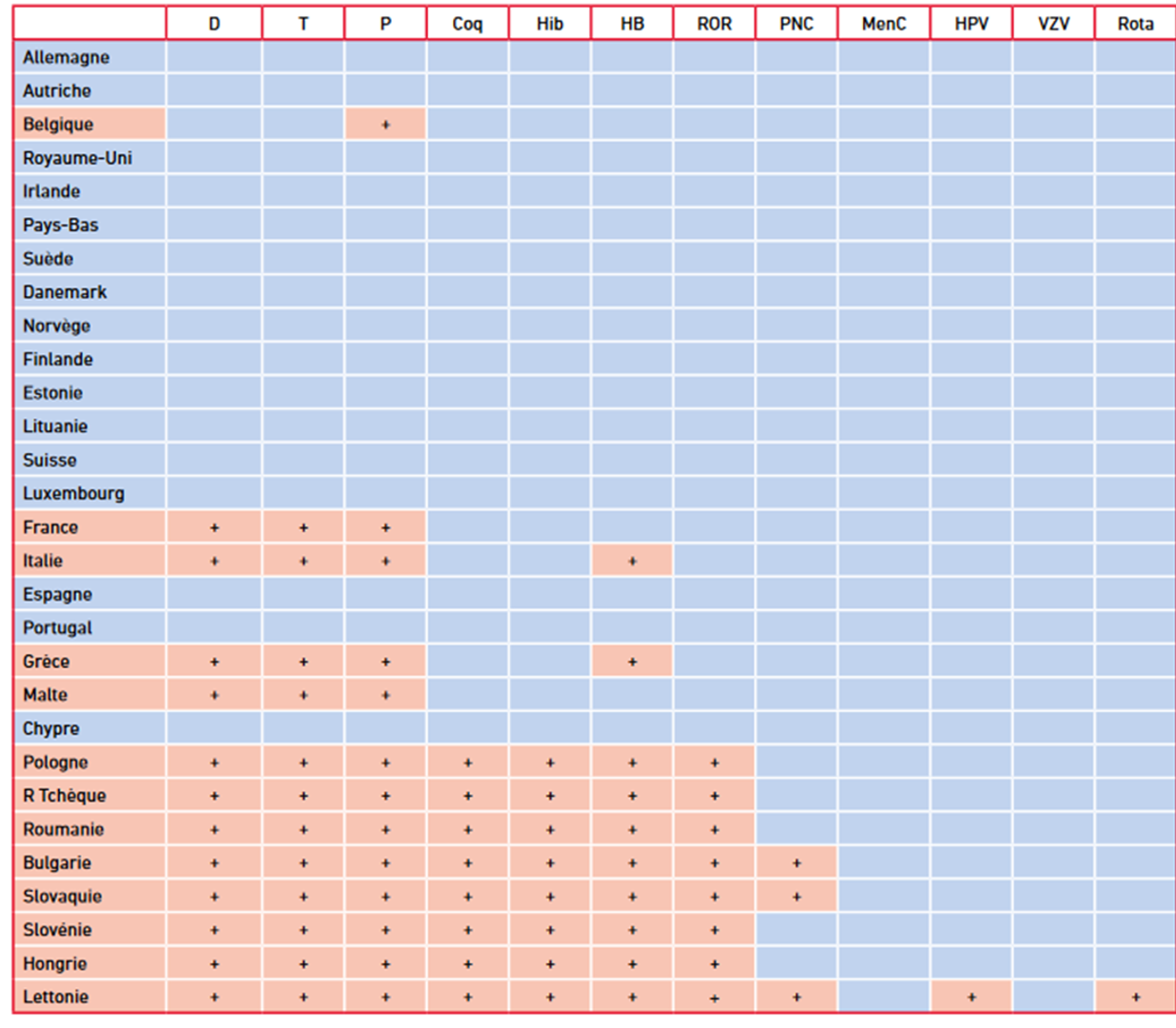
Calendrier vaccinal 2020
- L’article L. 3111-1 du code de la santé publique (CSP) dispose que : « la politique de vaccination est élaborée par le ministre chargé de la santé qui fixe les conditions d’immunisation, énonce les recommandations nécessaires et rend public le calendrier des vaccinations après avis de la Haute autorité de santé ».
- Le calendrier des vaccinations : fixe les vaccinations applicables aux personnes résidant en France en fonction de leur âge, émet les recommandations vaccinales « générales » et des recommandations vaccinales « particulières » propres à des conditions spéciales (risques accrus de complications, d’exposition ou de transmission) ou à des expositions professionnelles.1
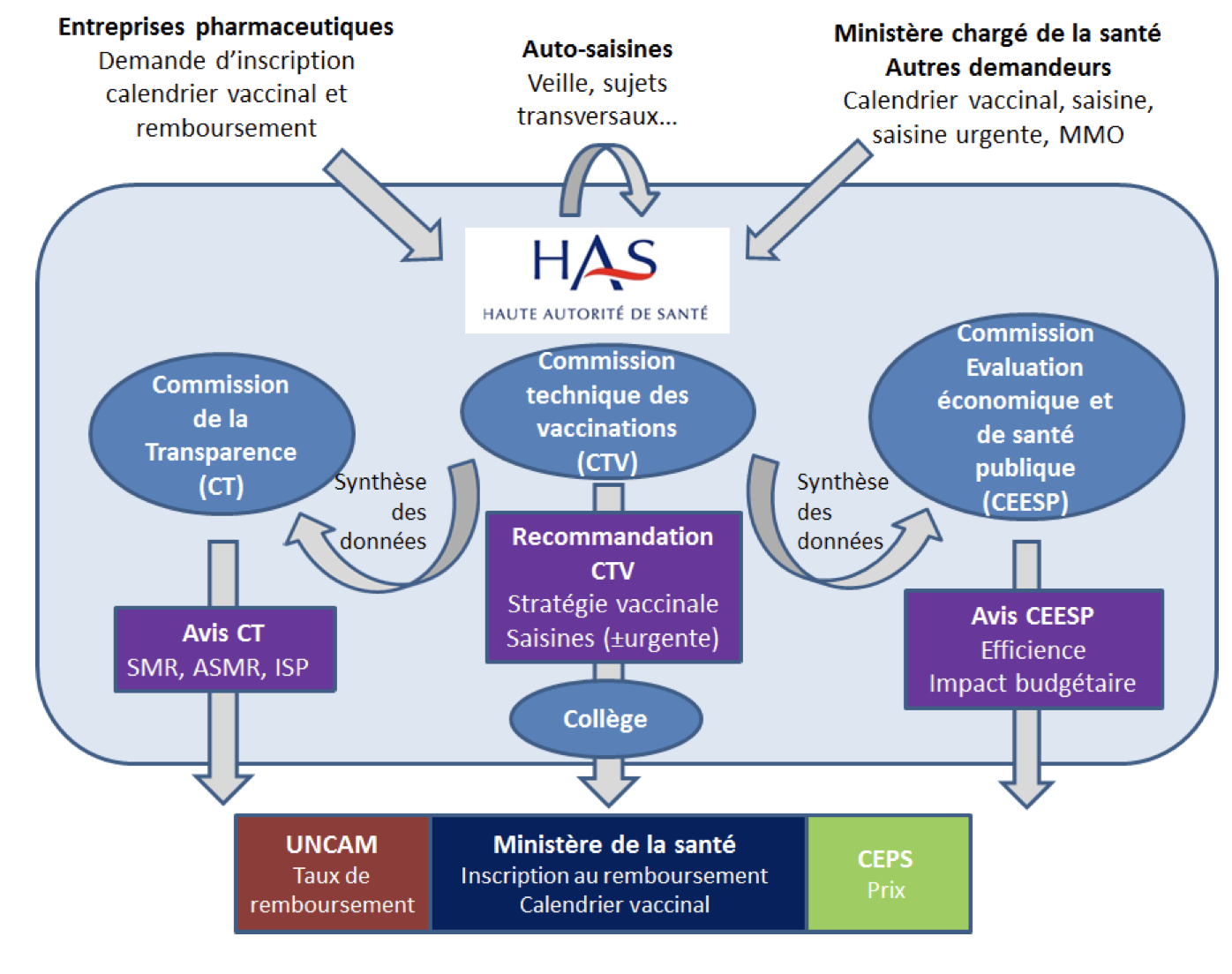
A) La commission technique des vaccinations (CTV)
- Elle a été créée le 22 mars 2017, pour un mandat de 3 ans, afin d'assurer les nouvelles missions en matière de vaccination de la HAS.
- Elle reprend les anciennes missions du comité technique des vaccinations du Haut Conseil de la santé publique (HCSP).
- La CTV regroupe des experts de différentes disciplines (infectiologie, pédiatrie, microbiologie, immunologie, épidémiologie, santé publique, médecine générale, économie de la santé, sociologie...).
- Elle a pour missions l’élaboration de la politique de vaccination, de préparer les délibérations du collège relatives notamment :- aux recommandations vaccinales, y compris en urgence à la demande du ministre chargé de la santé ;- au calendrier vaccinal arrêté par le ministre chargé de la santé.
- aux mentions minimales obligatoires des campagnes publicitaires portant sur des vaccins.
- Elle collabore également à la préparation des avis de la commission de la transparence et de la commission évaluation économique et de santé publique portant sur des vaccins.
- Elle propose au collège les outils méthodologiques nécessaires à l’exercice de ses missions en matière de vaccination.
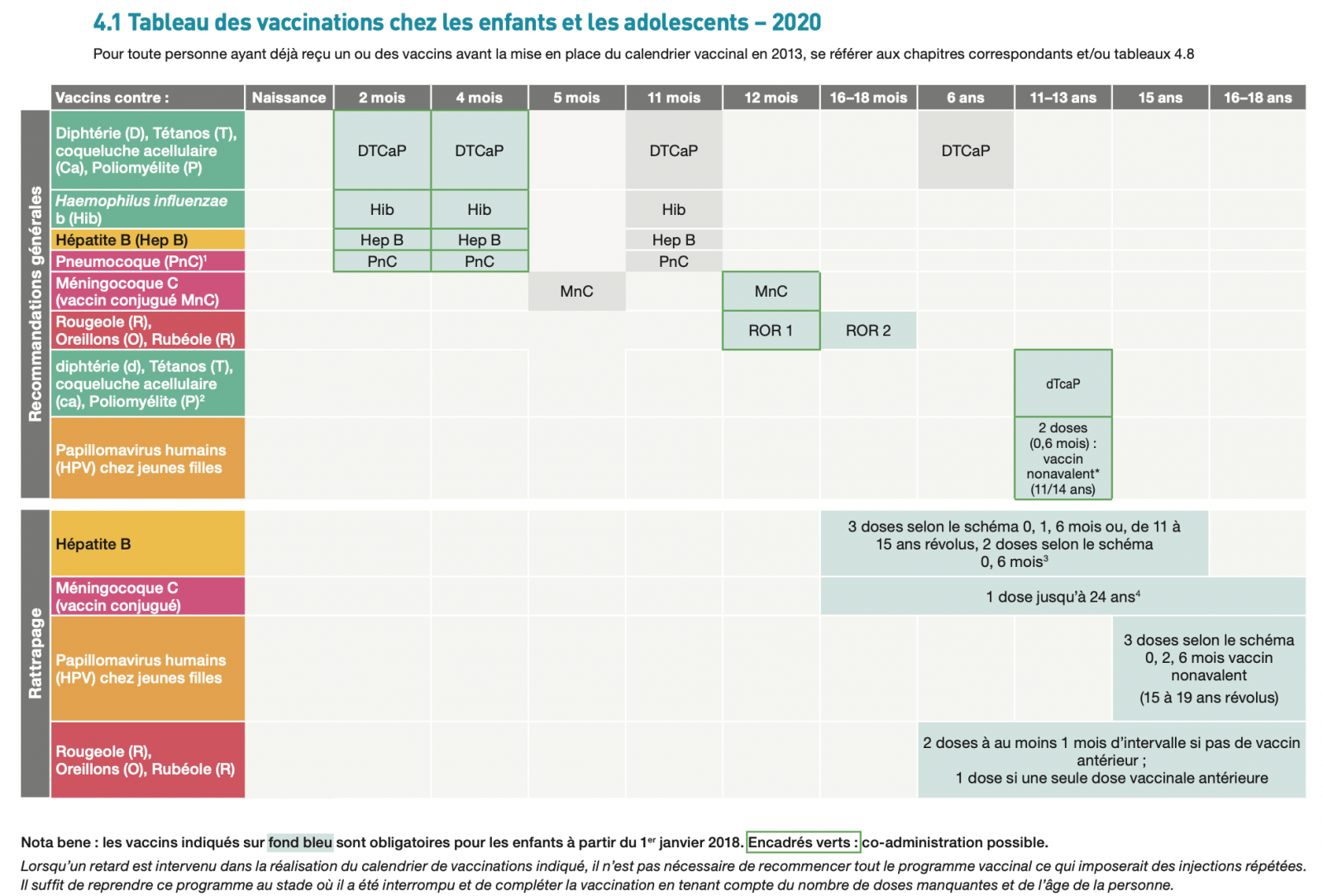
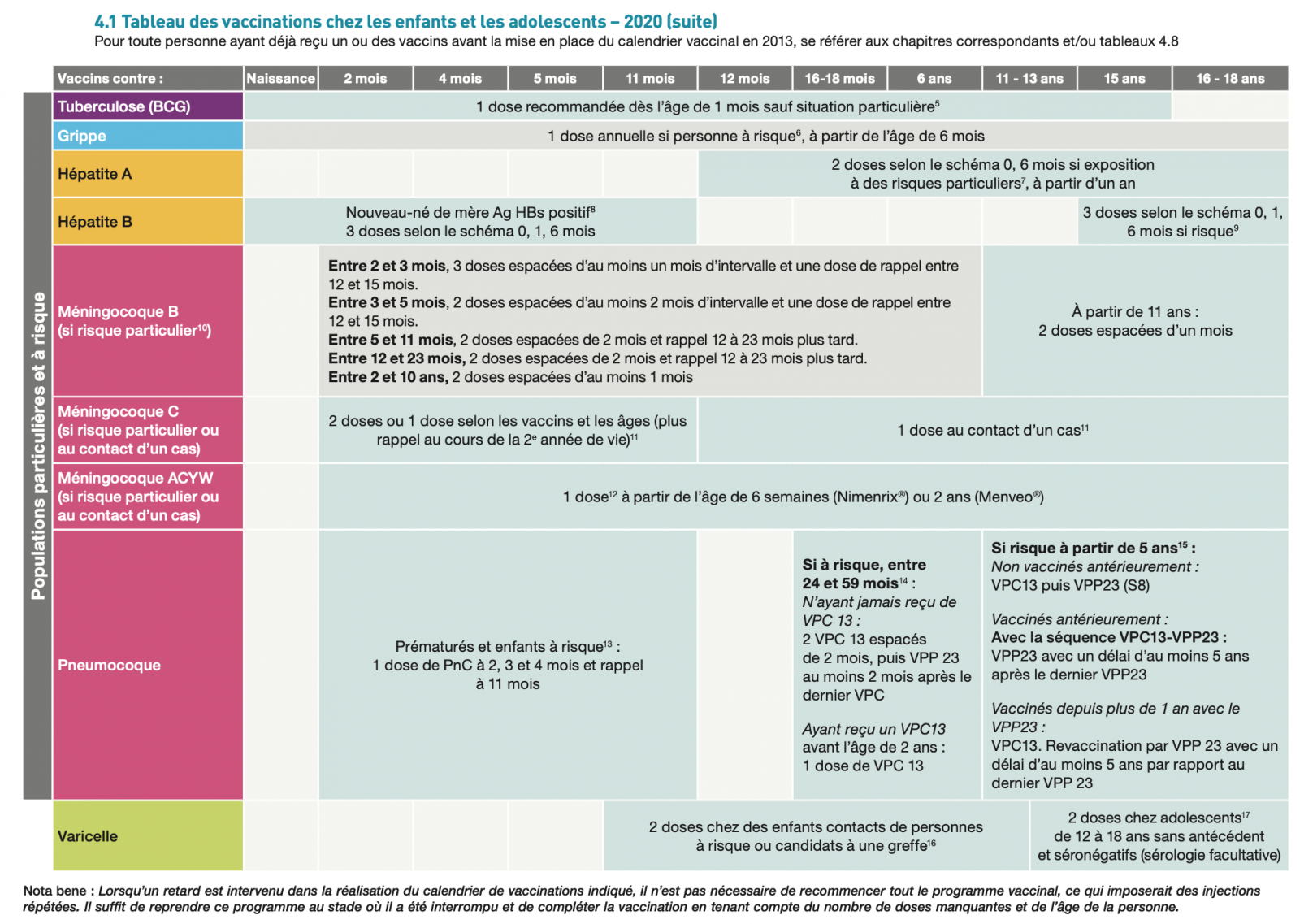
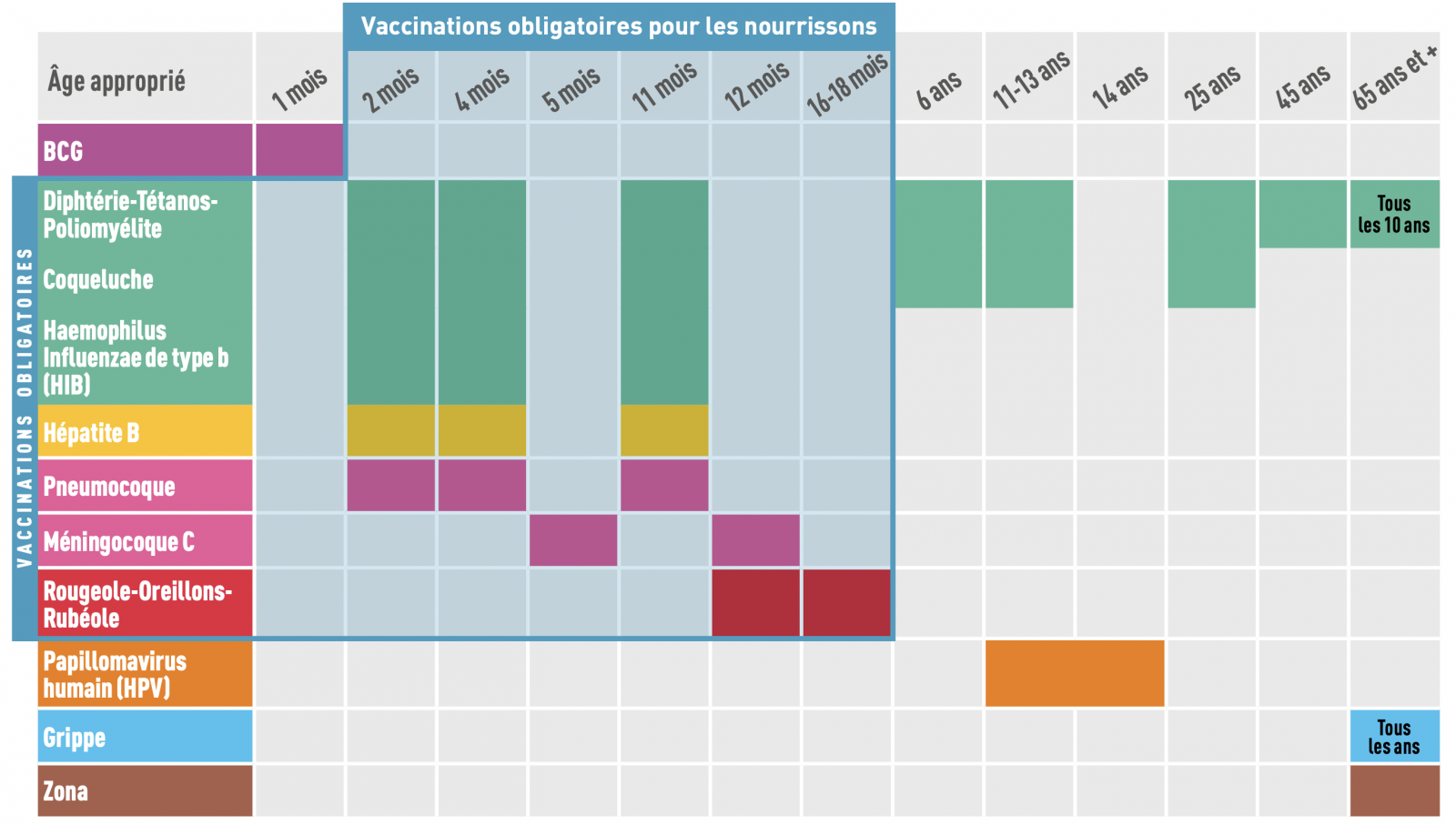
B) Le calendrier vaccinal chez les enfants 1 1
Calendrier des vaccinations et recommandations vaccinales 2020 1
-
Depuis le 1er janvier 2018, huit vaccinations, auparavant recommandées sont devenues obligatoires : il s’agit des vaccinations contre la coqueluche, les infections invasives à Haemophilus influenzae de type b, l’hépatite B, les infections à pneumocoque, les infections invasives à méningocoque de sérogroupe C, la rougeole, les oreillons et la rubéole ; soit un total de 11 vaccinations obligatoires.
-
Ces 11 vaccinations sont pratiquées, sauf contre-indication médicale reconnue, dans les 18 premiers mois de l’enfant selon le présent calendrier et sont exigibles, pour l’entrée ou le maintien en collectivité, pour tout enfant né à compter du 1er janvier 2018.
-
Lorsqu’une ou plusieurs vaccinations font défaut, le code de la santé publique prévoit que l’enfant est provisoirement admis. Les vaccinations obligatoires manquantes selon l’âge de l’enfant et conformément au calendrier des vaccinations doivent être effectuées dans les 3 mois suivant l’admission. Une fois la vaccination débutée, il est ensuite nécessaire de poursuivre l’immunisation selon le calendrier vaccinal en vigueur.
-
Lorsque l’enfant est admis dans une collectivité d’enfants pour une durée supérieure à un an, la justification de la réalisation des vaccinations obligatoires pour le maintien dans cette collectivité est annuelle.
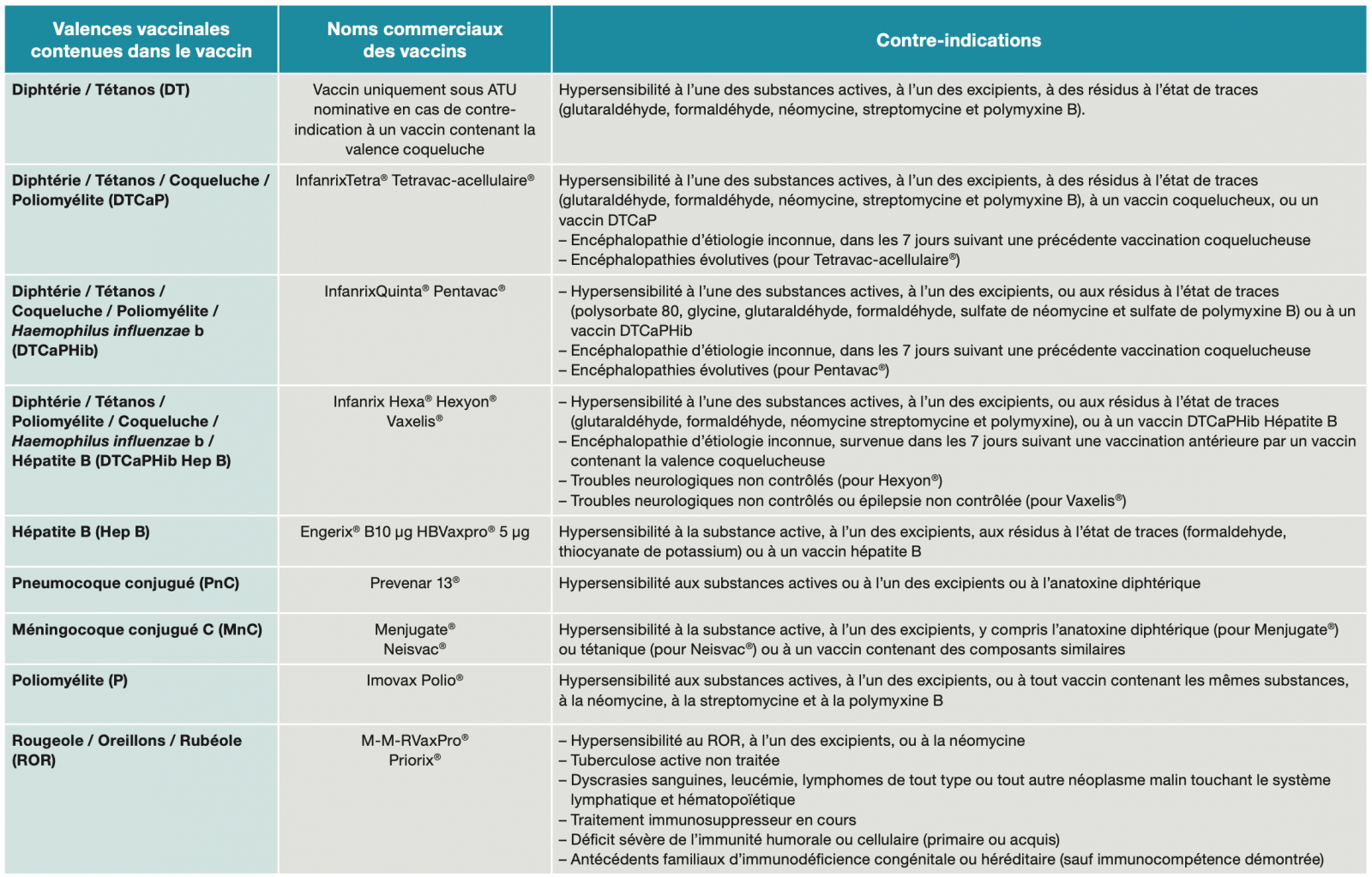
(Se reporter à la notice de chaque vaccin pour une description détaillée)
C) Nouveauté 2020 1
1) Nouvelles recommandations
- La vaccination contre les infections par les papillomavirus humains est dorénavant recommandée chez les garçons de 11 à 14 ans révolus avec un schéma 2 doses (M0-M6) avec un rattrapage possible chez les adolescents et les jeunes hommes de 15 à 19 ans révolus selon un schéma 3 doses (M0, M2, M6). Toute vaccination chez le jeune garçon doit être initiée avec le Gardasil9®. La recommandation sera applicable au 1er janvier 2021.
- A compter de la saison 2020, compte tenu de l’épidémiologie particulière observée depuis plusieurs années à Mayotte, la campagne de vaccination contre la grippe saisonnière à Mayotte sera calquée sur celle de l’hémisphère Nord et utilisera les mêmes vaccins. La campagne de vaccination doit être initiée précocement, idéalement en septembre, dès la mise à disposition des vaccins antigrippaux.
2) Nouveautés règlementaires
- Vaccination contre la grippe saisonnière par les pharmaciens d’officine : depuis la campagne de vaccination contre la grippe saisonnière 2019/2020 dans l’hémisphère nord, les pharmaciens d’officine volontaires et formés peuvent vacciner contre la grippe saisonnière, dès lors que l’activité de vaccination a été déclarée conformément aux dispositions de l’article R. 5125-33-8 du code de la santé publique – les personnes majeures, ciblées par les recommandations vaccinales, à l’exception des personnes présentant des antécédents de réaction allergique sévère à l’ovalbumine ou à une vaccination antérieure4.
- Vaccination contre la fièvre typhoïde : Le décret n°2020-28 du 14 janvier 2020 suspendant l’obligation de vaccination contre la fièvre typhoïde des personnes exerçant une activité professionnelle dans un laboratoire de biologie médicale est entré en vigueur le 1er mars 2020. La vaccination contre la fièvre typhoïde n’est dès lors plus exigible pour ces professionnels5.
D) Le vaccin anti-rotavirus : Gastro-entérite à Rotavirus
- La vaccination n’est actuellement pas recommandée dans le cadre du calendrier vaccinal, mais peut être proposée aux nouveaux parents.
- Le HCSP rappelle que si cette vaccination est pratiquée à titre individuel et dans le cadre de son AMM, le médecin doit informer les parents du risque d’invagination intestinale aiguë (IIA) et des signes fonctionnels devant motiver une consultation en urgence.
- Le vaccin contre le rotavirus est prescrit et administré par voie orale par un médecin.
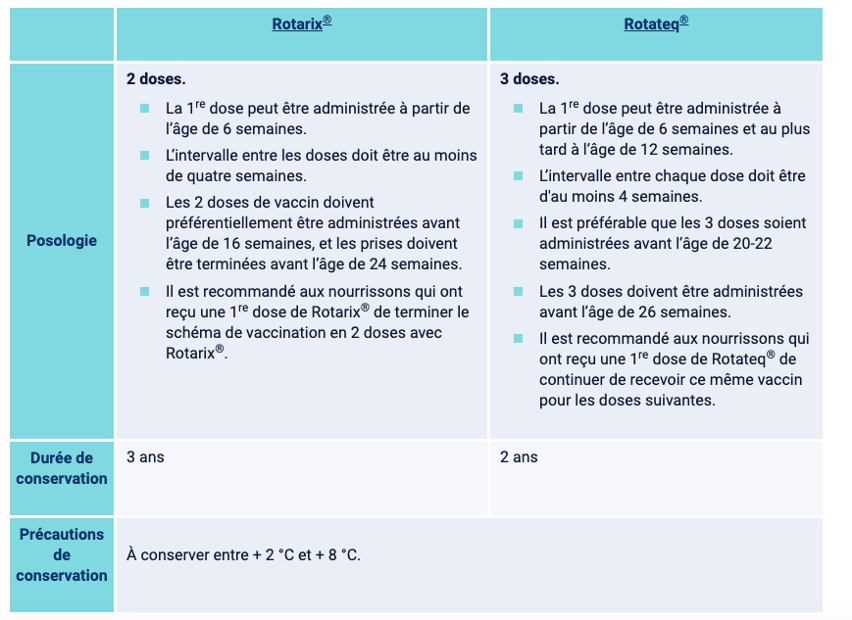
1) Le vaccin peut être administré aux enfants :
- allaités
- anciens prématurés > 6 semaines de vie en bon état général et sortis ou sortants d’hospitalisation
- ayant déjà présenté une gastro-entérite y compris à rotavirus
- vivant avec un patient immunodéprimé dans l’entourage (y compris au domicile)
- ayant des contacts avec une femme enceinte.
2) Histoire de la recommandation vaccinale contre le rotavrus :
- Le HCSP a recommandé la vaccination de tous les nourrissons contre les gastroentérites aiguës à rotavirus en France dans un avis daté du 29 novembre 2013 et publié le 14 février 2014. 1
- Cependant, au vu d’éléments défavorables du rapport bénéfices-risques (risque rare mais grave d’IIA, pouvant survenir dans le mois suivant le vaccin et en particulier dans les 7 jours après la 1ère dose chez ces nourrissons < 6 mois), le HCSP a décidé de suspendre sa recommandation de vacciner les nourrissons contre les rotavirus dans un avis daté du 21 avril 2015 et publié le 7 mai 2015. 1
- Plusieurs pays de l’UE recommandent la vaccination contre les rotavirus. Dans ces pays où la recommandation était déjà effective avant la recommandation française de novembre 2013, le sur-risque d’IIA avait été pris en compte.
- L'excès de cas d’IIA survenant après la vaccination contre les rotavirus a été évalué dans la littérature pour chacun des deux vaccins : il est de 3,5 à 6 cas pour 100 000 nourrissons vaccinés. Ce sur-risque est également noté dans le résumé des caractéristiques du produit des vaccins Rotarix® et RotaTeq®.
3) Suivi de pharmacovigilance des vaccins contre le rotavirus :
- 47 cas d’IIA ont été notifiés depuis mai 2006, date de commercialisation du vaccin Rotarix® et janvier 2007, celle de RotaTeq®, jusqu'au 31 octobre 2014.
- L'évolution des cas a été défavorable dans 14 cas, nécessitant une intervention chirurgicale, tandis que deux autres nourrissons sont décédés.
- Pour l'un de ces décès, l'imputabilité du vaccin ne pouvait être exclue ni affirmée, le décès étant survenu une semaine après la 3ème dose (le sur-risque étant documenté pour la semaine suivant la 1ère dose).
- Les enquêtes conduites lors de ces deux décès indiquent que la gravité de ces cas est en grande partie liée à une prise en charge tardive (au-delà de 36 heures après le début des signes cliniques).
- Au niveau international, une 20aine de décès a été rapportée aux USA, mais 5 seulement ont pu être documentés par rapport aux dates de vaccination. Hormis en France, aucun décès imputable à la vaccination à rotavirus n'a été rapporté en Europe.
- Lorsque la prise en charge est réalisée sans délai, l'évolution est constamment favorable. Mais les effets indésirables observés en France ont montré que ces conditions n'étaient pas toujours réunies.
- Ainsi, compte tenu de l'évolution défavorable de ces cas d’IIA et ne pouvant exclure que de telles situations se reproduisent, le HCSP a préféré suspendre la recommandation de vacciner tous les nourrissons contre les infections à rotavirus en France. 1
- La France a communiqué aux autres états membres de l’UE ces données de pharmacovigilance. Cependant, l'Agence européenne des médicaments n'a pas pour autant modifié les conditions de l'autorisation de mise sur le marché de ces 2 vaccins, considérant que la survenue de ces effets indésirables était déjà connue et prise en compte.
- Autres pays européens : pas de changement des recommandations vaccinales contre les rotavirus.
5) peut-on continuer à vacciner contre rotavirus ?
- Pour autant, les bénéfices de la vaccination anti-rotavirus demeurent.
- Sur le plan pratique, la vaccination des nourrissons de moins de 6 mois contre la gastroentérite à rotavirus peut toujours être pratiquée par le médecin, sous réserve d'une surveillance adaptée de l'enfant.
- Le praticien devra alors informer la famille de l'enfant vacciné du risque d'invagination intestinale aiguë et des signes cliniques par lesquels elle doit se manifester pour une prise en charge rapide et adaptée.
- La vigilance des parents doit être renforcée dans le mois qui suit l'administration de la dose orale vaccinale et en particulier au cours de la première semaine.
E) Cas particulier du vaccin contre le méningo B
- Le vaccin Bexsero® a obtenu une AMM européenne le 14 janvier 2013 pour « l'immunisation active des sujets à partir de l'âge de 2 mois contre l'infection invasive méningococcique causée par Neisseria meningitidis de groupe B ».
- Pas de recommandation généralisée à ce jour en France.
- Cependant, le méningo B étant le sérotype prédominant en France avec le Méningo C, certaines sociétés savantes comme la Société Française de Pédiatrie SFP et le société de pathologie infecteuses SPILF encouragent la généralisation de cette vaccination.
- L'absence de recommandation en population générale repose sur le fait que malgré les données d'immunogénicité de ce vaccin en faveur d'une efficacité pour la prévention des infections invasives à méningocoques B :
- les données d'efficacité clinique sur le terrain font défaut.
- la durée de protection est limitée à 6-12 mois chez le nourrisson
- aucune donnée montrant un effet sur le portage (donc sur une éventuelle immunité de groupe) n'est disponible.
Recommandations vaccinales en population générale
Calendrier des vaccinations et recommandations vaccinales 2020
A) Tuberculose : Tuberculose
1) Recommandations particulières
- La vaccination par le BCG est fortement recommandée pour les enfants exposés à un risque élevé de tuberculose dans leur entourage ou dans leur environnement.
- Depuis la publication du décret de suspension de l’obligation de vaccination par le BCG des enfants et des adolescents et de la circulaire d’application,1 la vaccination par le BCG ne peut plus être exigée à l’entrée en collectivité.
- Pour les enfants exposés à un risque élevé de tuberculose, la vaccination par le BCG est recommandée à partir de l’âge de 1 mois, idéalement au cours du 2ème mois. Toutefois pour les enfants originaires de Guyane, de Mayotte ou ayant un membre de l’entourage atteint d’une tuberculose récente (moins de 5 ans), la vaccination est recommandée avant la sortie de la maternité. Le vaccin peut être co-administré avec les vaccins prévus à l’âge de 2 mois.
- Chez les enfants à risque non vaccinés, la vaccination peut être réalisée jusqu’à l’âge de 15 ans.
- Il n’est plus indiqué de pratiquer une intradermoréaction (IDR) à la tuberculine préalablement à la vaccination pour les enfants de moins de 6 ans, à l’exception de ceux ayant résidé ou effectué un séjour de plus d’un mois dans un pays de forte incidence de la tuberculose. La vaccination ne s’applique qu’aux personnes ayant une intradermoréaction à la tuberculine négative.
- Les contre-indications médicales temporaires à la vaccination BCG sont constituées par les dermatoses étendues en évolution et les contre-indications définitives par les déficits immunitaires congénitaux ou acquis, notamment dus au VIH. 1
Sont considérés comme enfants à risque élevé de tuberculose les enfants qui répondent au moins à l’un des critères suivants :
- Enfant né dans un pays de forte endémie tuberculeuse ;
- Enfant dont au moins l’un des parents est originaire de l’un de ces pays ;
- Enfant devant séjourner au moins un mois d’affilée dans l’un de ces pays ;
- Enfant ayant un antécédent familial de tuberculose (collatéraux ou ascendants directs) ;
- Enfant résidant en Île-de-France, en Guyane ou à Mayotte ;
- Enfant dans toute situation jugée par le médecin à risque d’exposition au bacille tuberculeux, notamment enfant vivant dans des conditions de logement défavorables (habitat précaire ou surpeuplé) ou socioéconomiques défavorables ou précaires (en particulier parmi les bénéficiaires de la protection universelle maladie ou de la couverture et de la complémentaire santé solidaire) ou en contact régulier avec des adultes originaires d’un pays de forte endémie.
Les zones géographiques à forte incidence 1 tuberculeuse, selon les estimations de l’OMS 1, et en tenant compte de certaines imprécisions liées aux difficultés du recueil fiable des données épidémiologiques dans certains pays, sont :
- Le continent africain dans son ensemble.
- Le continent asiatique dans son ensemble à l’exception du Japon, y compris les pays du Proche et Moyen-Orient à l’exception de Chypre, des Emirats Arabes Unis, d’Israël, de la Jordanie et d’Oman.
- Les pays d’Amérique centrale et du Sud à l’exception d’Antigua et Barbuda, Barbade, Bermudes, Bonaire, Cuba et du Costa Rica, Curaçao, Jamaïque, Iles Vierges et Caïmans, Porto Rico.
- Les pays d’Europe centrale et de l’Est à l’exception de la Grèce, de la Hongrie, de la Slovaquie, de la Slovénie et de la Tchéquie.
Rappel : la revaccination par le BCG, en population générale et chez les professionnels exposés à la tuberculose, n’est plus indiquée depuis 2004. En conséquence, l’IDR à la tuberculine à 5 Unités (Tubertest®) n’a pas lieu d’être pratiquée à titre systématique, notamment après la vaccination par le BCG.
2) Recommandations pour les professionnels 1
- Un décret suspendant l’obligation de vaccination contre la tuberculose des personnes mentionnées au C de l’article R. 3112-1 et à l’article R. 3112-2 du code de la santé publique est entré en vigueur le 1er avril 2019. Depuis cette date, la vaccination par le BCG n’est plus exigée lors de la formation ou de l’embauche de ces personnes.1
Toutefois, il appartiendra aux médecins du travail d’évaluer le risque d’exposition au bacille de la tuberculose et de proposer, le cas échant, une vaccination par le vaccin antituberculeux BCG au cas par cas aux professionnels du secteur sanitaire et social non antérieurement vaccinés et ayant un test immunologique de référence négatif et susceptibles d’être très exposés tels que :
- Les personnels en contact répétés avec des patients tuberculeux et tout particulièrement ceux à risque de tuberculose multi résistante et chez qui les mesures de confinement sont difficiles à appliquer.
- Les personnels de laboratoires travaillant en routine sur le bacille de la tuberculose (cultures, modèles animaux, ...).
Il est rappelé la nécessité d’un respect strict de mesures barrières (mesures standard et précaution air) pour les personnes travaillant dans les milieux à risque.1
3) Schéma vaccinal : BCG AJVaccines®
- Enfants âgés de moins de 12 mois : Une dose de 0,05 ml de vaccin reconstitué doit être administrée strictement par voie intradermique
- Adultes et enfants, âgés de 12 mois et plus : Une dose de 0,1 ml de vaccin reconstitué doit être administré strictement par voie intradermique.
- Le vaccin une fois reconstitué doit être utilisé immédiatement ou dans un délai ne dépassant pas 4 h (conservé à 2-8°c).
4) L’IDR doit être pratiquée :
- pour vérifier l’absence de tuberculose avant vaccination, excepté chez les enfants < 6 ans qui sont vaccinés sans test préalable sauf si séjour de plus d’un mois récent dans un pays à risque.
- au cours des enquêtes autour d’un cas de tuberculose.
- comme aide au diagnostic de la tuberculose.
- comme test de référence dans le cadre de la surveillance des professions à risque.
B) Coqueluche : Vaccin coqueluche acellulaire
- L’immunité coquelucheuse après maladie naturelle est de l’ordre d’une dizaine d’années. Il n’y a pas lieu de revacciner les personnes éligibles à la vaccination moins de 10 ans après une coqueluche documentée. En revanche, une injection de rappel est recommandée aux personnes éligibles ayant contracté la maladie plus de 10 ans auparavant.
- Ceci ne s’applique pas au nourrisson qui doit être vacciné même s’il a contracté la maladie.
1) Recommandations générales
a) Nourrissons
- Il n’existe pas de vaccin anticoquelucheux non combiné. La vaccination contre la coqueluche est pratiquée avec le vaccin acellulaire combiné à d’autres valences.
- La vaccination contre la coqueluche est obligatoire pour tous les enfants nés à partir du 1er janvier 2018.
- Elle comporte une primovaccination de deux injections à deux mois d’intervalle, aux âges de 2 mois (8 semaines) et 4 mois, suivies d’un rappel à l’âge de 11 mois. Ce schéma ne doit pas être différé.
- Les vaccins hexavalents utilisés pour cette primovaccination comprennent une dose entière d’antigènes coquelucheux (DTCaP) : Infanrix Hexa®, Hexyon®, Vaxelis®.
b) À l’âge de 6 ans
- Un rappel de ce vaccin est recommandé 1 à l’âge de 6 ans avec un vaccin à doses entières d’anatoxine diphtérique et d’antigène coquelucheux (DTCaPolio) : Tétravac acellulaire®, Infanrix Tetra®.
c) Entre 11 et 13 ans
- Le rappel diphtérie, tétanos coqueluche et poliomyélite est recommandé.
- Si l’enfant a eu son rappel coquelucheux à 6 ans : vaccination avec une dose réduite d’antigènes coquelucheux (dTcaPolio) : Repevax®, Boostrixtetra®.
- Si l’enfant n’a pas reçu de rappel coquelucheux à l’âge de 6 ans ou s’il a reçu à 6 ans une dose réduite d’antigènes coquelucheux (dTcaPolio) : vaccination avec une dose entière d’antigènes coquelucheux (DTCaPolio) : Tetravac acellulaire®, Infanrix Tetra®.
2) Recommandations particulières
a) Chez les adultes
- Le but de la vaccination chez les adultes est de réduire le risque de coqueluche grave chez les nourrissons dont le schéma complet de vaccination n’est pas achevé.
- À l’exception des jeunes adultes ayant reçu une vaccination contre la coqueluche au cours des cinq dernières années, un rappel avec le vaccin quadrivalent dTcaPolio est recommandé, à l’occasion du rappel diphtérie-tétanos-poliomyélite fixé à l’âge de 25 ans.
- Pour les personnes âgées de plus de 25 ans n’ayant pas reçu ce rappel, un rattrapage avec un vaccin dTcaPolio pourra être proposé jusqu’à l’âge de 39 ans révolus.
Le vaccin tétravalent à doses réduites d’antigènes coquelucheux (dTcaPolio) est recommandé chez :
- Les adultes âgés de 25 ans avec un rattrapage possible jusqu’à l’âge de 39 ans révolus.
- Dans le contexte professionnel.
- Dans le cadre de la stratégie du cocooning.
- Chez les personnes en contact avec un cas de coqueluche ou lorsqu’il existe des cas groupés.
- En France, la vaccination contre la coqueluche n’est actuellement pas recommandée chez la femme enceinte (sauf à Mayotte dans le contexte actuel épidémique lié à une baisse de la couverture vaccinale).
b) Stratégie du cocooning
- Cette stratégie se définit comme la vaccination des personnes susceptibles d’être en contact étroit avec le nourrisson durant ses six premiers mois de vie.
+ La stratégie du cocooning concerne les populations suivantes :
- Aux adultes ayant un projet parental.
- Dans l’entourage d’une femme enceinte pour : 1
- les enfants de la fratrie et le conjoint
- les personnes susceptibles d’être en contact étroit et durable avec le futur nourrisson au cours de ses 6 premiers mois. Ceci peut concerner les grands-parents, les baby-sitters...
- En post-partum immédiat pour :
- La mère, qu’il conviendrait idéalement de vacciner avant la sortie de la maternité, même si elle allaite
- Les personnes susceptibles d’être en contact étroit et durable avec le futur nourrisson au cours de ses 6 premiers mois si la mise à jour de la vaccination n’a pas été faite antérieurement
+ Modalités de vaccination :
- Personnes non antérieurement vaccinées contre la coqueluche ou n’ayant pas reçu de vaccin coquelucheux depuis l’enfance : une dose de vaccin dTcaPolio.
- Personnes antérieurement vaccinées :
- adolescents et jeunes adultes de moins de 25 ans : une dose de rappel si la dernière injection date de plus de cinq ans ;
- adultes de plus de 25 ans : une dose de rappel de vaccin dTcaPolio si la vaccination coquelucheuse antérieure remonte à dix ans ou plus.
- Dans tous les cas, un délai minimal de 1 mois devra être respecté par rapport au dernier vaccin dTPolio. Par la suite, le recalage sur le calendrier en cours pour les rappels dTPolio ultérieurs se fera suivant les recommandations introduites en 2013.
3) Recommandations pour les professionnels
a) La vaccination contre la coqueluche est recommandée pour :
- les professionnels soignants dans leur ensemble, y compris dans les établissements d’hébergement pour personnes âgées dépendantes (EHPAD). Les personnes travaillant en contact étroit et répété avec les nourrissons âgés de moins de 6 mois (maternité, service de néonatalogie et de pédiatrie) devraient être vaccinées en priorité ;
- les étudiants des filières médicales et paramédicales ;
- les professionnels de la petite enfance dont les assistants maternels ;
- les personnes effectuant régulièrement du baby-sitting ;
b) selon les modalités suivantes :
- Les personnes concernées, non antérieurement vaccinées contre la coqueluche ou n’ayant pas reçu de vaccin coquelucheux depuis l’âge de 18 ans et dont le dernier rappel date de plus de cinq ans recevront une dose de vaccin dTcaPolio en respectant un délai minimal d’un mois par rapport au dernier vaccin dTPolio. Le recalage sur le calendrier en cours se fera suivant les recommandations introduites en 2013 (cf. tableaux 4.8) ;
- Pour les personnes ayant déjà reçu une dose de vaccin coquelucheux à l’âge adulte, le recalage sur le calendrier en cours se fera suivant les recommandations introduites en 2013.
- Pour l’ensemble de ces personnes, les rappels administrés aux âges de 25, 45, 65 ans comporteront systématiquement la valence coqueluche (vaccin dTcaPolio).

4) Conduite à tenir devant un ou plusieurs cas de coqueluche 1
- La mise à jour des vaccinations de la population exposée selon le calendrier vaccinal en vigueur est recommandée autour d’un cas ou de cas groupés de coqueluche.
- Cette population exposée comprend toutes les personnes en contact avec le cas pendant sa phase contagieuse (3 semaines après le début des signes ou 3 à 5 jours après le début du traitement par un antibiotique adapté).
- La vaccination en post-exposition n’a aucune efficacité pour prévenir la maladie chez une personne déjà contaminée. Cette vaccination de rattrapage a pour but de protéger dans l’hypothèse d’une contamination ultérieure.
- Un avis du HCSP en 2014 recommande également une antibioprophylaxie dans l’entourage des cas (pour tous les contacts proches mal vaccinés, et tous les contacts occasionnels à risque de coqueluche grave ou ayant dans leur entourage des personnes à risque de coqueluche grave).
C) Diphtérie, tétanos, poliomyélite
1) Recommandations générales
- La primo-vaccination (deux injections suivies d’un rappel) est obligatoire chez tous les enfants nés à compter du 1er janvier 2018.
- La vaccination des nourrissons est pratiquée avec un vaccin combiné. La primo vaccination comporte deux injections à l’âge de 2 mois (8 semaines) et 4 mois, suivies d’un rappel à l’âge de 11 mois. Ce schéma ne doit pas être différé.
- Les rappels ultérieurs sont recommandés 1 à l’âge de 6 ans, et sont réalisés avec un vaccin combiné contenant la valence coqueluche acellulaire (Ca) et les valences tétanique et diphtérique à dose complète d’anatoxine diphtérique et d’antigènes coquelucheux (DTCaPolio), puis, entre 11 et 13 ans, avec un vaccin combiné contenant des doses réduites d’anatoxine diphtérique et d’antigènes coquelucheux (dTcaPolio).
- L’ensemble des rappels à l’âge de 6 ans et de 11-13 ans contre la diphtérie, le tétanos, la poliomyélite, et la coqueluche sont indispensables pour conférer une protection à long terme.
- Les rappels de l’adulte sont recommandés aux âges fixes de 25 ans, (à cet âge, le vaccin, inclura la valence coqueluche à dose réduite (ca) chez l’adulte n’ayant pas reçu de vaccination contre la coqueluche au cours des cinq dernières années (dTcaPolio)), 45 ans et 65 ans, puis à 75 ans, 85 ans.... (intervalle de dix ans à partir de 65 ans, compte tenu d’une moins bonne réponse vaccinale), en utilisant un vaccin à dose réduite d’anatoxine diphtérique combiné à l’anatoxine tétanique et aux antigènes poliomyélitiques (dTPolio).
2) Recommandations pour les professionnels
- Les rappels sont effectués aux mêmes âges fixes (25 ans, 45 ans et, en fonction de la poursuite des activités professionnelle, 65 ans), avec un vaccin contenant une dose réduite d’anatoxine diphtérique (dTPolio).
- Ces vaccinations sont obligatoires pour certains professionnels notamment les professionnels de santé.1
- Nota : pour les professionnels de santé et de la petite enfance, les rappels comportent la valence coquelucheuse (vaccin dTcaPolio),

D) Infections à pneumocoque (IP) : vaccin pneumococcique conjugué
1) Recommandations générales
- La primovaccination contre le pneumocoque (deux injections suivies d’un rappel) est obligatoire chez tous les enfants nés à compter du 1er janvier 2018.
- La vaccination par le vaccin pneumococcique conjugué 13-valent41 (VPC13) est effectuée selon un schéma vaccinal de primovaccination à deux injections à deux mois d’intervalle à l’âge de 2 mois (8 semaines) et à 4 mois suivies d’une dose de rappel à l’âge de 11 mois.
2) Recommandations particulières
- Pour les prématurés et les nourrissons à risque élevé de contracter une infection à pneumocoque (cf. ci-dessous la liste des personnes à risque), le maintien d’un schéma vaccinal renforcé comprenant une primovaccination à trois injections (2 mois, 3 mois, 4 mois) du vaccin pneumococcique conjugué 13-valent suivies d’une dose de rappel est recommandé.
- À partir de l’âge de 2 ans, la vaccination est recommandée pour les patients à risque ; elle est effectuée avec un vaccin conjugué 13-valent, ainsi qu’avec un vaccin un vaccin pneumococcique polyosidique non conjugué 23-valent42 (VPP 23) selon les modalités figurant dans le schéma vaccinal mentionné plus bas : elle s’adresse aux personnes suivantes :
a) Patients immunodéprimés (patients concernés par les recommandations de vaccination des immunodéprimés)
- Aspléniques ou hypospléniques (incluant les syndromes drépanocytaires majeurs) ;
- Atteints de déficits immunitaires héréditaires ;
- Infectés par le VIH ;
- Patients présentant une tumeur solide ou une hémopathie maligne ;
- Transplantés ou en attente de transplantation d’organe solide ;
- Greffés de cellules souches hématopoïétiques ;
- Traités par immunosuppresseur, biothérapie et/ou corticothérapie pour une maladie auto-immune ou inflammatoire chronique;
- Atteints de syndrome néphrotique.
b) Patients non immunodéprimés porteurs d’une maladie sous-jacente prédisposant à la survenue d’Infection Invasive à Pneumocoque (IIP) :
- Cardiopathie congénitale cyanogène, insuffisance cardiaque
- Insuffisance respiratoire chronique, bronchopneumopathie obstructive, emphysème
- Asthme sévère sous traitement continu
- Insuffisance rénale
- Hépatopathie chronique d’origine alcoolique ou non
- Diabète non équilibré par le simple régime
- Patients présentant une brèche ostéo-méningée, un implant cochléaire ou candidats à une implantation cochléaire.
3) Schéma vaccinal
a) Le vaccin anti-pneumococcique conjugué (VPC13).
- Il entraîne une immunité chez le jeune enfant, induit une réponse mémoire et agit sur le portage des pneumocoques dans la gorge.
- Le PCV 7-valent (VPC7) a d’abord été recommandé en 2003 chez les enfants de moins de 2 ans présentant un risque accru d’infection invasive à pneumocoques, puis en 2006 chez tous les enfants < 2ans.
- Il a été remplacé depuis 2010 par le VPC 13-valent (VPC13), qui couvre 13 sérotypes (1, 3, 4, 5, 6A, 6B, 7F, 9V, 14, 18C, 19A, 19F et 23F).
- Ce vaccin est disponible pour la vaccination des enfants depuis 2010 et de l’adulte depuis 2013.
b) Le vaccin anti-pneumococcique polysaccharidique 23-valent (VPP23)
- Il couvre 23 sérotypes (1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19A, 19F, 20, 22F, 23F et 33F).
- Ce vaccin est très peu immunogène chez le jeune enfant et n’agit pas sur le portage.
- Ce vaccin est disponible depuis 1983.
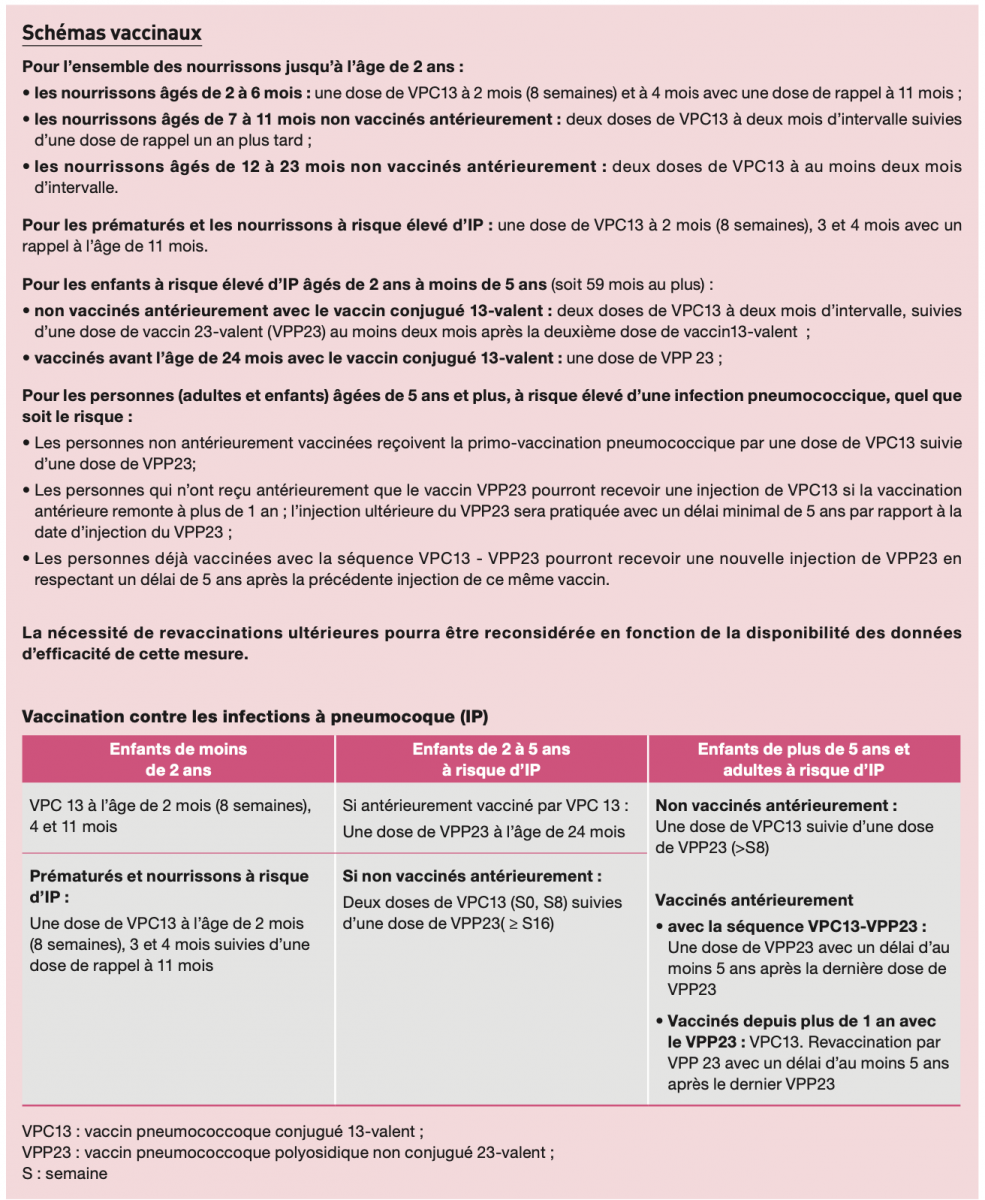
E) Infections invasives à méningocoque (IIM) : Infections invasives à méningocoque (IIM)
1) Recommandations générales
- La vaccination contre les IIM de sérogroupe C (une dose à 5 mois ainsi qu’une deuxième dose à 12 mois) est obligatoire chez tous les enfants nés à compter du 1er janvier 2018.
- Le vaccin Neisvac® est le seul vaccin méningococcique C conjugué à disposer d’une AMM pour la primovaccination en une seule dose avant l’âge de un an, et ce, dès l’âge de 4 mois.
- La dose de 12 mois peut être co-administrée avec le vaccin rougeole oreillons rubéole.
- À partir de l’âge de 12 mois et jusqu’à l’âge de 24 ans révolus, la vaccination est recommandée, selon un schéma à une dose unique, avec un vaccin conjugué méningococcique C conjugué pour les nourrissons, enfants, adolescents et jeunes adultes n’ayant pas reçu de primovaccination antérieure.
- L’obtention d’une immunité de groupe par la vaccination étendue aux enfants de plus de 12 mois, adolescents et adultes jeunes est un enjeu majeur de santé publique. Une couverture vaccinale élevée dans l’ensemble de ces classes d’âge permettra de réduire la transmission de la bactérie dans la population et de protéger indirectement les sujets non vaccinés.
2) Recommandations particulières
- Pour les personnes souffrant de déficit en fraction terminale du complément, recevant un traitement anti-C5, porteuses d’un déficit en properdine ou ayant une asplénie anatomique ou fonctionnelle et chez les personnes ayant reçu une greffe de cellules souches hématopoïétiques : la vaccination 1 est recommandée par un vaccin tétravalent conjugué ACYW et par le vaccin contre les IIM de sérogroupe B. Pour ces personnes, un rappel de vaccin tétravalent ACYW est recommandé tous les 5 ans.
- Si la personne a reçu antérieurement un vaccin tétravalent polyosidique non conjugué ACYW ou un vaccin polyosidique non conjugué A+C, un délai de 3 ans est recommandé avant de la vacciner avec un vaccin tétravalent conjugué ACYW.
3) Recommandations pour les professionnels
- La vaccination contre les IIM de sérogroupe B et de sérogroupes A, C, Y, W est recommandée chez les personnels des laboratoires de recherche travaillant spécifiquement sur le méningocoque.

E) Hépatite B : vaccin de l’hépatite B
La politique de vaccination contre l’hépatite B en France repose sur deux stratégies :
- l’identification et la vaccination des personnes à risque élevé d’exposition ;
- et, dans la perspective de contrôle à plus long terme de l’hépatite B, la vaccination des nourrissons et le rattrapage des enfants et adolescents jusqu’à l’âge de 15 ans révolus.
1) Recommandations générales
- La primovaccination (deux injections suivies d’un rappel) est obligatoire tous les enfants nés à compter du 1er janvier 2018.
- La vaccination des nourrissons est pratiquée avec un vaccin combiné, elle comporte deux injections à l’âge de 2 mois (8 semaines) et 4 mois, suivies d’un rappel à l’âge de 11 mois
- L’utilisation d’un vaccin combiné hexavalent contre la diphtérie, le tétanos, la coqueluche (vaccin acellulaire), la poliomyélite (vaccin inactivé), les infections à Haemophilus influenzae de type b et l’hépatite B permet d’immuniser les nourrissons contre ces maladies en une seule injection.
- Un rattrapage vaccinal est recommandé chez les enfants et les adolescents jusqu’à l’âge de 15 ans révolus. Tout enfant ou adolescent âgé de moins de 16 ans, non antérieurement vacciné, devrait se voir proposer la vaccination contre l’hépatite B à l’occasion d’une consultation médicale ou de prévention. Dans ce contexte, pour les adolescents de 11 à 15 ans révolus, un schéma simplifié à deux injections séparées de six mois peut être utilisé
2) Recommandations particulières
Bien que déjà ciblées par les recommandations générales, les catégories d’enfants et adolescents suivantes sont exposées à un risque particulier qu’il convient de souligner :
- enfants et adolescents accueillis dans les services et institutions pour l’enfance et la jeunesse handicapées ;
- enfants d’âge préscolaire accueillis en collectivité.
Sont en outre concernés les :
- nouveau-nés de mère porteuse de l’antigène HBs ainsi que ceux nés en Guyane ou à Mayotte ;
- enfants et adultes accueillis dans les institutions psychiatriques ;
- personnes ayant des relations sexuelles avec des partenaires multiples, exposées aux IST ou ayant une IST en cours ou récente ;
- usagers de drogues par voie parentérale ou intranasale ;
- voyageurs dans les pays de moyenne ou de forte endémie ;
- personnes amenées à résider en zones de moyenne ou de forte endémie ;
- personnes susceptibles de recevoir des transfusions massives et/ou itératives ou des médicaments dérivés du sang (hémophiles, dialysés, insuffisants rénaux...)
- personnes candidates à une greffe d’organe, de tissu ou de cellules ;
- personnes de l’entourage d’une personne atteinte d’hépatite B aigüe ou chronique (personnes vivant sous le même toit) ;
- partenaires sexuels d’une personne infectée par le virus de l’hépatite B ou d’un porteur chronique de l’antigène HBs ;
- personnes détenues qui peuvent cumuler un certain nombre de facteurs d’exposition au virus de l’hépatite B ;
- personnes porteuses d’une hépatopathie chronique ;
- personnes infectées par le VIH ou le virus de l’hépatite C.
La pratique de rappels systématiques n’est pas recommandée.
Toutefois chez les patients insuffisants rénaux chroniques dialysés et les personnes immunodéprimées exposées au risque, une sérologie annuelle (recherche d’anticorps anti-HBs) est recommandée avec pratique d’une injection d’une dose de rappel dès que le taux d’anticorps anti-HBs descend au-dessous du seuil protecteur (10 UI/L), quel que soit l’âge.
RATTRAPAGE VACCINAL
A) Généralité
1) Retard vaccinal 1
De nombreuses raisons peuvent amener des enfants ou adultes à accumuler un retard vaccinal :
- La négligence, des patients/parents ou des médecins, est certainement la plus importante.
- Les infections bénignes sont encore considérées, à tort, comme un motif de report des vaccins.
- Parfois, d’autres causes sont au premier plan : affections intercurrentes sévères/chroniques, traitements immunosuppresseurs, biothérapies ou immunoglobulines, accidents de la vie, changement de lieu de résidence, opposition des parents aux vaccins, précarité...
Quoiqu’il en soit, il est impératif de proposer un rattrapage vaccinal afin d’assurer une protection optimale au vu des antécédents et du nouvel environnement. Toutes les opportunités de rattrapage doivent être saisies (consultations, hospitalisations, embauche, entrée en collectivité…)
2) Les 7 règles de base de tout «rattrapage vaccinal»
- Chaque dose de vaccin reçue compte : « on ne recommence pas tout ».
- Tous les vaccins (inactivés ou vivants) peuvent être administrés le même jour.
- Dans le cas où ils ne sont pas administrés le même jour, aucun intervalle particulier n’a à être respecté entre des vaccins inactivés. Par contre un délai de 1 mois est recommandé entre 2 vaccins viraux vivants (Tableau).
- Protéger en priorité contre les infections les plus sévères : coqueluche avant 3 mois, infections invasives avant 2 ans, rougeole dès que possible, papillomavirus et hépatite B chez l’adolescent, tétanos à tout âge, etc.
- Effectuer le rattrapage le plus rapidement possible en profitant de toutes les occasions de vacciner, même en cas d’infection banale ...
- Terminer le rattrapage en tenant compte de la tolérance de l’enfant et des parents vis à vis du nombre d’injections à chaque séance et des possibilités denouvelles consultations dans des délais acceptables : classiquement, deux injections sont réalisées par séance mais, en cas de nécessité, 3 à 4 vaccins différents peuvent être injectés, toujours en des sites différents (distance d’au moins 2,5 cm entre 2 points d’injection).
- Chaque fois que possible, se recaler sur le calendrier en vigueur (pour DTCaP depuis 2013 : 2, 4, 11-12 mois, 6 ans, puis dTcaP 11-12 ans puis rappels adulte à 25-45- 65 ans puis tous les 10 ans).
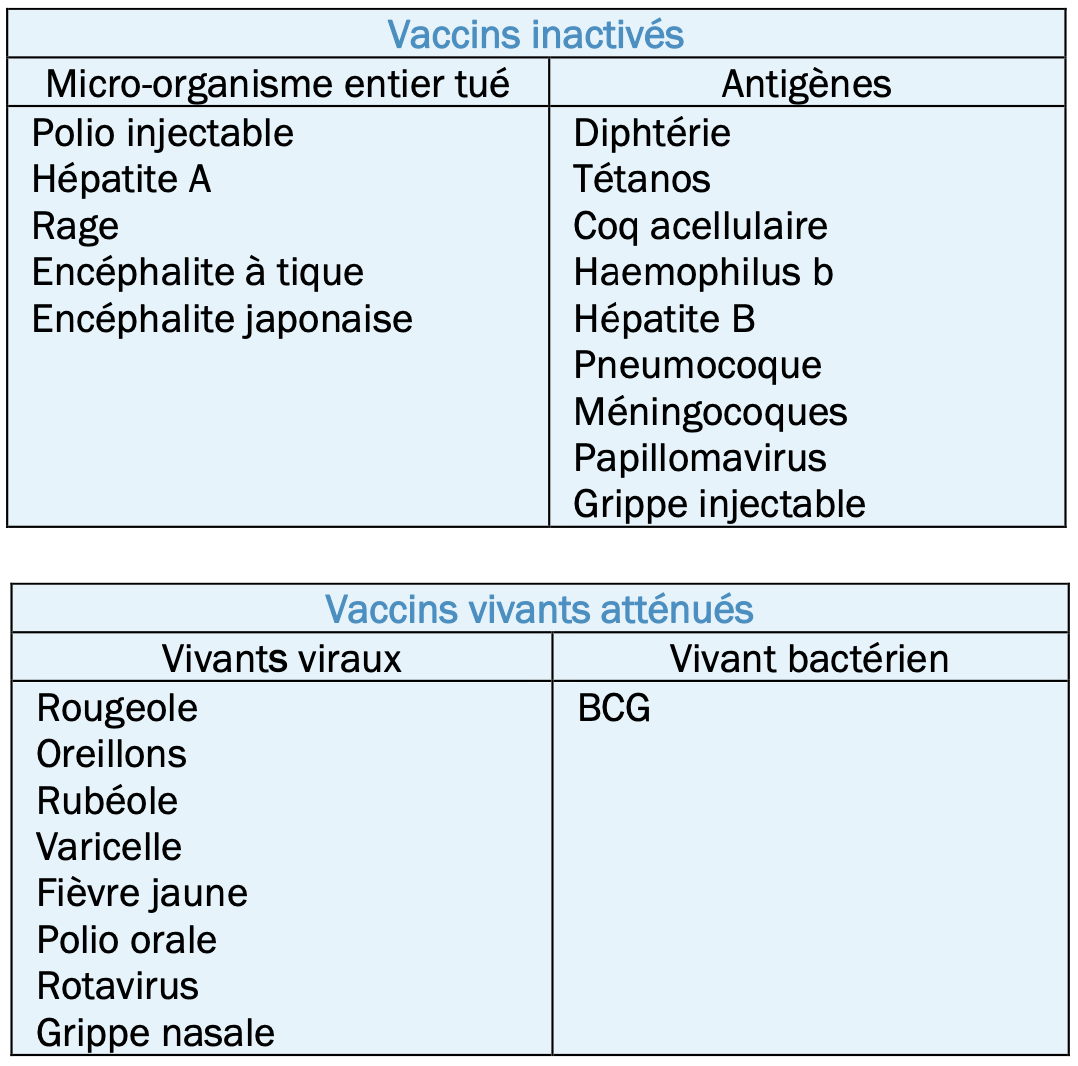
B) Procédures de rattrapage
1) Déterminer, pour chaque valence, le nombre de doses que le sujet aurait dû recevoir en tenant compte de 2 paramètres :
- l’âge lors du début de sa vaccination, le cas échéant
- l’âge au moment du rattrapage : non seulement chez le sujet jamais vacciné mais aussi en cas de vaccination incomplète.
On ne dépassera pas le nombre d’injections qui serait pratiqué si ce patient était primo-vacciné à cet âge.
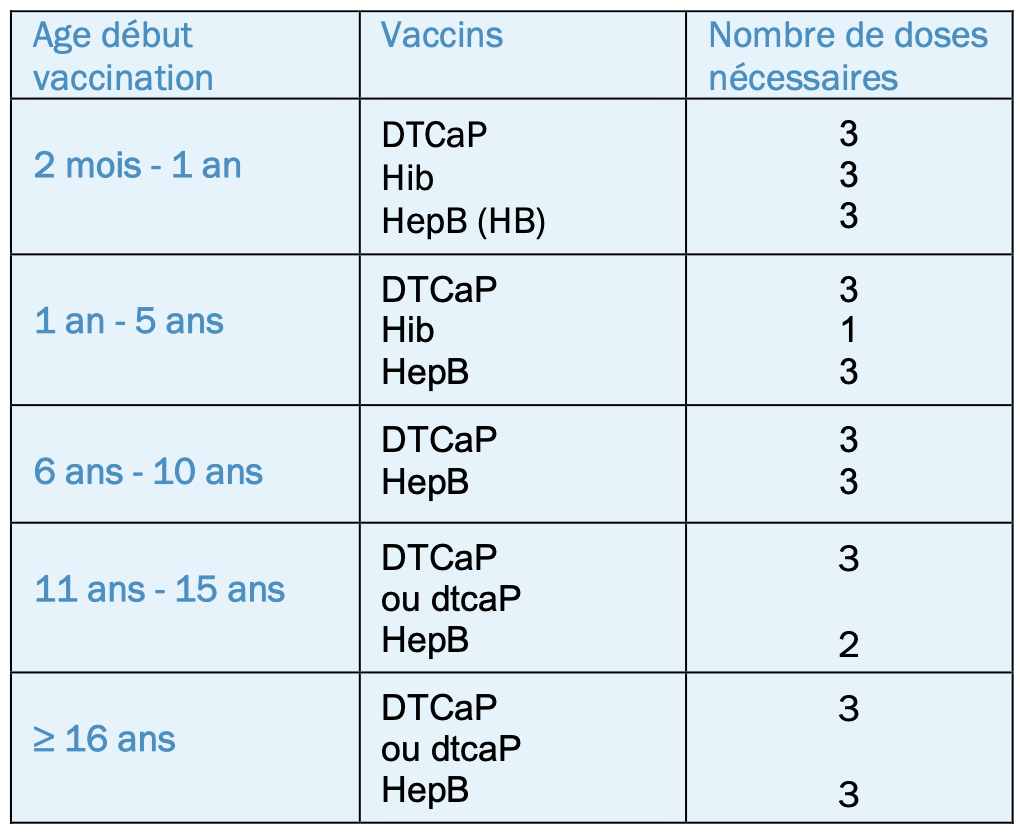
Exemple de rattrapage Hib : A 4 ans, pour la valence Hib, un enfant ayant eu une dose à l’âge de deux mois ne recevra qu’une seule dose puisqu’elle suffirait en primo-vaccination à cet âge-là.
2) Choisir, les combinaisons les plus « adaptées (permettant de réduire le nombre d’injections).
- Il n’existe pas ou plus de vaccin monovalent pour les maladies suivantes: Coqueluche, Diphtérie, Tétanos, Rougeole, Oreillons, Rubéole. (Encadré 2)
3) Proposer le schéma le plus raisonnable en nombre d’injections pour l’enfant
- Si l’utilisation des vaccins combinés permet de diminuer le nombre d’injections, on peut (on doit ?) les utiliser même si les combinaisons n’ont pas d’AMM à cet âge. (Encadré 3)
4) Respecter les intervalles optimaux entre les doses itératives :
- Primo-vaccination par DTPCaHibHB et Prevenar 13 : 2 mois d’intervalle pour les 2 premières doses (minimum 6 semaines). Si l’écart entre 2 doses est inférieur, la primo-vaccination doit être faite en 3 doses (c’était le schéma antérieur à 2013, avec un délai minimum entre chaque dose de 3 semaines)
- Pour les vaccins monovalents hépatite B et pour la vaccination HPV dans le cadre d’un schéma 2+1, un délai de 1 mois peut être acceptable entre les 2 doses de primo-vaccination, même si l’AMM indique 2 mois pour le Gardasil®.
- Pour être considérée comme dose de rappel, une dose doit être administrée au moins 5 à 6 mois après la dernière dose de primo-vaccination (minimum toléré : 4 mois), quel que soit le vaccin.
- Un délai d’un mois minimum est également nécessaire entre deux doses de vaccin ROR ou Varicelle (la 2ème dose n’est quasiment pas un rappel, mais essentiellement un rattrapage)

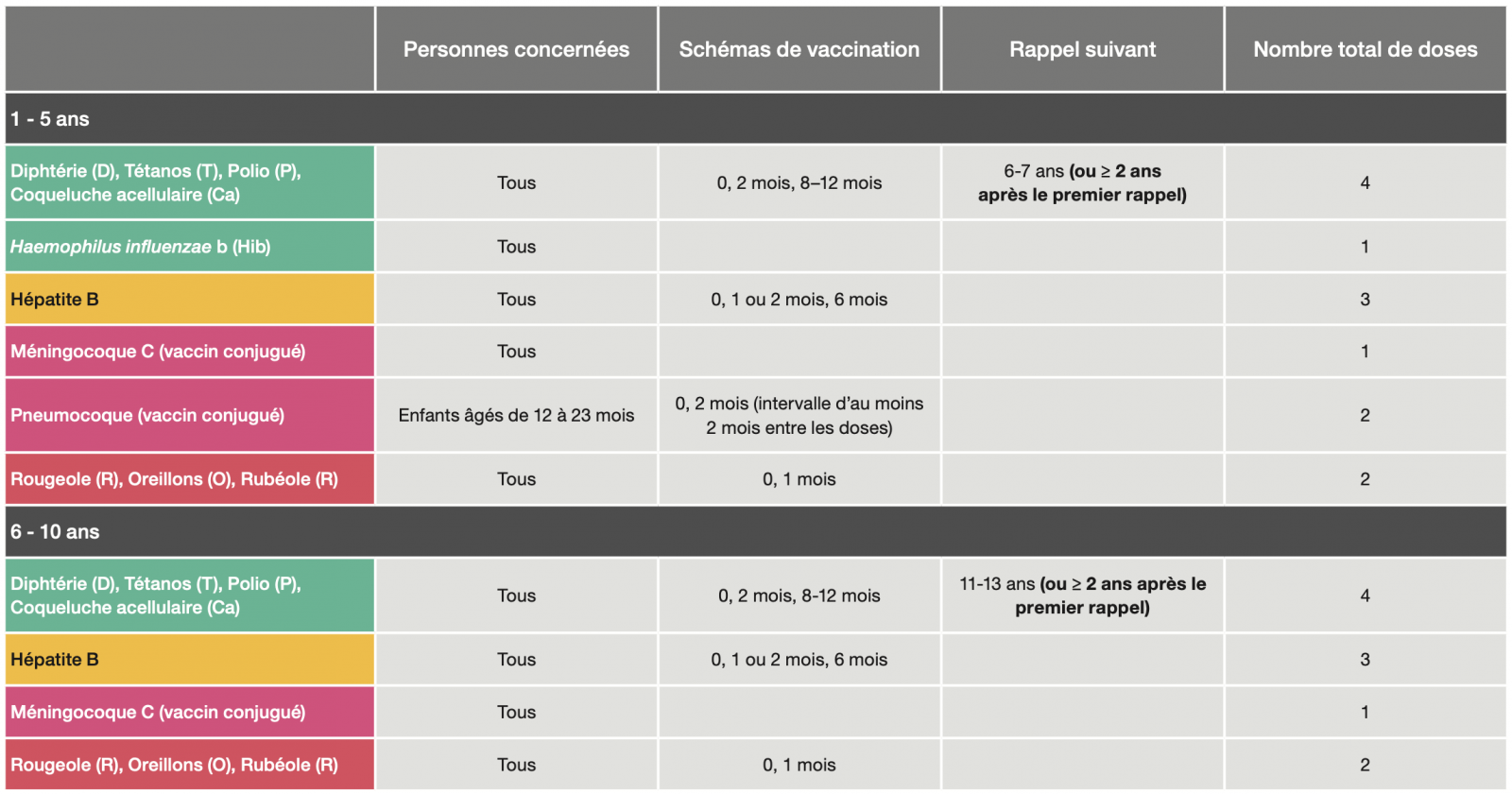
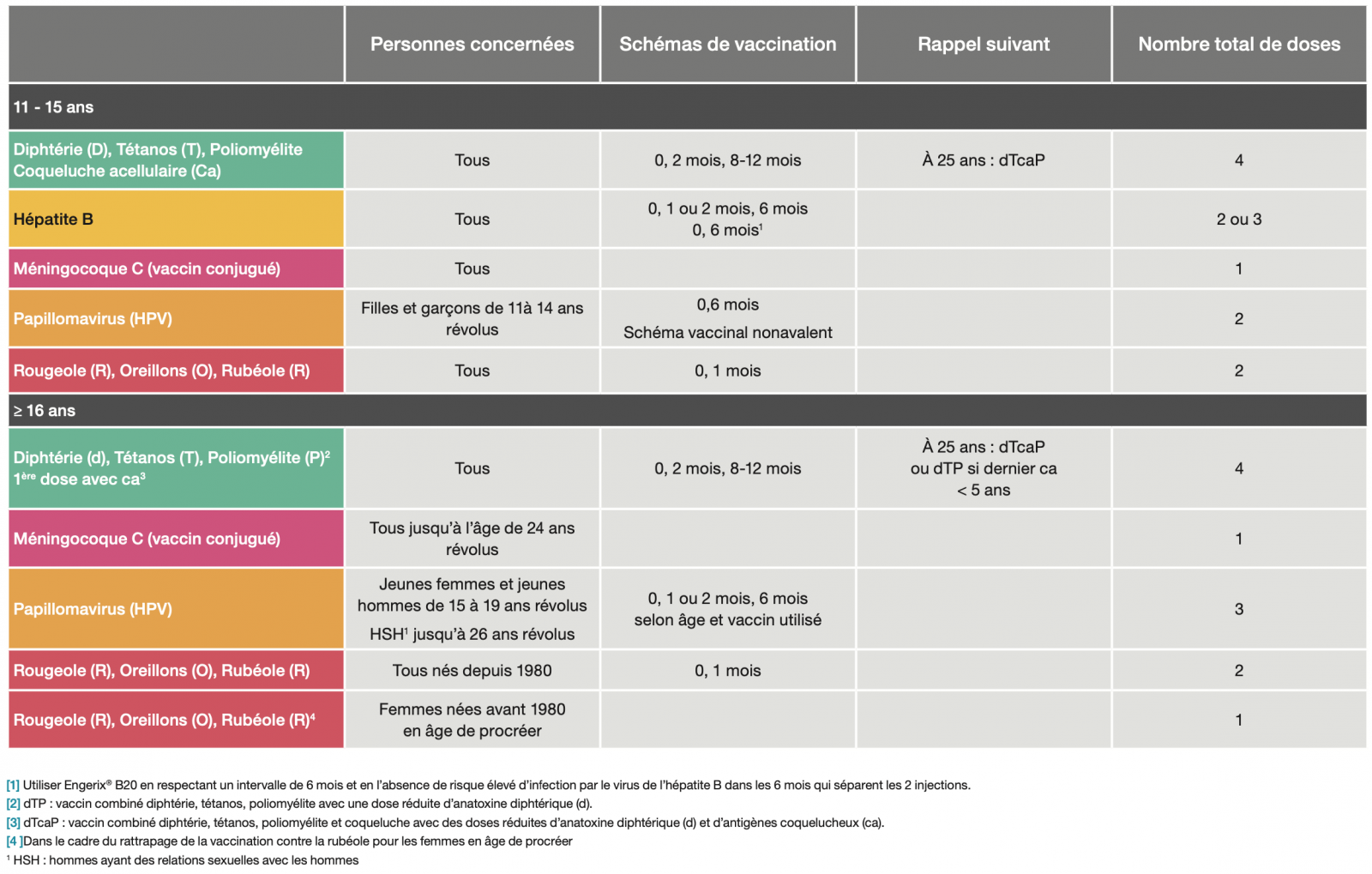
- Il faut faire la différence entre vaccins dosés pour la primo-vaccination des enfants et ceux pour adultes moins dosés en diphtérie, coqueluche et en tétanos.
- Il n’y a pas de données sur l’utilisation des vaccins faiblement dosés en diphtérie, tétanos et coqueluche pour une primovaccination, quel que soit l’âge, ni pour le rappel de 11 mois.
- Ces vaccins ne doivent donc en aucun cas être utilisés dans ces tranches d’âge.
C) Enfant à statut vaccinal connu
1) Diphtérie, Tétanos, Coqueluche, Poliomyélite, Haemophilus Influenzae type b (Hib), Hépatite B (HB)
- Le tableau 3 présente le schéma de rattrapage à proposer pour aligner les vaccinations sur le calendrier vaccinal français postérieur à 2013. Le nombre de doses correspond à la primo vaccination + le 1er rappel.
- Pour un sujet qui n’aurait jamais été vacciné, il indique le nombre de doses en fonction de l’âge du début de la vaccination.Pour un sujet incomplètement vacciné : il précise le nombre de doses qu’il aurait dû recevoir en fonction de l’âge qu’il avait lors de la première dose.
- Dans tout le texte l’utilisation de majuscules (D,T,Ca) ou de minuscules (dTca) permet de faire la différence entre vaccins dosés pour la primo-vaccination des enfants et ceux pour adultes moins dosés en diphtérie et coqueluche mais aussi en tétanos.
- Pour coqueluche « a » veut dire acellulaire. Les vaccins dTcaP ne sont pas uniquement faiblement dosés pour la valence diphtérique, ils le sont aussi pour les valences tétaniques et pour différents antigènes de la coqueluche (Tableau 4).
a) Diphtérie - Tétanos - Polio - Coqueluche
- Il n’y a pas de données sur l’utilisation des vaccins faiblement dosés en diphtérie, tétanos et coqueluche pour une primo- vaccination, quel que soit l’âge, ni pour le rappel de 11 mois. Ces vaccins ne doivent donc en aucun cas être utilisés dans ces tranches d’âge.
b) Haemophilus influenzae type b (Hib)
Le nombre de doses est fonction de l’âge au moment du rattrapage :
- de 6 mois à 12 mois : 2 doses + rappel
- de 1 an à 5 ans : 1 dose.
- après 5 ans, ce vaccin n’est plus nécessaire en population générale.
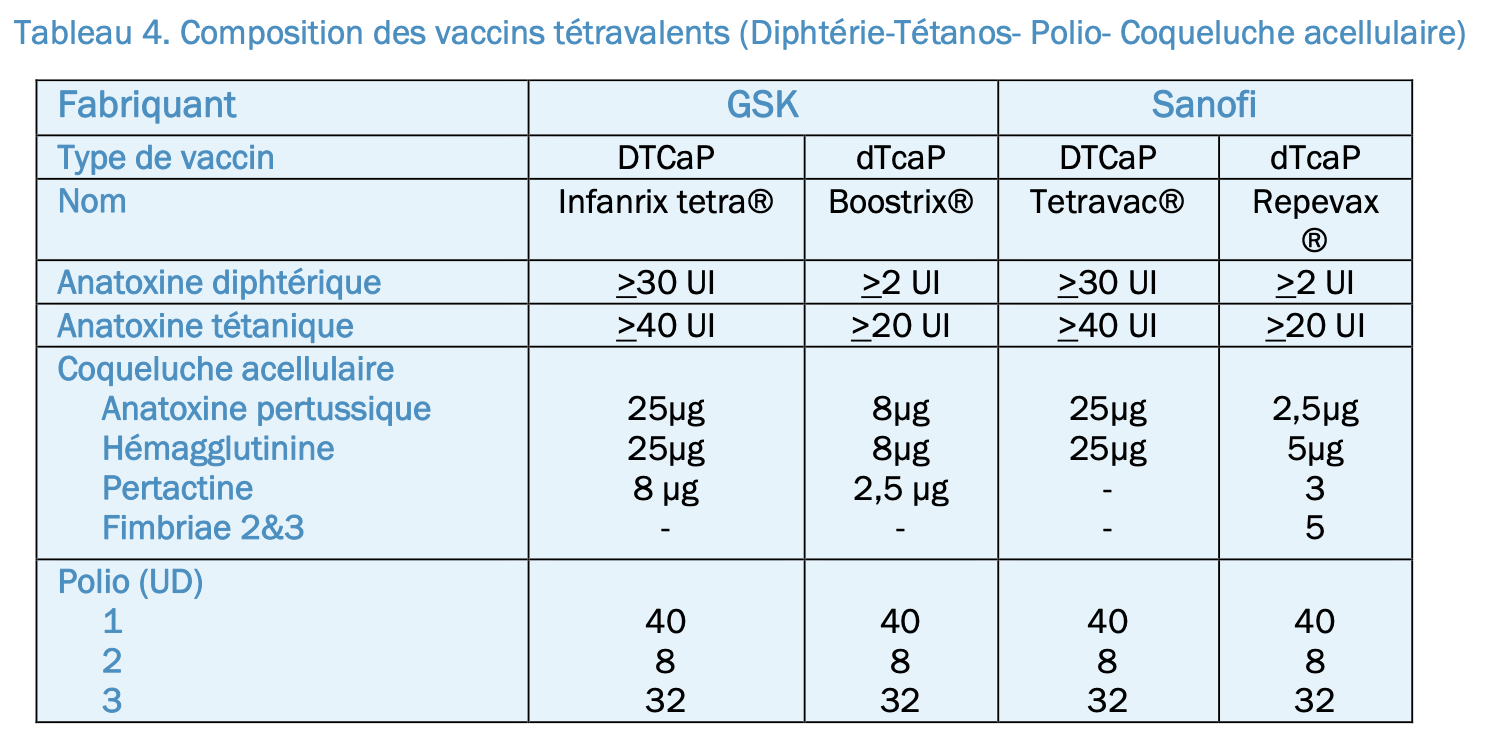
c) Hépatite B (hors risque professionnel ou départ en pays de forte endémie)
+ Absence de vaccination :
- Règle générale : 2 injections initiales à 1 ou 2 mois d’intervalle, rappel au moins 5-6 mois plus tard.
- Entre 11 et 15 ans : 2 injections de vaccins dosés à 20μg à 6-12 mois d’intervalle suffisent (en l’absence de risque élevé d’infection par le virus de l‘hépatite B dans l’intervalle). (Encadré 4)

d) Hépatite A + Hépatite B
Les vaccins combinés hépatite A + hépatite B offrent la possibilité de coupler la protection contre ces deux maladies ce qui est particulièrement utile avant un voyage dans des zones à risque pour l’hépatite A et pour les personnes jamais vaccinées contre l’hépatite B. Ils sont plus immunogènes contre l’hépatite B que les vaccins monovalents. Ils ont le défaut de ne pas être remboursés.
Les schémas proposés sont les suivants :
- Entre 11-15 ans : 2 Twinrix® adulte à 6-12 mois d’écart
- Entre 1 et 11 ans, deux possibilités :
- Soit 2 Twinrix enfant® à 1 ou 2 mois d’intervalle puis rappel Twinrix enfant 6 mois plus tard
- Soit 2 Twinrix adulte® à 6-12 mois d’intervalle (AMM européenne dès l’âge d’un an sous le nom d’Ambirix® qui est identique au Twinrix adulte®).
2) Rougeole, Oreillons, Rubéole (adulte : cf chapitre adulte)
- Depuis 2013, les recommandations françaises sont de pratiquer une 1ère injection à 12 mois, et une 2ème au moins un mois après, en général vers 16-18 mois.En cas de contage entre 6 et 10 mois, l’enfant doit recevoir une dose dans les 72 h puis deux doses suivant les recommandations du calendrier vaccinal.
- A partir de l’âge d’un an, tous les enfants et toutes les personnes nées depuis 1980, non vaccinés, doivent recevoir ou avoir reçu 2 doses de vaccin ROR, à au moins un mois d’intervalle.
3) Méningocoque C
- Depuis avril 2009, un vaccin conjugué était recommandé en population générale pour les enfants de 12 à 24 mois, avec rattrapage des personnes de 2 à 24 ans révolus.
- Cette stratégie partait du postulat qu’une très bonne couverture vaccinale (CV) entre 1 et 24 ans suffirait à protéger les plus petits qui sont la cible principale des méningocoques C (pic vers 3-5 mois).
- Cela a été un échec en raison de la faible CV obtenue. Il a donc été décidé de débuter la vaccination avec une dose à 5 mois tout en laissant une 2ème dose à 12 mois.
- En France, tant que le taux de CV des adolescents n’est pas suffisant pour empêcher le méningocoque C de circuler, comme c’est le cas actuellement au Royaume-Uni (grâce à l’immunité de groupe), il est par ailleurs prudent (recommandation InfoVac) de faire une 2ème dose de ce vaccin aux personnes de 11 à 24 ans ayant été vaccinées avant l’âge de 5 ans.
- En effet, le 2ème pic de fréquence des infections à méningocoque C survient chez l’adolescent et l’adulte jeune: c’est donc à ce moment-là qu’une protection optimale est souhaitable. Devant l’émergence du sérotype W depuis 2018, Infovac recommande d’utiliser pour cela un vaccin ACYW (Nimenrix®, Menveo®).
4) Pneumocoque
Le rattrapage peut concerner le vaccin pneumococcique conjugué Prevenar 13® (PCV13) et/ou le vaccin polyosidique non conjugué Pneumovax® (ex Pneumo23) (VPP23).
- Pour les nourrissons à risque élevé d’infection invasive à pneumocoque (IIP), le schéma comporte 3 doses à 4 semaines d’intervalle plus un rappel.
- Pour les nourrissons à terme < 12 mois : PCV13 en primo-vaccination en 2 doses, à 8 semaines d’intervalle. En cas de retard, faire la ou les doses manquantes dès que possible. Un rappel est recommandé à 11 mois mais avec un intervalle minimum de 5 à 6 mois après la deuxième dose de primo-vaccination. Si deux doses de primo-vaccination ont été faites par erreur avec moins de 6 semaines d’intervalle, revenir à un schéma en trois doses + rappel.
- Pour les enfants âgés de 12 à 23 mois, 2 doses de PCV13, à au moins 8 semaines d’intervalle sans rappel sont suffisantes.
- Pour les enfants âgés de 24 mois à 5 ans considérés comme à risque d’IIP :
- S’ils sont déjà vaccinés par le PCV13: une dose de vaccin VPP23, au moins 8 semaines après le dernier PCV13.
- S’ils n’ont jamais été vaccinés PCV13 : 2 doses de PCV13 à 8 semaines d’intervalle puis 1 dose de VPP23 au moins 8 semaines après
- Pour les patients âgés de 5 ans et plus, à risque élevé d’IIP :
- S’ils n’ont jamais été vaccinés contre le pneumocoque ou vaccinés avec le Prevenar 7®: une dose de PCV13 suivie, au moins 8 semaines plus tard, d’une dose de VPP23 sont recommandées.
- S’ils ont reçu uniquement le vaccin VPP23 : une dose de PCV13, au moins un an après puis une seule injection de VPP23 avec un délai minimal de 5 ans, sont considérées comme utile.
- Enfin, les personnes vaccinées suivant la séquence PCV13 - VPP23 pourront recevoir une seule nouvelle injection du VPP23 en respectant un délai de 5 ans.
5) Papillomavirus (HPV)
Plusieurs cas de figure sont aussi à considérer :
- Lorsque la première dose a été reçue avant 15 ans, la deuxième dose peut être administrée dès que possible en respectant un délai d’au moins 6 mois entre les deux doses. Quelle que soit la date de la seconde dose (même plusieurs années après) un schéma débuté avant 15 ans ne comportera que deux doses au total.
- Si la première dose a été réalisée après 15 ans, un schéma à 3 doses (2+1) est recommandé. Il faut rattraper la ou les doses manquantes en respectant unintervalle d’au moins un à deux mois entre les doses de primo-vaccination et d’au moins 4-5 mois entre la 2ème dose de primo-vaccination et le rappel.
- Si la vaccination a été débutée avec un vaccin bivalent (Cervarix®) ou quadrivalent (Gardasil®), il faut continuer la vaccination avec un vaccin nonavalent (Gardasil9®) en suivant les mêmes règles que précédemment. Cette recommandation d’InfoVac et de la très grande majorité des pays occidentaux est différente de celle de l’HAS en 2018 qui incite à poursuivre avec le même vaccin.
6) Varicelle
- Deux doses à au moins un mois d’intervalle sont nécessaires pour tous les patients de plus de 11 ans sans antécédent de varicelle et dont la sérologie est négative.En l’absence d’antécédent de varicelle, l’entourage des sujets immunodéprimés, du fait de leur maladie ou des traitements reçus, doit aussi être vacciné.
- Enfin les sujets sans antécédent de varicelle et devant commencer une biothérapie (pour une maladie inflammatoire digestive ou maladie rhumatismale...) doivent bénéficier de la vaccination avant le début du traitement.
D) Adulte jamais vacciné
- Si on se fie aux AMM, la situation est complexe : d’une part les vaccins DTCaP pédiatriques n’ont pas l’AMM chez l’adulte (faute d’étude) et d’autre part, les vaccins dTcaP n’ont pas l’AMM en primo-vaccination.
- Le choix vaccinal est donc à moduler en fonction du contexte :
- Si on a la quasi-certitude de non vaccination, il vaut mieux faire un vaccin pédiatrique DTCaP (Infanrix Tetra® ou Tetravac®). Les doses plus élevées des différents antigènes sont plus à même d’induire une réponse immunitaire en primo-vaccination.
- A contrario, s’il s’agit simplement d’un doute sur l’existence d’une vaccination dans l’enfance, les vaccins dTcaP et dTP sont à privilégier. En effet, Il y a un risque potentiel de réactogénicité accrue en cas de doses multiples de la valence diphtérie fortement dosée et il semble préférable d’utiliser des vaccins avec d. Un schéma mixte DTCaP puis dTcaP peut être envisagé en fonction du contexte.
E) Adulte incomplètement vacciné
1) Vaccination DTP chez l’adulte ayant eu au moins 5 doses dans l’enfance :
- Rattraper le calendrier vaccinal 25-45- 65 ans en refaisant une dose si la dernière a plus de 5 ans ou attendre le prochain rendez-vous vaccinal sans dépasser un intervalle de 25 ans depuis la dernière dose (règle 5-25 ans).
2) Coqueluche : une seule dose dTcaP est considérée en France comme suffisante.
- Un rappel coquelucheux avec le vaccin quadrivalent dTcaP (4) est recommandé, en particulier, à l’occasion du rappel diphtérie-tétanos-poliomyélite fixé à l’âge de 25 ans.
- Le « Cocooning » concerne les mères, pères et toutes les personnes susceptibles d’avoir un contact étroit et durable avec un nourrisson dans ses 6 premiers mois. Une dose de dTcaP est recommandée pour :
- Les personnes non antérieurement vaccinées contre la coqueluche.
- Les sujets de moins de 25 ans n’ayant pas reçu de vaccin coquelucheux depuis plus de 5 ans. ▪les adultes de plus 25 ans, si la vaccination coquelucheuse antérieure remonte à 10 ans ou plus.
- Un délai minimum de 1 mois est conseillé après le dernier vaccin dTP.
- Le recalage sur le calendrier en cours pour les rappels dTP ultérieurs se fera suivant les recommandations en cours (25- 45-65 ans puis tous les 10 ans).
- Si un patient a fait une coqueluche clinique documentée, il est considéré comme protégé contre cette maladie pour une durée de 10 ans : un vaccination avec un vaccin contenant une valence coquelucheuse bien que non dangereuse est inutile.
3) ROR : Toutes les personnes nées depuis 1980 doivent avoir reçu deux doses de vaccin rougeole-rubéole- oreillons.
- Les personnes nées avant 1980, non vaccinées et sans antécédent de rougeole (ou dont l’histoire est douteuse) exerçant une profession en charge de la petite enfance doivent avoir reçu une dose de rougeole-oreillons-rubéole (sans contrôle sérologique préalable).
- Les femmes nées avant 1980, non vaccinées contre la rubéole et ayant un projet de grossesse doivent avoir reçu ou recevoir une dose de vaccin.
De nombreux experts pensent que, quel que soit l’âge, pour les personnes non immunisées (absence de vaccination et/ou de maladie connue) contre la rougeole ou les oreillons ou la rubéole, deux doses de vaccin trivalent à >1 mois d’intervalle sont nécessaires. En effet, il n’y a aucune étude ou raison de penser que les sujets âgés aient une meilleure immunogénicité que les sujets plus jeunes pour lesquels 2 doses sont nécessaires.
F) Adulte à statut vaccinal indéterminé
- Aucun inconvénient à administrer un vaccin ROR, Hib, hép B ou polio à une personne éventuellement déjà immune pour ces maladies.
- Pour le tétanos et surtout la diphtérie, il existe cependant un risque théorique d’hyper-immunisation et d’hyper-réactogénicité (phénomène d’Arthus).
- Si doute sur la vaccination antérieure diphtérie, tétanos et hépatite B : faire une dose de vaccin puis faire un dosage des Anticorps antitétaniques et anti hépB (anti HBs), 4 à 12 semaines après. 1
G) Patient venant de l'étranger
- Pour les patients venant de l’étranger, il faut tenir compte du pays d’origine.
- En général, ils ont été vaccinés au moins par DT+Polio (Polio souvent oral).
- Le calendrier vaccinal de chaque pays se trouve sur le siteOMS :
- Attention, l’appellation DTP, dans les pays anglophones, correspond à Diphtérie-Tétanos-Coqueluche (P pour « pertussis », coqueluche).
Vaccination des populations spécifiques
A) Personnes immunodéprimées ou aspléniques 1 : Recommandations
Les personnes immunodéprimées ou aspléniques sont exposées à un risque accru d’infections sévères responsables d’une morbidité et d’une mortalité importantes. La vaccination en cas d’immunodépression présente certaines particularités qui justifient des recommandations spécifiques :
- le risque de survenue de maladie vaccinale après vaccination par vaccins vivants contre-indique de principe l’utilisation de ces vaccins chez l’immunodéprimé ; cependant, ces vaccins peuvent être envisagés dans certaines situations et au cas par cas, après avoir confronté le risque de la vaccination d’une part, et le risq u e d e la maladie infectieuse que l’on cherche à prévenir d’autre part :
- la diminution de l’immunogénicité des vaccins pouvant justifier des schémas vaccinaux particuliers ;
- un risque accru pour certaines infections justifiant la recommandation de vaccinations spécifiques.
La tolérance et l’efficacité des vaccins chez les personnes immunodéprimées sont conditionnées par la nature et l’intensité de l’immunodépression, qui sous-tend la fréquence du risque infectieux et sa gravité.
Il est possible de distinguer deux types de déficit immunitaire : les déficits immunitaires héréditaires et les déficits immunitaires secondaires ou acquis (infection par le VIH, transplantation d’organe solide ou de cellules souches hématopoïétiques, traitement immunosuppresseur, chimiothérapie et autres). Le déficit immunitaire est souvent difficile à quantifier et peut concerner l’immunité humorale et/ou cellulaire selon la situation clinique.
En dehors de l’infection par le VIH, les données disponibles concernant la vaccination des personnes immunodéprimées sont très peu nombreuses (peu de publications, peu d’études spécifiques) en ce qui concerne l’immunogénicité, l’efficacité clinique, la tolérance et l’impact sur la maladie sous-jacente. Dans un grand nombre de situations, les considérations théoriques priment, et les recommandations reposent sur des avis d’experts.
1) Les vaccins vivants atténués 1
- En général, les personnes immunodéprimées ou dont le statut immunitaire est douteux, ne doivent pas recevoir de vaccins vivants atténués, viraux ou bactériens, en raison du risque de survenue de maladie infectieuse vaccinale.
- Malgré les contre-indications ainsi que l’efficacité sub-optimale des vaccinations chez les patients immunodéprimés, certains patients peuvent bénéficier au cas par cas (analyse du ratio bénéfice/risque de la vaccination versus risque de la maladie) de vaccinations particulières, dont des vaccins vivants, possiblement en ciblant des intervalles de temps où l’immunodépression est moindre.
2) Les vaccins inactivés
- L’administration de vaccins inactivés ou subunitaires et d’immunoglobulines doit être effectuée de façon systématique, à partir des recommandations spécifiques pour les patients immunodéprimés car le risque d’effets indésirables n’est pas augmenté dans cette population.
- Le seul risque est celui d’une réponse immunitaire diminuée, ce qui est fréquent en cours d’immunodépression et qui peut donc nécessiter, pour améliorer l’immunogénicité, des schémas de vaccination intensifiés.
- La capacité de développer une réponse correcte dépend du type et de la date de survenue de l’immunodépression. Pour certains vaccins, le dosage des anticorps sériques protecteurs peut être proposé quatre à six semaines après la vaccination pour vérifier l’existence d’une réponse immune à la vaccination et éventuellement proposer des doses supplémentaires de vaccin, notamment dans le cadre de la vaccination contre l’hépatite B.
-
Le vaccin inactivé contre la grippe saisonnière doit être administré rigoureusement chaque année.
-
Le vaccin contre le pneumocoque est fortement recommandée pour les populations pédiatriques et adultes d’immunodéprimés, d’autant plus qu’il existe un vaccin polysaccharidique conjugué qui a fait preuve d’une meilleure immunogénicité par rapport au vaccin polysaccharidique seul.
-
Il est également recommandé de maintenir les rappels diphtérie-tétanos-poliomyélite avec un intervalle raccourci de dix ans.
-
Si l’immunodépression est transitoire, comme après l’arrêt d’une chimiothérapie ou d’une biothérapie, la réponse immunitaire redevient correcte entre trois mois et un an environ après l’arrêt du traitement, les vaccinations pourront reprendre.
-
Dans certaines situations où l’immunogénicité est diminuée, la forme clinique sévère ou encore si la vaccination n’est pas recommandée (vaccin vivant, par exemple), une prophylaxie par immunoglobulines pourra être envisagée.
-
Remarque : Une latence d’au moins 5 mois est à respecter après un traitement d’immunoglobulines ou l’administration de produits sanguins.
B) Patient asplénique : Recommandations
- Asplénie anatomique (splénectomie chirurgicale ou asplénie congénitale) ou fonctionnelle (drépanocytose, réaction du greffon contre l'hôte).
- Il est prioritaire de vacciner les patients aspléniques contre les bactéries encapsulées (méningocoques, pneumocoque, Haemophilus influenzae b).
- Il n’existe aucune contre-indication vaccinale chez les sujets aspléniques.
- En cas de splénectomie programmée, il est recommandé de vacciner si possible au moins deux semaines avant l’intervention.

c) Femmes enceintes
1) Avant la grossesse :
- Les vaccinations doivent être mises à jour dans la mesure du possible, au cours d’une consultation pré-conceptionnelle, en particulier pour le vaccin ROR, le vaccin contre la coqueluche et le vaccin contre la varicelle.
2) Pendant la grossesse :
- Le vaccin grippal injectable est recommandé quel que soit le stade de la grossesse (pris en charge par l’assurance maladie).
- Les vaccins vivants ROR, varicelle et BCG sont contre-indiqués pendant la grossesse. La grossesse doit être évitée dans le mois qui suit la vaccination avec un vaccin vivant.
-
Vaccin DTP : Les données sur la toxicité embryo-fœtale sont rassurantes. Pour la diphtérie, un vaccin à valence réduite est recommandé afin d’éviter les réactions fébriles (dTP). En attendant une future recommandation de vaccination contre la coqueluche durant la grossesse, il est préférable de reporter la vaccination dTP jusqu’à la fin de la grossesse et de vacciner la mère immédiatement après l’accouchement avec un vaccin quadrivalent contenant la valence coqueluche.
-
Vaccin coqueluche : Aucune complication n’a été rapportée en cas de vaccination pendant la grossesse. À ce jour, en France, cette vaccination est recommandée aux femmes en pré-conceptionnel, pendant la grossesse aux autres membres du foyer et à la mère dans le post-partum immédiat (stratégie du cocooning). Cependant, dans de nombreux pays, elle est recommandée au 3e trimestre de grossesse.
Quel que soit le niveau de recommandation (recommandée ou déconseillée), si la vaccination est justifiée du fait d’un voyage imprévu en zone endémique ou d’un contexte épidémique, elle doit être réalisée.
Cependant :
- Une vaccination avec un vaccin vivant, réalisée par inadvertance au cours de la grossesse n’est pas une indication à interrompre la grossesse.
- La vaccination contre la fièvre jaune de la femme enceinte peut être justifiée lors de séjour en zone d’endémie après évaluation du rapport bénéfice-risque. Chez la femme allaitante, la vaccination contre la fièvre jaune doit être reportée tant que le nourrisson n'a pas atteint l'âge de 6 mois, sauf en cas de situation épidémique.
- Compte tenu des données disponibles concernant la vaccination des femmes enceintes, la réalisation des autres vaccins au cours de la grossesse se justifie en cas de risque infectieux (contexte épidémique, risque professionnel, séjour en zone à risque …)
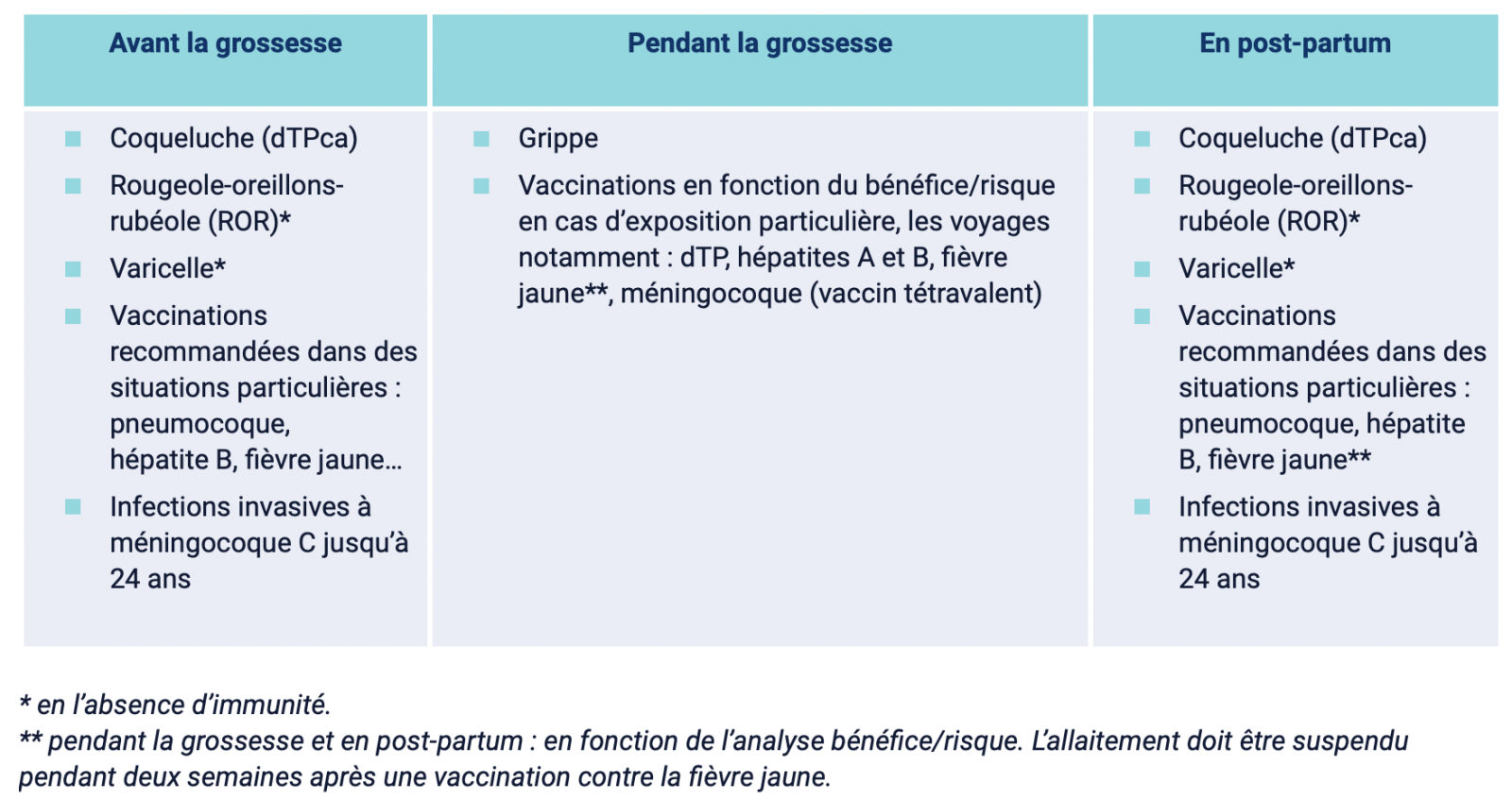
3) Après la grossesse
- La période post natale sera l’occasion de procéder à cette mise à jour si elle n’a pu être réalisée avant la grossesse en particulier pour les vaccins ROR, le coqueluche et varicelle.
4) Allaitement
- En dehors de la vaccination contre la fièvre jaune, il n’y pas lieu de suspendre l’allaitement pour les autres vaccinations
D) Prématurés 1
- Le prématuré est exposé à un risque infectieux accru en termes d’incidence et de gravité, en particulier pour la coqueluche.
- La vaccination de routine doit débuter à 2 mois d’âge chronologique, quel que soit le degré initial de prématurité.
- Leur immaturité immunologique est responsable d’une réponse à la vaccination inférieure à celle observée chez le nouveau-né à terme, en particulier du vaccin contre Hib.
- Toutefois, le prématuré est capable de répondre de manière satisfaisante aux vaccins dès l’âge de 8 semaines. Il n’y a pas de données justifiant un schéma renforcé pour la vaccination contre l’Haemophilus influenzae de type b.
1) Vaccination contre la coqueluche
- Elle est particulièrement indiquée en raison du risque accru de complications de la maladie chez le prématuré.
- Toutefois le prématuré est exposé à un risque spécifique d’apnée/bradycardie durant les 48h suivant la 1ère injection d’un vaccin combiné contenant la valence coquelucheuse.
- Ce risque est particulièrement identifié (8 % à 50 %) chez les nourrissons < 33 semaines d’aménorrhée et/ou de poids de naissance inférieur à 1 500 g, ayant eu des antécédents d’apnée, d’oxygéno-dépendance ou de broncho-dysplasie pendant la période postnatale.
- Ce risque disparaît au-delà de 60-70 jours de vie.
- Chez le prématuré qui présente ces facteurs de risque, il est donc recommandé d’administrer la première dose de vaccin hexavalent avant sa sortie de la maternité (le cas échéant, de le ré-hospitaliser) et de le garder sous monitoring cardio-respiratoire pendant 48 heures.
- En cas d’apnée ou de bradycardie lors de la première vaccination, une récidive est possible lors de la deuxième injection.
2) Vaccination contre pneumocoque
- La vaccination avec le vaccin conjugué 13-valent est indiquée chez le prématuré et le schéma vaccinal est renforcé.
- Les prématurés ont plus de risques d’infections invasives à pneumocoque.
- Le schéma vaccinal du prématuré comprend une primovaccination renforcée à trois doses de vaccin pneumococcique conjugué 13-valent (Prevenar 13) à 2, 3 et 4 mois, suivies d’un rappel à l’âge de 11 mois.
3) Vaccination contre hépatite B
Chez le grand prématuré, des études ont montré une corrélation inverse entre le poids de naissance et le taux de séroconversion après une vaccination commencée à la naissance avec 3 doses de vaccin contre l’hépatite B : (55% pour les poids de naissance < 1000g, 71% pour les poids de naissance compris entre 1000 et 1500 g, 96% pour les poids de naissance supérieurs à 1500 g).
- Les réponses sont satisfaisantes pour les enfants de plus de 2000g à la naissance ou les enfants dont la vaccination a débuté à 2 mois, quel que soit leur poids de naissance. Les enfants de mère non porteuse de l’AgHBs peuvent être vaccinés dès 2 mois d’âge réel.
- Les enfants nés de mère porteuse de l’AgHBs, doivent impérativement être vaccinés à la naissance selon un schéma à 3 doses (naissance, à 1 mois et à 6 mois). La 1ère dose étant associée à l’administration d’immunoglobulines anti-HBs.
- Un schéma de vaccination à 4 doses (1 à la naissance, puis à 1, 2 et 6 mois) est recommandé pour les prématurés de moins de 32 semaines ou de poids inférieur à 2 kg.
- Dans les deux cas, un contrôle sérologique des marqueurs (AgHBs et Ac anti-HBs) devra être effectué à partir de l’âge de 9 mois, au mieux un à quatre mois après la dernière dose, pour vérifier l’efficacité de la protection
.png)
Nouveau-né de mère AgHBs positive :
- Prématuré > 32 SA ou poids de naissance >2 kg : schéma à trois doses. Vaccin monovalent HBVAXPRO® 5μg ou ENGERIX®B10µg : 1 dose à la naissance simultanément aux immunoglobulines anti-HBs, puis à 1 et à 6 mois.
- Prématuré < 32 SA ou poids de naissance <2 kg : schéma à quatre doses. Vaccin monovalent vaccin HBVAXPRO® 5μg ou vaccin ENGERIX®B 10µg : une dose a la naissance simultanément aux immunoglobulines anti-HBs, puis à 1, 2 et 6 mois. Pour la dose à l’âge de 2 mois il est recommandé de remplacer le vaccin monovalent par un vaccin hexavalent
E) Vacciner les personnes âgées 1
- Le risque d’infection, en particulier d’infections graves croît avec l’âge (immunosénescence).
- Il est d’autant plus important qu’il existe une altération des statuts nutritionnel et fonctionnel ainsi que, des comorbidités ou une poly-médication.
- L’incidence des infections grippales, à pneumocoque et des zonas est augmentée dans la population âgée et tout particulièrement dans la population âgée dépendante avec des conséquences sévères en termes de morbi-mortalité.
- La vaccination contribue à la prévention de ce risque infectieux.
- Cependant, la réponse vaccinale s’altère avec l’âge.
- C’est la raison pour laquelle, la fréquence des rappels est augmentée et que la vaccination antigrippale est recommandée également chez les professionnels interagissant avec les sujets âgés.
F) Cas particulier du zona 1
- Dans le calendrier des vaccinations, la vaccination est recommandée chez les adultes âgés de 65 à 74 ans.
- Couverture vaccinale : la vaccination contre le zona est actuellement sous-utilisée en France puisque moins de 10% des personnes éligibles sont vaccinées, alors qu’en Grande-Bretagne, 61,8% des personnes éligibles ont reçu ce vaccin en 2013-2014.
- Recommandations : Sur la base de son AMM, le vaccin Zostavax® peut être proposé chez les personnes > 50 ans, qu’elles aient déjà eu la varicelle ou non, pour diminuer le risque de zona et surtout le risque de douleurs de névralgies post-zostériennes. Le fait d'avoir eu un zona ne protège pas d'une rechute et justifie le fait de vacciner également ces patients.
G) Voyageurs
Le programme de vaccination à établir pour chaque voyageur doit tenir compte de plusieurs facteurs.
- L’évaluation des risques réels encourus par le voyageur (épidémies, situation sanitaire, hygiène, conditions de séjour, facteurs de risque individuels, statut vaccinal antérieur).
- L’obligation administrative de présenter un certificat de vaccination pour entrer dans certains pays, soit dans le cadre du Règlement sanitaire international (vaccination contre la fièvre jaune), soit du fait d’une exigence particulière du pays d’accueil.
- La nécessité de réaliser les vaccinations au moins 15 jours avant le départ (délai plus court pour les rappels vaccinaux).
- La mise à jour des vaccinations recommandées en France dans le calendrier vaccinal (certaines des infections visées peuvent être endémiques dans le pays de destination).
1) Où s'informer :
Les recommandations figurant dans le Bulletin épidémiologique hebdomadaire hors-série « Recommandations sanitaires pour les voyageurs », qui paraît tous les ans au printemps, peuvent ne pas prendre en compte l’évolution des risques et l’émergence de nouvelles maladies infectieuses.
Les recommandations aux voyageurs sont donc susceptibles d’être actualisées en fonction de l’évolution de la situation internationale. Pour être informé de ces mises à jour, il est conseillé de consulter un des sites suivants : https://www.hcsp.fr/explore.cgi/avisrapportsdomaine?clefr=719
- Site du Ministère des Solidarités et de la Santé
- Site du Ministère de l’Europe et des Affaires Etrangères
- Site de Santé publique France
- Site de l'Organisation Mondiale de la Santé
2) Où se faire vacciner
Certains vaccins ne se font que dans des centres de vaccinations internationales ou des centres agréés pour la vaccination contre la fièvre jaune
Les centres de vaccinations spécialisés :
CONTRE-INDICATIONS AUX VACCINS
Les véritables contre-indications à la vaccination sont exceptionnelles. Les textes d’AMM des vaccins comportent les contre-indications et sont régulièrement mis à jour, par exemple :
- dans le Répertoire des spécialités pharmaceutiques sur le site de l’ANSM
- dans la Base de données publique des médicaments
A) Véritables contre-indications
- Allergie grave connue à l’un des composants du vaccin.
- Réaction allergique grave lors d’une précédente injection du vaccin. En cas de réaction allergique bénigne (urticaire), la vaccination peut être poursuivie avec des précautions particulières (médicament anti-histaminique).
- La vaccination par un vaccin vivant est contre-indiquée chez les malades dont le système immunitaire est déficient (immunodéficience cellulaire, infection avancée à VIH/SIDA (CD4 < 500/µl entre 1 et 5 ans, <200/µl à partir de 6 ans) et qui prennent un traitement immunosuppresseur (en particulier, prednisone >=2 mg/kg/jour ou 20 mg/jour pendant > 14 jours, chimiothérapie, biothérapie).
B) Fausses idées sur les contre-indications
- Contrairement à l’opinion publique, les épisodes infectieux mineurs, l’asthme, l’eczéma, les dermatoses chroniques, les affections chroniques cardiaques, respiratoires, rénales, hépatiques, les séquelles neurologiques, le diabète, la malnutrition et la prématurité ne constituent pas des contre-indications aux vaccinations. Les contre-indications seront discutées en fonction de chaque vaccin et de la situation clinique rencontrée.
- La fièvre n’est pas une contre-indication absolue tout comme la prise d’antibiotiques mais selon l’état clinique du patient, il peut être recommandé de reporter d’une semaine la vaccination…
C) Et l’allergie à l’œuf ?
- Chez les patients allergiques à l’oeuf, les vaccins ROR (cultivés sur fibroblastes de poulets), et les vaccins grippe, fièvre jaune, et encéphalite à tiques (cultivés sur des œufs embryonnés de poule) font peur aux patients, mais aussi aux médecins, qui trop souvent les contre-indiquent dans cette population.
- Les mentions légales accompagnant ces vaccins renforcent la conviction des médecins de leur dangerosité chez les allergiques à l’oeuf.
- Les vaccins actuels contiennent, pour la plupart, des quantités infimes de protéines d’oeuf (grippe) ou n’en contiennent pas (ROR).
- Ils sont seulement contre-indiqués chez les personnes ayant des antécédents d’accidents d’allergie graves à l’ingestion d’œufs.
D) Des mentions légales qui n’incitent pas à la vaccination
- Les vaccins contre ROR indiquent : « les sujets ayant des antécédents de réactions anaphylactiques, anaphylactoïdes ou autres réactions immédiates (par exemple : urticaire généralisée, gonflement de la gorge et de la bouche, difficultés respiratoires, hypotension ou choc) suite à l’ingestion d’oeufs peuvent être plus à risque de développer une réaction d’hypersensibilité immédiate suite à la vaccination, bien que ces types de réactions ne soient observés que très rarement » (mention légale, avril 2009).
- Les vaccins grippe saisonnière et grippe H1N1 sont contre-indiqués chez l’allergique à l’oeuf (Vidal® 2010).
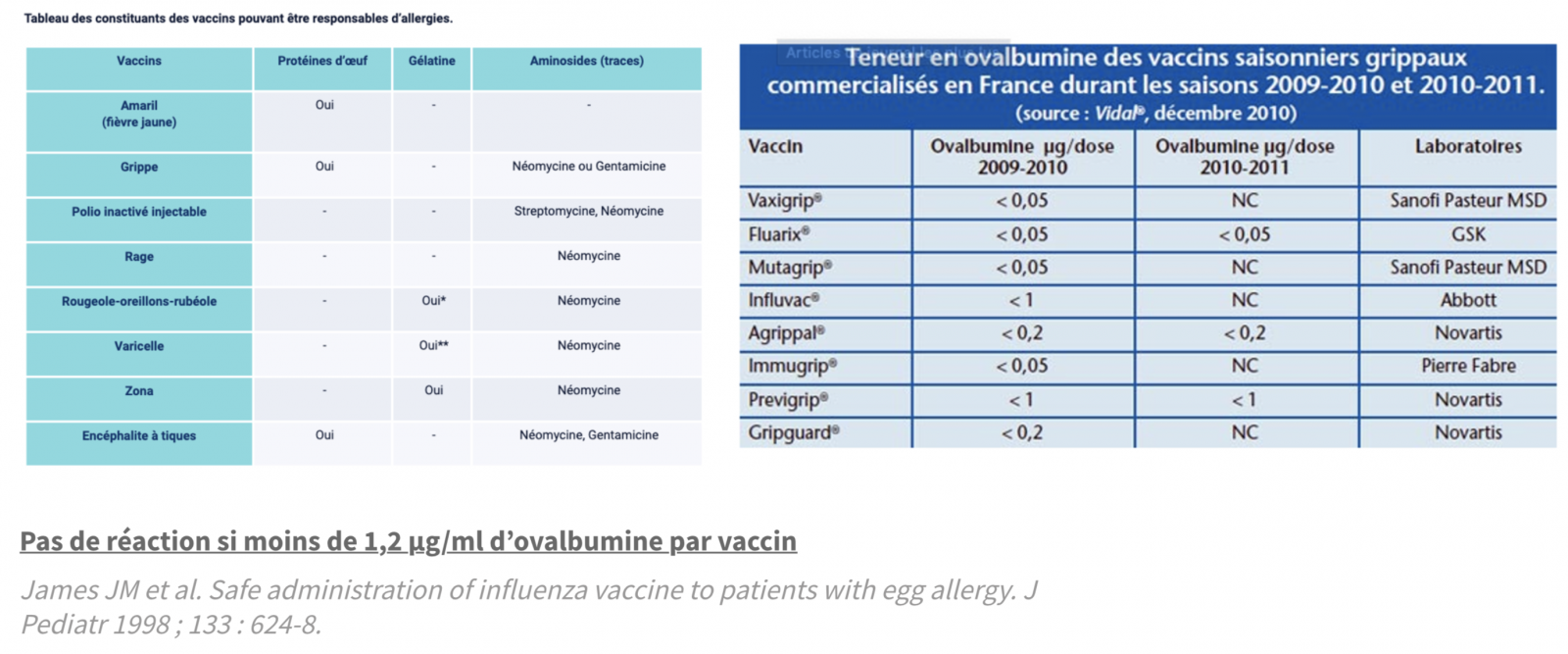
- Il paraît urgent de modifier les notices légales des différents vaccins pour les mettre en accord avec les connaissances récentes. 1
- La prudence actuelle des notices est un frein pour une couverture vaccinale ROR et grippale.
- Les notices actuelles ne permettent pas aux médecins praticiens de vacciner en toute quiétude leurs patients allergiques à l’oeuf pour ROR et grippe.
- Ces patients sont souvent référés en consultation spécialisée hospitalière, ce qui est une source non négligeable de dépense de santé inutile.
- Une campagne d’information de tous les médecins pratiquant les vaccinations est indispensable pour transmettre cette information.
E) En pratique
Le caractère parfois imprévisible de l’allergie, et en particulier de sa forme grave, la réaction ou le choc anaphylactique, impose que tout vaccinateur, dans son cabinet, dispose des moyens thérapeutiques immédiats pour y faire face. 1
1) Un certain nombre de précautions s’appliquent à la vaccination des personnes allergiques :
- ne pas vacciner lors d’une poussée évolutive de la maladie ;
- s’assurer que le vaccin utilisé ne contient pas d’antibiotiques en traces (par exemple la néomycine) chez des patients qui seraient allergiques;
- prescrire un antihistaminique le matin même de la vaccination et poursuivre le traitement jusqu’à deux jours après celle-ci.
- en cas d’antécédents d’allergie supposée à un vaccin, il convient de faire préciser le type clinique de réaction et de rechercher l’allergène en cause. Si le bilan allergologique n’est pas possible dans un bref délai et si la vaccination est urgente, on peut envisager une épreuve de tolérance, consistant à évaluer la sensibilité du sujet avec une solution de vaccin dilué dans du sérum physiologique. Ces épreuves doivent être pratiquées par des équipes entraînées, avec une voie veineuse en place.
- Les allergies supposées, non avérées, ou les allergies chez des proches de la famille ne sont pas des contre-indications. Les seules contre-indications sont les réactions anaphylactiques chez la personne à vacciner.
2) Place du bilan allergologique
Le bilan allergologique permet d’identifier les patients présentant un risque réel de développer une réaction anaphylactique en cas de nouvelle exposition. La revaccination dépendra alors de ce bilan allergologique. Cependant, différents cas de figure sont à distinguer :
- Si la réaction est uniquement locale, aucun bilan allergologique n'est nécessaire. Il ne s'agit pas d'une réaction IgE médiée associée à un risque plus élevé de réaction anaphylactique lors d'une prochaine vaccination.
- Si la réaction n'est pas immédiate, l’évaluation clinique suffit et une investigation allergologique est inutile. Ce type de réaction n’est pas dangereux. Le risque d'hypersensibilité immédiate suite à la revaccination est faible. Par exemple, une réaction urticarienne bénigne post-vaccinale ne contre-indique donc pas une nouvelle vaccination. Pour assurer le confort du patient, celle-ci peut se faire sous couverture antihistaminique orale pendant 48 heures.
- Si l'anamnèse suggère une réaction immédiate de type anaphylactique, un bilan allergologique est impératif. Les réactions anaphylactiques imposent un bilan allergologique comportant des tests cutanés à lecture immédiate et des RAST (radio allergo sorbent test) aux divers antigènes vaccinaux, même si la valeur diagnostique et prédictive de ces tests est controversée.
Bénéfices individuels et collectifs de la vaccination
A) Bénéfices Individuels
- La dimension individuelle consiste en l’induction d’une protection chez la personne vaccinée grâce au déclenchement par le vaccin d’une réaction immunitaire spécifique contre l’agent infectieux concerné.
- Comme nous l’avons décrit dans le module sur les mécanismes d’action, tous les vaccins n’ont pas la même capacité à induire une réponse immunitaire protectrice. Tous les vaccins destinés aux nourrissons (à l’exception du vaccin contre la coqueluche dont l’efficacité se situe autour de 90%), ont une efficacité d’au moins 95%.
- Cela signifie que moins de 5% des nourrissons vaccinés ne sont pas protégés.
- Les durées de protection sont différentes selon les vaccins : elles varient de seulement quelques années pour la coqueluche, à plusieurs décennies, voire à vie, pour la rougeole, la rubéole ou l’infection par le virus de l’hépatite B.
B) Bénéfices Collectifs
- Au-delà de sa propre protection, la personne vaccinée va également contribuer à protéger d’autres personnes qu’elle-même.
- En effet, la vaccination évite la multiplication de l’agent pathogène chez la personne vaccinée.
- Une personne vaccinée n’est donc plus susceptible de transmettre le microbe à son entourage, évitant ainsi à ses proches, et en particulier ceux qui ne sont pas vaccinés, d’être contaminés, de développer la maladie et de disséminer le virus ou la bactérie dans la population générale.
-
La personne vaccinée agit, vis-à-vis du reste de la population, comme une barrière contre l’agent pathogène, en interrompant la chaine de transmission.
-
Plus la population est vaccinée, plus on réduit la circulation de la bactérie ou du virus concerné.
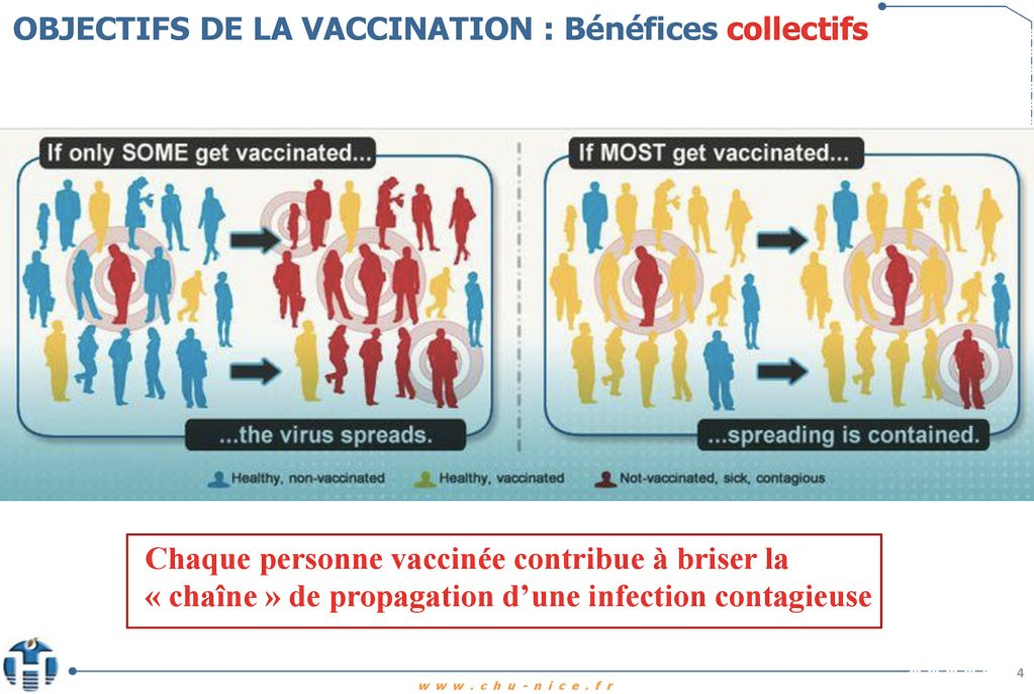

- Cet exemple illustre le fait qu’une couverture vaccinale de 50% de la population permet de réduire le nombre de cas d’une proportion supérieure à 50%.
- Non seulement les sujets vaccinés ne tombent plus malades mais ils ne contaminent plus leur entourage.
Exception :
- Parmi les vaccins aujourd’hui inclus dans le calendrier vaccinal, seule la vaccination contre le tétanos n’est pas concernée par cette dimension collective.
- En effet, la contamination se fait à partir des spores tétaniques telluriques et la maladie ne se transmet pas de personne à personne.
- En France, malgré une couverture vaccinale des nourrissons de 99%, on a recensé, entre 2012 et 2016, 3 cas de tétanos chez des enfants très vraisemblablement non vaccinés, âgés entre 3 et 8 ans.
1) Immunité de groupes
De tels effets de protection collective des sujets réceptifs constituent ce qu’on appelle l’immunité de groupe.
Ces effets vont bénéficier à plusieurs catégories de personnes :
- les enfants trop jeunes pour être vaccinés,
- les personnes qui ne sont pas ou plus protégées par le vaccin qu’elles ont reçu
- et celles qui, bien que ciblées par les recommandations vaccinales présentent une contre-indication.
Si la couverture vaccinale est suffisamment élevée, cette diminution de l’incidence de la maladie affectant l’ensemble de la population, vaccinée et non vaccinée, peut permettre d’éradiquer une maladie. Cela a été le cas pour la variole et a permis d’interrompre la vaccination. Ce succès a été obtenu sans avoir besoin d’obtenir 100% de couverture vaccinale dans tous les pays du monde, ce qui aurait été impossible.
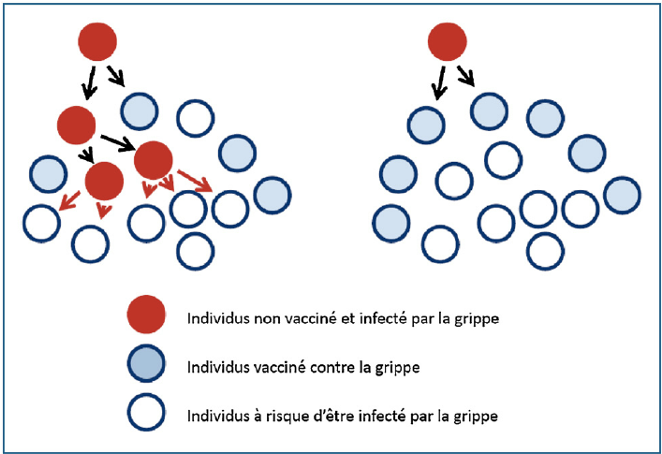
2) Immunité de groupe : effet limité
- Ce succès permis par l’immunité de groupe ne doit pas faire oublier que l’effet barrière qu’elle induit peut être limité dans le temps et dans l’espace.
- Dans le temps car, sauf si la couverture vaccinale est suffisamment élevée pour faire disparaître l’agent infectieux, il reste des malades dans la population, et les sujets réceptifs pourront finir un jour ou l’autre par rencontrer un de ces malades et être contaminés. Ils feront la maladie à un âge plus tardif que lorsque l’agent pathogène circulait librement.
- Pour les maladies dont la sévérité augmente avec l’âge, ceci entraîne donc un risque accru de complications.
- Ce risque disparaît si la couverture vaccinale est suffisamment élevée pour interrompre totalement la circulation de l’agent.
- Cet effet négatif est donc la conséquence d’une mise en œuvre insuffisante de la stratégie de vaccination.
- Exemple : vaccination contre la Varicelle.
3) Des succès
- L’élimination, en France, de la diphtérie et de la poliomyélite, les quasi-disparitions des méningites à Haemophilus influenzae b, de la rubéole et des oreillons résultent d’une combinaison d’une protection individuelle de la quasi-totalité des enfants, reflet d’une couverture vaccinale très élevée, et de l’induction par cette couverture élevée d’une immunité de groupe.
4) Des échecs
- A contrario, les niveaux insuffisants de couverture vaccinale atteints pour la vaccination contre la rougeole, au regard de sa très grande transmissibilité, ainsi que pour la vaccination contre le méningocoque C, n’ont pas permis d’induire une immunité de groupe suffisante pour éliminer ces maladies, à l’origine de résurgences épidémiques de la maladie de grande ampleur comme cela fut le cas entre 2008 et 2012 pour la Rougeole.
a) Cas de la rougeole :
- Atteindre une couverture vaccinale > 95% permettrait d’éviter les cas qui surviennent chez des enfants ou des adultes qui ne peuvent être vaccinés et qui constituent les populations les plus à risque de forme grave de la maladie (nourrissons < 1 an et personnes avec contre-indication au vaccin).
- Lors de l’épidémie de 2008-2012, 7% des cas, sont survenus chez des nourrissons de moins de 1 an et, parmi les 10 décès qui ont été rapportés aux agences régionales de santé, 7 sont survenus chez des sujets immunodéprimés.
- Tous ces cas et ces décès auraient été évités grâce à l’immunité de groupe, si une couverture vaccinale plus élevée avait été atteinte et avait permis d’interrompre la circulation du virus.
b) Cas du méningocoque C
- La vaccination contre le méningocoque C a été introduite en 2010 dans le calendrier vaccinal français, en 1 injection chez les enfants de 1 an avec rattrapage jusqu’à 24 ans pour un double objectif : protéger les enfants et jeunes adultes d’une pathologie aiguë rare mais très sèvère, et induire une immunité de groupe suffisante pour protéger les nourrissons de < 1 an sans avoir à ajouter au calendrier de vaccination les 3 doses nécessaires à la vaccination avant 1 an.
- Le suivi de couverture vaccinale et la surveillance épidémiologique ont montré l’échec de cette stratégie.
- La couverture à 2 ans était, fin 2016, de 71%, et elle diminue très rapidement avec l’âge : 26% chez les 15-19 ans et 10% chez les 20-24 ans.
- L’incidence des infections à méningocoque C a augmenté entre 2010 et 2014, en particulier chez les nourrissons, très vraisemblablement à cause d’un nouveau cycle épidémique que l’insuffisance de la vaccination n’a pas réussi à contrôler. Si la couverture vaccinale avait été suffisamment élevée pour induire une immunité de groupe, une très grande partie des plus de 70 décès survenus entre 2011 et 2017 chez des personnes de moins de 1 an ou de plus de 24 ans aurait été évitée, au-delà de la trentaine de décès survenus chez des sujets non vaccinés âgés de 1 à 24 ans. En effet, aux Pays-Bas, il a été observé la quasi-disparition des infections à méningocoque C grâce à une couverture vaccinale très élevée chez les enfants de 1 à 18 ans.
Fausses idées reçues sur les vaccins
- La vaccination sauve tous les ans 2 à 3 millions d’enfants dans le monde, mais 1,5 million meurt encore chaque année de maladies qui peuvent être évitées par la vaccination.
- 1 enfant sur 5 dans le monde n’a toujours pas accès à la vaccination selon l’Unicef.
- La poliomyélite n’est toujours pas éradiquée, le tétanos pas complètement éliminé, et la rougeole continue de tuer.
- Et pourtant dans les pays industrialisés, les idées reçues et les anti-vaccins continuent…
A) Polémique n°1 vaccin contre l’hépatite b et la sclérose en plaques
- Durant les années 1990, des cas de SEP survenus après une vaccination anti-VHB ont été rapportés.
- Ces notifications sont survenues dans un contexte de très large activité de vaccination dans des populations chez qui elle était recommandée mais aussi chez des adultes non à risque (75 millions de doses fin 1997).
- En 1998, la médiatisation de ces cas a conduit les pouvoirs publics, malgré l’absence de preuves d’un lien quelconque, à interrompre la campagne de vaccination en milieu scolaire, tout en maintenant la vaccination en ville.
- La possibilité d’un lien entre vaccination anti-VHB et SEP a été explorée par de nombreux travaux épidémiologiques. À ce jour, aucun lien statistiquement significatif n’a été montré. La Commission nationale de pharmacovigilance française a donc estimé, en 2011, que les données scientifiques n’avaient pas permis de démontrer l’existence d’une association significative entre le risque de survenue de SEP et la vaccination contre l’hépatite B. Cet avis est en accord avec les avis rendus par d’autres pays dans le monde. Les données constituées depuis plus de 15 ans permettent d’écarter avec une grande sûreté un lien entre vaccination contre le virus de l’hépatite B et la survenue d’une sclérose en plaques. Ce vaccin n’est pas associé à un sur-risque de développer une SEP. Il n’est pas contre-indiqué en cas de SEP préexistante ou d’antécédent familial de SEP. À ce jour, environ 1,5 milliard de doses de vaccin anti-VHB ont été administrées dans le monde.
1) Paradoxe dans le domaine judiciaire
- Ces considérations scientifiques sont parfois prises en compte de façon paradoxale dans le domaine judiciaire lorsque, par exemple, des professionnels de santé atteints de SEP qu’ils estiment secondaire au vaccin anti-VHB font une démarche d’indemnisation.
- La Cour européenne de justice a d’ailleurs estimé, en 2017, que le fait qu’il n’existe pas de preuve scientifique ne doit pas complètement fermer la porte à une possible indemnisation d’un plaignant.
- « En l’absence de consensus scientifique, le défaut d’un vaccin et le lien de causalité entre celui-ci et une maladie peuvent être prouvés par un faisceau d’indices graves, précis et concordants ». Cour de justice de l’Union européenne. Communiqué de presse n°66/17. Luxembourg, le 21 juin 2017. Arrêt dans l’affaire C-621/15 N. W e.a./Sanofi Pasteur MSD e.a.
2) Etudes épidémiologiques vaccin hépatite B et SEP : 1 1 1 1 1 1 1 1 1 1 1 1
B) Polémique n°2 vaccin ROR et autisme
- En 1998, le journal médical britannique de référence The Lancet publie une étude remettant en cause l’innocuité du vaccin ROR.
- Le travail porte sur 12 enfants et conclut que le vaccin est responsable d’un tableau combinant autisme et troubles digestifs (« autistic enterocolitis »).
- Le chirurgien Andrew Wakefield, premier auteur de la publication, organise à l’occasion de cette publication une conférence de presse dans un hôpital londonien et appelle les parents à immuniser leurs enfants avec un vaccin monovalent contre chacune des trois maladies, qu’il déclare moins dangereux que le vaccin combiné.
- La presse britannique va relayer et donner une grande ampleur à ces propos, qui font rapidement leur effet auprès de l’opinion publique. Cette controverse a eu comme conséquence au Royaume-Uni une baisse importante de la couverture vaccinale du ROR dès l’année 1998, provoquant la résurgence de la rougeole (en régression constante depuis 1994, elle est ainsi redevenue d’actualité à partir de l’année 2000, deux ans après la publication de l’article).
-
La progression du nombre de cas de rougeole est ainsi directement imputable à la controverse provoquée par Wakefield.
-
La couverture vaccinale n’est repartie à la hausse qu’en 2005-2006. En parallèle, les conclusions de l’article d’A. Wakefield ont progressivement été remises en cause sur un plan scientifique.
-
D’une part, sur un plan épidémiologique, aucune des études menées sur des populations importantes ne mettait en évidence de lien entre ROR et des troubles du spectre autistique.
D’autre part, il apparaissait que les données présentées dans cet article résultaient d’une fraude :
- les enfants ne présentaient pas de lésions digestives,
- le délai entre la vaccination et les signes d’autisme n’était pas celui qu’avaient rapporté les parents,
- et leur inclusion dans l’étude résultait de la volonté de leurs parents de poursuivre le fabricant du vaccin et non de la constatation d’un état clinique particulier.
- L’article est désavoué par le Lancet en 2010.
L’enquête sur l’étude est publiée un an plus tard dans le British Medical Journal et révèle deux aspects supplémentaires de la fraude :
- A. Wakefield était rétribué avant la parution de son article par un cabinet d’avocats, dans le but d’asseoir un lien scientifique entre la vaccination et une maladie, ce qui faciliterait la mise en œuvre d’une plainte à grande échelle,
- A. Wakefield prévoyait de commercialiser un test de dépistage pour « l’entérocolite autistique », test dont la rentabilité était estimée à plusieurs dizaines de millions de livres par an.
Cet épisode peut donc se résumer comme :
- la publication dans des conditions problématiques d’un travail scientifique frauduleux,
- réalisé pour servir des intérêts financiers,
- et qui, du fait d’un grand écho médiatique,
- va être associé à une perte de confiance dans le vaccin,
- une baisse de la couverture vaccinale
- et une résurgence d’une maladie infectieuse ;
- Et cela alors qu’aucun travail scientifique n’était venu corroborer les résultats de l’étude initiale.
- Le Royaume-Uni, épicentre de cette controverse qui, du fait de sa rédaction en langue anglaise, s’est largement répandue.
- Elle persiste dans de nombreux esprits malgré la révélation de la fraude et le fait que des dizaines d’études épidémiologiques et physiopathologiques n’ont jamais mis en évidence un lien quelconque entre le ROR et l’autisme.
- En 2019, une nouvelle étude danoise de grande ampleur, menée par Anders Hviid, vient conforter cette absence de lien. Tous les enfants danois nés entre 1999 et 2010 (plus de 650 000) ont été suivis jusqu’en 2013. De nombreuses données ont été prises en compte, notamment les antécédents d’autisme dans la famille, l'âge des parents, le tabagisme pendant la grossesse, la prématurité, le score d’Apgar et le poids de naissance/périmètre crânien.
- L’étude permet d’affirmer que le ROR n’augmente pas le risque d’autisme, ne déclenche pas d’autisme chez les enfants ayant des facteurs de risque et n’est pas associée à l’apparition de cas groupés d'autisme à des temps donnés après la vaccination.
C) Polémique n°3 adjuvants vaccinaux et aluminium
-
Les adjuvants vaccinaux sont indispensables à l’efficacité de très nombreux vaccins. Ils sont utilisés pour augmenter la réponse immunitaire contre l’antigène microbien contenu dans la plupart des vaccins autres que les vaccins vivants. Les sels d’aluminium sont les adjuvants les plus utilisés dans le monde avec un recul d’utilisation de quatre-vingt-dix ans et des centaines de millions de doses injectées.
-
L’aluminium n’est pas un composant minéral de l’organisme humain et sa présence est toujours d’origine exogène. L’exposition à l’aluminium provient essentiellement des aliments, de l’eau, de médicaments tels que certains pansements gastriques et médicaments anti-acides, des onguents, des anti-perspirants, des adjuvants vaccinaux aluminiques et parfois d’une exposition accidentelle ou professionnelle. La neurotoxicité de l’aluminium n’a été décrite que pour des intoxications massives aiguës ou des consommations chroniques à des doses élevées, ainsi que chez les dialysés ou les prématurés nourris par alimentation parentérale.1
-
Les apports totaux (non professionnels) sont estimés à 3-15 mg/jour. Chez les sujets sains, on retrouve de l’aluminium dans de nombreux tissus (os, poumon, foie) ainsi que dans le cerveau [190 ng/g (20-400 ng/g)]. La dose d’aluminium maximum contenue dans les vaccins utilisés en France chez le nourrisson est de 0,82 mg, inférieure à la limite supérieure de 1,25 mg figurant dans la monographie des vaccins de la Pharmacopée européenne.1
-
La dose d’aluminium administrable par voie intraveineuse sans toxicité documentée est comprise entre 1 et 2 mg.1
-
Il n’existe à ce jour aucune preuve de toxicité neurologique imputable à l’aluminium issu de l’alimentation ou des adjuvants.

1) Myofasciite à macrophages et aluminium
Une équipe de recherche française du centre de référence des maladies neuromusculaires du CHU de Créteil a émis, en 1998, l’hypothèse d’une responsabilité de l’aluminium utilisé comme adjuvant vaccinal dans l’apparition d’une nouvelle entité nosologique appelée « myofasciite à macrophages (MFM) ».
Cette appellation recouvre 2 entités distinctes :
a) La MFM, histologique, reconnue scientifiquement
- La MFM histologique est caractérisée par une lésion inflammatoire localisée au point d’injection vaccinal : cristaux d’aluminium localisés au niveau des macrophages de la lésion.
- Des macrophages, recrutés dans le muscle, phagocytent l’hydroxyde d’aluminium et peuvent persister sur le site de la vaccination pendant plusieurs mois/années.
- L’association entre cette lésion et l’aluminium contenu dans les vaccins, mise en évidence par cette équipe de recherche, ne fait aucun doute et fait l’objet d’un consensus des organismes scientifiques nationaux ou internationaux concernés. Elle est ainsi considérée comme une cicatrice ou un tatouage vaccinal.
b) La MFM maladie.
La même équipe considère que cette entité histologique peut être associée à des signes cliniques, tels que myalgies, arthralgies, fatigue persistante et troubles cognitifs, regroupés dans le syndrome de fatigue chronique (MFM-maladie).1 Elle affirme que, pour certaines personnes génétiquement prédisposées, les macrophages ayant phagocyté l’aluminium vaccinal ne seraient pas capables de l’assimiler et des nanoparticules migreraient dans le cerveau où leur dépôt serait à l’origine de la symptomatologie. 1 1
Plusieurs éléments doivent être pris en compte pour évaluer la pertinence de cette hypothèse :
- D’une part, dans la mesure où une biopsie musculaire n’est pratiquée que chez des patients symptomatiques, il est attendu d’identifier des signes chez tous les patients porteurs de la lésion histologique MFM.
- D’autre part, l’étude cas-témoins menée par l’Afssaps en 2002 n’a pas permis de conclure à une association entre la lésion histologique et l’existence d’un syndrome clinique spécifique, ce qui a amené le comité scientifique de l’Afssaps à conclure en mai 2004 qu’ « aucun syndrome clinique spécifique n’est retrouvé associé à la vaccination avec des vaccins contenant un adjuvant aluminique ».1 1
2) Position des institutions scientifiques en france
- L’alerte lancée par l’équipe du Professeur Gherardi en 1998 a fait l’objet d’un suivi et d’une analyse régulière par les autorités de santé et les institutions nationales et internationales. L’Académie de médecine en 2012, le Haut Conseil de la santé publique en 2013, puis l’Académie de pharmacie en mars 2016, ont publié des rapports sur les adjuvants et les vaccins.1 1 1
- Ces trois institutions ont conclu qu’il n’existait pas de lien de causalité entre les signes cliniques et la présence d’aluminium dans les vaccins.
- Pour l’Académie de médecine, « aucune preuve de toxicité neurologique imputable à l’aluminium de l’alimentation ou des vaccins n’a pu encore être fournie à ce jour ».
- Pour le Haut Conseil de la santé publique, « le lien entre la vaccination et la présence dans les muscles de granulomes contenant de l’aluminium est reconnu mais aucune étude dans la littérature ne permet d’affirmer le lien de causalité entre les signes cliniques rapportées et la présence de granulomes contenant de l’aluminium ». « Les récents travaux chez la souris dans des conditions expérimentales non transposables à l’homme et à la vaccination, apportent des éléments éclairant le mode de transport de l’aluminium dans divers organes dont le cerveau sans apporter d’éléments démontrant sa nocivité ni de lien entre une éventuelle présence cérébrale et les manifestations cliniques de la MFM ».
- Enfin, l’Académie de pharmacie « constate que, même si certaines manifestations cliniques sévères ont pu être associées à des injections vaccinales, aucun lien de causalité n’a pu être établi à ce jour avec les adjuvants, d’autant que ces manifestations paraissent limitées dans le temps (…) et dans l’espace (…). »
- Ces trois institutions ont convenu de la nécessité de poursuivre les recherches quant au devenir de l’aluminium vaccinal.
3) MFM à l’international ?
- Aucune autre équipe, indépendante de l’équipe française, n’a publié de résultats expérimentaux qui viendraient conforter les conclusions de l’équipe française ces 20 dernières années.
- L’OMS a soumis à plusieurs reprises les données disponibles à son groupe d’expert sur la sécurité du vaccin, qui a invariablement conclu à l’absence de données permettant de conclure à l’association entre l’administration de vaccins contenant des adjuvants aluminiques et la survenue d’une maladie.
D) Polémique n°4 : vaccins et mort inattendue du nourrisson (MIN)
- Le questionnement sur un éventuel lien de causalité entre les vaccins et survenue d’une MIN a émergé dans les années 1970 suite à l’introduction, en 1966, du premier vaccin tétravalent (Tetracoq®).
- En effet, l’introduction du vaccin a coïncidé avec une période d’augmentation rapide du nombre de décès par MIN entre 1975 et 1980.
- Cependant, association temporelle n’est pas causalité.
-
De nombreux travaux ont montré par la suite que la forte augmentation du nombre de cas de MIN à partir des années 1970 était en fait à mettre en lien avec l’adoption, à cette époque, de la position ventrale pour coucher les bébés, reconnue ultérieurement comme facteur de risque majeur de MIN. En outre, un certain nombre de MIN survient avant l’âge de 2 mois et avant toute vaccination. Enfin, une diminution très importante du nombre de MIN a été observée dans les années 1990 suite aux campagnes de prévention préconisant le couchage sur le dos et de meilleures literies.
-
Une méta-analyse s’appuyant sur plusieurs études cas-témoins a été menée pour répondre à la question de l’existence d’un éventuel lien de causalité entre vaccination et mort inattendue du nourrisson.
-
Aucun lien de causalité entre vaccination et MIN n’a été démontré dans cette méta-analyse, la vaccination pourrait, au contraire, avoir un effet protecteur avec un OR multivarié de 0,54 (IC 95% ; 0,39-0,76). - Plusieurs hypothèses peuvent être avancées pour expliquer un tel résultat :
- la contribution de la coqueluche à la mort inattendue du nourrisson voire un effet non spécifique de l’induction par la vaccination d’une immunité contre différents agents pathogènes qui pourraient être impliqués dans la MIN.
- un biais d’indication qui pourrait également contribuer à cette protection : la MIN survient parfois dans un contexte infectieux. Or, les bébés qui ne sont pas en parfaite santé sont moins souvent vaccinés, les médecins préférant reporter la vaccination. Dans cette hypothèse, le moindre risque de MIN chez les nourrissons vaccinés traduirait le fait que la vaccination est plus un marqueur d’un meilleur état de santé qu’un facteur de protection.1
-
E) Polémique n°5 : vaccin HPV et maladies auto-immunes
- En France, la controverse sur le lien supposé entre maladie auto-immune (MAI) et la vaccination anti-HPV est née en 2013 suite à la survenue, dans les 2 mois suivant la 2nde injection de Gardasil®, d’une sclérose en plaque chez une adolescente.
- Les parents de cette jeune fille ont alors déposé une plainte contre le laboratoire fabricant, d’une part, et contre l’Agence nationale de la sécurité du médicament (ANSM), d’autre part, pour « violation d’une obligation manifeste de sécurité et méconnaissance des principes de précaution et [de] prévention ».
- Suite aux conclusions en faveur d’un lien causal émises par la Commission régionale de conciliation et d’indemnisation des accidents médicaux (CRCI) d’Aquitaine saisie par les parents, une plainte collective a été également déposée pour dénoncer un lien de causalité entre les maladies auto-immunes dont les plaignantes étaient atteintes et les vaccins anti-HPV qu’elles avaient reçus. Cette affaire a été relayée par les médias nationaux pendant plusieurs semaines.
-
En novembre 2015, le Parquet du pôle de santé du Tribunal de grande instance de Paris a classé l’enquête sans suite, considérant qu’il n’y avait pas de lien de causalité direct entre le vaccin Gardasil® et les maladies auto-immunes (MAI) que présentaient les plaignantes. Cet avis s’est appuyé notamment sur les résultats de l’étude pharmaco-épidémiologique sur la sécurité d’utilisation de la vaccination anti-HPV réalisée par l’ANSM et l’Assurance maladie à partir de l’analyse des bases de données médico-administratives françaises. Depuis les conclusions du Tribunal de grande Instance de Paris, il n’y a pas eu d’autres affaires médiatisées.1
-
À la suite des plaintes déposées contre l’ANSM et le fabricant, l’ANSM et l’Assurance maladie ont publié, en 2015, les résultats d’une grande étude qui avait pour but d’estimer les risques absolus et relatifs de MAI chez les jeunes filles vaccinées, comparativement à celles non vaccinées. Il s’agit d’une étude observationnelle longitudinale incluant plus de 2,2 millions de jeunes filles âgées de 13 à 16 ans entre 2008 à 2012. 14 maladies auto-immunes étaient sélectionnées. L’analyse des résultats n’a pas mis en évidence d’augmentation significative du risque de survenue d’une MAI (toutes MAIs confondues) chez les jeunes filles vaccinées, comparativement aux non vaccinées (Hazard ratio ajusté, HRa : 1,07 [IC95% : 0,99-1,16]). Pour 12 des 14 événements d’intérêt étudiés, les analyses effectuées n’ont pas permis d’observer une association statistiquement significative entre les jeunes filles vaccinées et la survenue de ces pathologies.
-
Compte-tenu des données colligées et analysées durant plus de 9 années de suivi national de pharmacovigilance associées aux résultats définitifs rassurants de l’étude évaluant le risque d’affections auto-immunes post-vaccinales à partir de la base de données SNIIRAM de la CNAMTS, les membres du Comité technique de pharmacovigilance considèrent qu’aucun fait nouveau de sécurité n’a été mis en évidence pour ces vaccins.
-
Le Comité consultatif mondial pour la sécurité des vaccins de l’OMS (GACVS) n’a pas trouvé de nouvelles études confortant les résultats de l’étude française relatifs au syndrome de Guillain-Barré (SGB) : « une étude autocontrôlée de grande ampleur portant sur une série de cas a été menée au Royaume-Uni parmi une population à laquelle 10,4 millions de doses avaient été administrées. Cette étude n’a relevé aucune augmentation significative du risque de SGB après une dose vaccinale quelconque ».
-
De même, le SGB a été spécifiquement sélectionné en tant que critère de jugement dans des études effectuées aux États-Unis en utilisant le système Vaccine Adverse Events Reporting System (VAERS) et le Vaccine Safety Datalink (VSD). Il a été présenté au GACVS de nouvelles données émises par le VAERS suite à l’administration de 60 millions de doses et par VSD après l’administration de plus de 2,7 millions de doses jusqu’à fin 2015. Aucune association entre le vaccin anti-HPV et le SGB n’a été mise en évidence. Les études britanniques et américaines ont conclu, sur la base de leurs données respectives, qu’un risque supérieur à 1 cas par million de doses pouvait maintenant être exclu.
F) Vaccin contre la grippe

G) 2 mois pour les premiers vaccins c’est pas trop tôt ?
- Les maladies évitables par ces vaccinations peuvent être particulièrement graves, voire mortelles, chez le bébé et le jeune enfant < 2 ans.
- Les anticorps transmis par la mère durant la grossesse diminuent au fil des mois. Ces anticorps ne le protègeront donc pas suffisamment longtemps et pas contre de nombreuses maladies infectieuses. L’entourage du nourrisson, même apparemment non malade, peut lui transmettre des maladies.
- La vaccination renforce le système immunitaire encore fragile du jeune enfant et lui permet de se protéger contre ces maladies.
- L’allaitement maternel protège le nourrisson contre de nombreuses infections parce que le lait contient des protéines qui stimulent son système immunitaire mais l’allaitement ne suffit pas pour le protéger complètement.
- La vaccination de l’enfant permet de prendre le relais de la protection transmise par sa mère dès les premières semaines de la vie. Lorsqu’il grandira, l’enfant consolidera son propre système immunitaire au contact des différents microbes qu’il rencontrera. Mais en attendant, il faut que l’immunité du nourrisson et de l’enfant en bas âge soit renforcée par la vaccination pour une protection efficace
H) Il n’y a aucun intérêt à vacciner les enfants contre l’hépatite B
- Risque de chronicisation de 90% chez le nouveau-né infecté et de 30% chez l’enfant de moins de 5 ans. Plus la maladie est contractée jeune, plus le risque de passage à la chronicité est élevé et donc plus le risque de voir apparaître une cirrhose ou un cancer est important.
- De plus, l’enfant n’ayant pas de signe d’infection, le risque de transmission au sein du foyer ou des personnes proches est important.
- L’immunité dure plusieurs décennies, y compris quand l’enfant est vacciné très jeune. Cette vaccination protège très efficacement et est parfaitement sûre chez les nourrissons. Il s’agit d’une protection à long terme qui protègera les enfants vaccinés dans l’enfance lorsqu’ils seront exposés au risque d’acquisition de l’hépatite B à l’adolescence ou à l’âge adulte (rapports sexuels, voyages, collectivités…)
I) Se faire vacciner contre une maladie qui a presque disparu ne sert a rien
- La politique de vaccination pour une maladie peut être arrêtée quand celle-ci a été complètement éradiquée.
- Cette décision se fait à l’échelle mondiale (OMS) ; un exemple en est l’interruption de la vaccination antivariolique en 1980.
- En revanche, on parle de maladie quasi disparue tant que le virus continue de circuler dans le pays à cause de personnes non-vaccinées.
- Il y a alors un risque de retour de la maladie.
- Exemple de la rougeole qui avait quasi disparu en France. Or une couverture vaccinale insuffisante a provoqué une recrudescence des cas ces dernières années
J) Les maladies infantiles ne sont pas graves
"Les maladies ayant quasi disparu, les gens ne perçoivent plus les risques qu’elles représentent. Il y a urgence à rappeler l’utilité des vaccins auprès du grand public et à insister sur les bénéfices qu’ils apportent, qui sont bien plus importants que leurs effets secondaires"
Si des vaccins ont été mis en place pour ces maladies, c’est qu’elles peuvent être graves, voire mortelles :
- Exemple de la poliomyélite : 1 cas sur 200 : paralysie irréversible.
- Exemple de la rougeole : cette maladie n’est généralement pas grave chez le jeune enfant mais dans de rares cas, elle peut provoquer des complications importantes comme une pneumonie ou une encéphalite aiguë. Chez la femme enceinte, la rougeole augmente le risque de fausse couche et d’accouchement prématuré.
- Exemple de la rubéole congénitale et le syndrome fœtal polymalformatif.
K) Faire plusieurs vaccins en même temps est dangereux et surcharge le système immunitaire
- Les données scientifiques montrent que le fait d’administrer simultanément plusieurs vaccins n’a pas d’impact négatif sur le système immunitaire d’un enfant. Les enfants sont exposés chaque jour à des centaines de substances étrangères déclenchant des réactions immunitaires. Le fait de manger introduit de nouveaux antigènes dans l’organisme et le nez et la bouche abritent de nombreuses bactéries. Un rhume banal ou un simple mal de gorge expose les enfants à bien plus d’antigènes que les vaccins.
- L’administration simultanée de plusieurs vaccins a pour avantage essentiel de diminuer le nombre des consultations médicales, ce qui permet d’économiser du temps et de l’argent. Par ailleurs, lorsque l’association de vaccins est possible (comme pour la diphtérie, la coqueluche et le tétanos), on fait moins d’injections, ce qui réduit la gêne pour l’enfant. On peut prendre un certain nombre de mesures pour diminuer la douleur au moment de la vaccination.1
- Les nourrissons de 2 mois ont un système immunitaire immature permettant une meilleure réponse immunitaire aux vaccins. De plus, on vaccine à partir de 2 mois pour mieux protéger les nourrissons plus sujets aux infections du fait de ce même système immunitaire immature
L) Les vaccins confèrent-ils une meilleure immunité que les infections naturelles ?
- Les vaccins interagissent avec le système immunitaire pour produire une réaction similaire à celle induite par l’infection naturelle sans provoquer la maladie ou exposer le sujet vacciné au risque des complications potentielles. En revanche, le prix à payer pour être immunisé par l’infection naturelle peut se traduire par des troubles cognitifs avec Haemophilus influenzae type b (Hib), des anomalies congénitales avec la rubéole, le cancer du foie avec le virus de l’hépatite B ou la mort avec les complications de la rougeole.
Nouvelles données suite à l’obligation vaccinale de 2018
A) Des premiers effets positifs des obligations vaccinales sur la protection de la population et les couvertures vaccinales
- Santé publique France a comparé les couvertures vaccinales à 7 mois des nourrissons nés entre janvier et mai 2018, avec celles des nourrissons nés entre janvier et mai 2017.
- Le recueil des données a été fait sur la base du remboursement des vaccins hexavalents délivrés de janvier à mai 2018 pour ces enfants.
- Le nombre de doses remboursées a été comparé à celui des années précédentes chez les enfants de la même classe d’âge.
1) Globalement, les couvertures vaccinales ont connu une nette amélioration avec :
- +36,4 points de couverture vaccinale de la 1ère dose du vaccin contre le méningocoque C : 39,3% en 2017 à 75,7% en 2018.Cette amélioration a permis de diminuer le nombre des infections invasives dues à ce germe chez les nourrissons < 1 an.
- +5,5 points pour le vaccin hexavalent.93,1% en 2017 à 98,6% en 2018.
- +1,4 point de couverture vaccinale de la 1ère dose du vaccin contre le pneumocoque.98,0% en 2017 à 99,4% en 2018.1
2) Les couvertures vaccinales s’améliorent également chez les enfants non soumis à l’obligation :
- La couverture vaccinale de la 1ère dose du vaccin ROR chez les enfants ayant eu 12 mois en 2018 est de 87,2%, alors qu’elle était de 85,0% chez ceux ayant eu 12 mois en 2017 (+2,2 points).
- Chez les enfants âgés de 2 à 5 ans, dans le cadre du rattrapage de la vaccination contre le méningocoque C, la couverture vaccinale a également évolué de 70,8 % en 2017 à 72,2 % en 2018.
- La couverture vaccinale de la première dose du vaccin HPV (recommandé) chez les jeunes filles de 15 ans en 2018 est de 29,4%, alors qu’elle était de 26,2% chez les jeunes filles nées l’année précédente (+3,2 points).
- La couverture vaccinale contre le papillomavirus chez les jeunes filles reste très insuffisante en France en 2018. A l’âge de 16 ans seules 23,7% des jeunes filles nées en 2002 ont reçu un schéma complet de vaccination contre les infections à papillomavirus.
B) Des effets positifs sur la perception des vaccins
Les progrès se lisent aussi dans la perception de la vaccination.
Ainsi, selon une enquête de Santé publique France :
- 67% des parents déclarent être favorables à cette extension de 3 à 11 vaccinations, parmi lesquels, 10% – selon leur souvenir – ne l’étaient pas en décembre 2017.
- 91% se déclarent convaincus de l'importance de la vaccination pour la santé des enfants
- 87% des jeunes parents de déclarent convaincus de l’importance des vaccins pour la protection de la collectivité (+5 points par rapport à juin 2018).
Du côté des professions de santé, des enquêtes menées en février et mars 2019 auprès d'un échantillon de 758 généralistes et de 615 pédiatres montrent :
- Une proportion de 99% de professionnels favorables à la vaccination.
- Le passage à 11 vaccinations obligatoires, voulu par Agnès Buzyn, est perçu de façon positive par 75% des médecins généralistes et 96% des pédiatres.
- Ces derniers sont par ailleurs 77% à estimer que cette mesure a facilité leur relation avec les parents et 69% à penser qu'elle a diminué la réticence des parents vis-à-vis de la vaccination.
C) Des efforts de tous au nom de la santé publique française
- La mise en œuvre de l'extension de l'obligation vaccinale a mobilisé de nombreux acteurs, au premier rang desquels les professionnels de santé de proximité (médecins, pharmaciens, sage-femmes et infirmiers), mais également les agences sanitaires, les unions régionales de professionnels de santé (URPS) et les agences régionales de santé (ARS).
- Ces professionnels et ces structures se sont appuyés sur des relais d'information avec différents types de supports dématérialisés, d'affiches, de brochures ou avec la mise en pratique de cas concerts (questions-réponses). Des conférences débats ont été organisés localement sous l'égide des ARS. Les plateformes vaccination-info-service.fr et mesvaccins.net propose à toute personne de faire le point sur ses vaccinations (diagnostic personnalisé) en fonction de son profil santé ou de son contexte professionnel ou environnemental, permettant de sensibiliser les personnes au-delà des enfants concernés par l'obligation vaccinale.
- Pour amplifier ce mouvement favorable, Santé publique France a lancé, avec le ministère des Solidarités et de la Santé, une campagne d'information diffusée à la télévision en avril/mai 2019 sur le web et sur les réseaux sociaux, dans la presse et dans les lieux de santé. Elle visait plus spécialement les jeunes parents, même si d'autres tranches d'âge sont concernées par la vaccination (par exemple contre la grippe pour les personnes âgées ou fragilisées).
- À noter : outre les résultats nationaux, Santé publique France diffusait également sur son site des bulletins de santé publique reprenant ces mêmes résultats pour chacune des régions de métropole et d'outre-mer (sauf la Réunion et Mayotte).
D) Suivi de pharmacovigilance
- Pour accompagner l'extension de l'obligation vaccinale, l'ANSM a mis à disposition des professionnels de santé et du public une information régulièrement actualisée sur les données de tolérance des vaccins administrés chez les enfants de moins de 2 ans.
- Pour cela, l'ANSM a consulté un comité scientifique spécialisé temporaire (professionnels de santé dont professionnels de la vaccination, représentants d’associations de patients et de la société civile, sociologues) comprenant des auditions publiques pour définir les modalités et les indicateurs de suivi de cette pharmacovigilance.
- Un premier bilan a été publié par l’ANSM en juin 2019 sur la tolérance des vaccins suite à l’obligation vaccinale : Au total, aucun nouveau signal en terme de tolérance des vaccins n'a été mis en évidence chez les enfants âgés de moins de 2 ans durant la période de 2012-2017 précédant la mise en place de l'obligation vaccinale et celle du premier semestre 2018. A partir de ces premiers éléments, le profil de tolérance des vaccins est comparable pour ces deux périodes.
Résumé