Dermatite atopique

INTRODUCTION/GÉNÉRALITÉ
- Le terme de dermatite atopique (DA) désigne la pathologie inflammatoire cutanée chronique et/ou récidivante la plus fréquente (prévalence de 10-25 % chez les enfants et 5-8 % chez les adultes selon les pays) [1-3].
- La DA a un impact important sur la qualité de la vie des malades et de leurs familles.
- Ses répercussions socio-économiques sont significatives [4].
Physiopathologie
- La DA est une pathologie polygénique dans laquelle les produits de mutations génétiques interagissent avec des facteurs environnementaux. En raison des progrès constants dans la compréhension de ces mécanismes, les concepts physiopathologiques doivent être constamment adaptés. De plus, la complexité de l'aspect clinique reflète certainement un haut degré de complexité physiopathologique.
- On peut cependant résumer très schématiquement les grandes lignes des mécanismes tels qu'illustrés dans la figure ci-dessous. Le caractère chronologique de ce schéma est valable en premier lieu pour les enfants atteints de DA. En ce qui concerne les formes à début plus tardif, l'application de ce concept et de ses composantes reste encore à être démontrée.
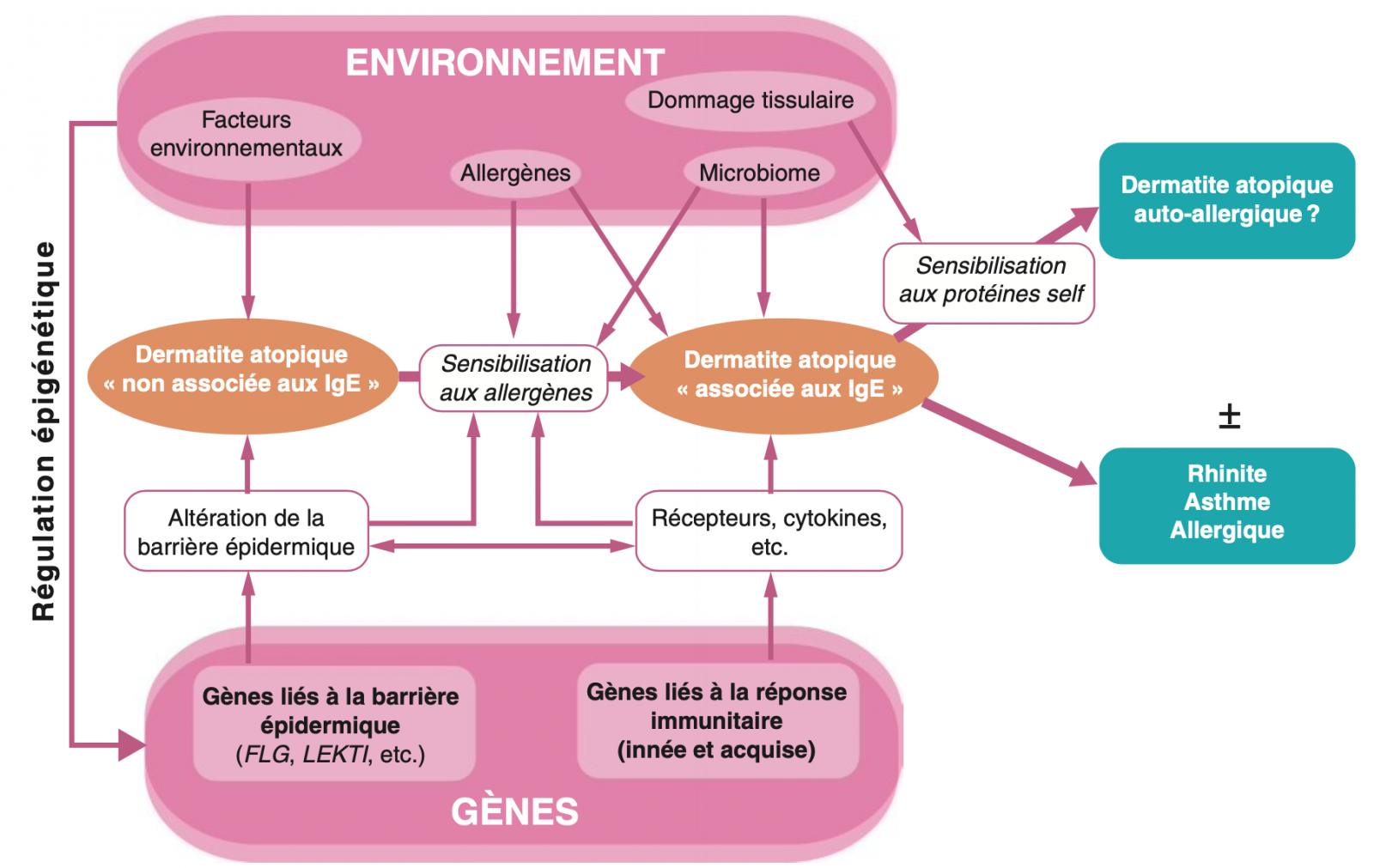
A) Génétique de la dermatite atopique
Les facteurs génétiques peuvent être classés en deux grandes familles de gènes :
- les gènes impliqués dans la structure et la régulation de la barrière épidermique;
- et ceux impliqués dans la régulation de la réponse immunitaire.
1) Gènes de la barrière épidermique
a) Filaggrine
- On a longtemps suspecté une certaine association entre l'ichtyose vulgaire et la dermatite atopique en raison de la xérose cutanée importante que l'on retrouve dans ces deux pathologies. Les études génétiques ont récemment confirmé cette association montrant que 30-50 % des sujets atteints de dermatite atopique dans la population européenne avaient une mutation du gène codant pour la filaggrine, responsable elle-même de cette forme particulière d'ichtyose la plus fréquente dans la population normale [18]. Il faut cependant signaler qu'au moins 10 % de la population européenne porte au moins un allèle avec une mutation de la filaggrine alors que 60 % des porteurs de cette mutation ne vont pas développer de dermatite atopique [19]. Cependant, il semble exister des différences dans la fréquence des localisations particulières de ces mutations entre les populations européennes et asiatiques par exemple [20].
- L'étude de ces séquençages complets du gène de la filaggrine dans ces différentes populations et leur signification fonctionnelle devraient apporter des informations plus précises concernant les types de mutation de la filaggrine dans les différentes populations.
- Dans la plupart des cas, une diminution de la synthèse de la filaggrine mène à une réduction de la production du Natural Moisturizing Factor (NMF) comme produit de dégradation de la filaggrine. Ce manque semble avoir de nombreuses conséquences physiologiques et physiopathologiques pour la fonction normale de la barrière épidermique.
b) Autres gènes
- Le gène classiquement rapporté dans la genèse du syndrome de Netherton, le gène codant pour l'antiprotéase de LEKTI, semble également un candidat de premier choix pour expliquer notamment les phénomènes initiaux de la dermatite atopique [21]. En effet, les variantes du gène LEKTI sembleraient induire une inflammation non spécifique au niveau cutané qui elle-même favorise le développement d'une réaction immunitaire du type Th2 et, en conséquence, une sensibilisation médiée par les IgE.
- De nombreux autres gènes impliqués dans la structure et la cohésion de l'épithélium épidermique ont été considérés récemment tels que les protéines des tight-junctions appelées Claudin-1 [22].
- On considère actuellement qu'il existe très certainement de nombreux autres gènes impliqués dans la fonction barrière épidermique qui pourraient être trouvés chez une proportion significative des malades atteints de dermatite atopique aussi bien dans les populations européennes que dans les populations asiatiques ou d'autres continents.
2) Gènes de la réponse immunitaire
De nombreuses études génétiques ont montré une association avec des gènes impliqués dans la régulation de la réponse immunitaire. Ces gènes candidats incluent notamment ceux codant pour l'interleukine 4, la chaîne alpha du récepteur de l'interleukine 4, l'interleukine 13, la chimiokine RANTES, de même que toute une série d'autres cytokines ou récepteurs impliqués dans la réponse immunitaire, dont l'association avec la DA doit être confirmée [23].
B) Facteurs environnementaux et microbiome
Pour la réalisation d'une maladie génétiquement complexe, le patrimoine génétique ne suffit en règle pas et il faut un ou plusieurs facteurs de provocation exogènes afin de déclencher la maladie.
- La DA est une maladie particulièrement sensible à des facteurs environnementaux tels que les produits appliqués directement sur la peau (savon, gel de douche, produit de soin quotidien), l'exposition aux allergènes alimentaires et aux aéroallergènes comme les allergènes de poussière de maison, les pollens ou les allergènes du monde animal.
- L'influence bénéfique des rayons ultraviolets est très souvent rapportée par les malades.
- Les infections microbiennes dues au staphylocoque doré sont particulièrement à l'origine de poussées sévères chez l'enfant. Cependant, on commence à peine à comprendre le rôle majeur de la composition du microbiome cutané et notamment des bactéries commensales pour l'établissement et la restauration d'une peau saine [24, 25]. Bien que classifié comme facteur environnemental, le microbiome cutané peut être considéré comme un second génome dont la croissance des éléments pathogènes tel que le staphylocoque doré semble pouvoir être à l'origine des poussées inflammatoires [26]. D'autre part, le traumatisme engendré par le grattage en réaction au prurit pourrait être à l'origine d'une accentuation de la réaction inflammatoire.
- Le dommage cellulaire occasionné par le grattage pourrait libérer des structures intracellulaires contre lesquelles le système immunitaire développera des IgE spécifiques [27].
- Finalement, il faudra aussi considérer l'impact possible des facteurs environnementaux tels que les aliments, les rayons ultraviolets, les xénobiotiques ou autres facteurs exogènes potentiellement capables d'influencer l'expression du patrimoine génétique par le truchement de mécanisme de régulation épigénétique [28].
C) Réponse immunitaire et sensibilisation médiée par les IgE
1) Phénomènes de sensibilisation
a) Dominance immunologique de la réponse du type Th2
- Du fait de son appartenance à la diathèse atopique, la DA a toujours été considérée comme une pathologie particulière dans laquelle une dominance immunologique de la réponse du type Th2 semble être essentielle dans le déclenchement et l'entretien de la réaction inflammatoire [29].
- Un autre dogme important de l'immunologie stipule qu'une réaction immunologique spécifique implique trois acteurs essentiels : des cellules présentatrices de l'antigène, un antigène ou un allergène et des cellules lymphocytaires T spécifiques pour les peptides issus de cet allergène/antigène. Dans ce scénario, les cytokines du type Th2 telles que l'IL-4 et l'IL-13 ont donc un rôle essentiel à jouer dans la régulation de la synthèse des IgE.
- De plus, les lymphocytes du type Th2, produisant de l'IL-13, semblent également responsables du phénomène de prurit occasionné par cette cytokine tout à fait particulière.
b) Réaction inflammatoire dans la peau apparemment normale
- En ce qui concerne l'infiltrat lymphocytaire présent dans les lésions de DA, les techniques d'analyse du transcriptome cutané ont d'une part confirmé la présence de cellules Th2 mais aussi des cellules du type Th22 ainsi que de cellules lymphocytaires innées du type 2. Il faut également noter que ces investigations ont confirmé la présence d'une réaction inflammatoire invisible dans la peau apparemment normale à distance des lésions de DA [30].
- Ces observations étayent le concept selon lequel l'inflammation cutanée dans la DA n'est pas limitée aux lésions visibles mais implique de plus grandes surfaces, avec un impact systémique très probable sur l'ensemble de la réponse immunitaire [31]. Ceci explique aussi une certaine corrélation entre l'importance et la chronicité des lésions dermatologiques d'une part, et l'apparition ainsi que l'extension du profil de sensibilisation IgE observée dans la phase chronique de la maladie notamment chez les enfants d'autre part.
2) Rôle des allergies
a) Atopènes
- Les antigènes susceptibles de déclencher une hypersensibilité aux IgE sont suffisamment spécifiques du phénomène atopique pour être dénommés atopènes. Ils varient cependant selon les conditions socio-culturelles et d'environnement des populations étudiées. Ainsi, le riz est un atopène au Japon et le pollen de bouleau l'est en Scandinavie.
- Cependant, certains atopènes sont ubiquitaires dans les zones tempérées, comme l'allergène majeur de l'acarien domestique (Dermatophagoides pteronyssinus).
b) Pénétration des atopènes
- Elle est possible à travers la peau et les muqueuses, malgré un poids moléculaire élevé, en raison de la perméabilité accrue de la barrière épidermique et d'une activité protéasique intrinsèque de certains allergènes [32, 33]. La peau est facilement pénétrée en raison de prédispositions génétiques et un lien de causalité existe par ce biais entre l'atteinte cutanée et les atteintes muqueuses – asthme et rhinite.
- En fonction de la voie de pénétration, on distingue les aéroallergènes qui peuvent être inhalés ou agir au contact de la peau, et les trophallergènes ingérés, des réactions croisées pouvant survenir entre des atopènes inhalés et ingérés (p. ex. pollen de bouleau et pomme).
3) Prévalence de la sensibilisation aux atopènes
- Dans une population déterminée, les sensibilisations aux atopènes ont une prévalence variable selon l'âge, qui tient sommairement compte du mode, de la chronologie et de la fréquence d'exposition : les trophallergènes sont les plus prévalents chez le nourrisson, puis les aéroallergènes deviennent majoritaires chez l'enfant et l'adulte.
4) Sensibilisation ou allergie cliniquement pertinente ?
Il convient de distinguer la sensibilisation, de l'allergie cliniquement pertinente.
a) Prick-tests et une recherche des IgE spécifiques
- Une sensibilisation est mise en évidence par un prick-test ou une recherche des IgE spécifiques pour un ou plusieurs allergènes.
- Cette sensibilisation n'entraîne pas toujours un phénomène d'allergie cliniquement détectable en raison des phénomènes de tolérance apparaissant au fil du temps et qui semblent être médiées par des IgG4 spécifiques.
- Ceci est bien connu pour certains allergènes alimentaires mais n'est pas la règle pour tous tels que les arachides par exemple.
b) Atopy patch-tests
- Les patch-tests utilisant les aéroallergènes ou les trophallergènes semblent aspécifiques pour détecter les allergènes responsables des poussées de la DA [34-36].
- Malheureusement, ces atopy patch-tests n'ont pas encore été standardisés et ne font donc pas l'objet d'examens de routine dans les cabinets dermatologiques.
c) Auto-immunité à IgE
- L'apparition d'anticorps IgE dirigés contre les structures épi- dermiques intracellulaires suggère qu'une certaine forme d'auto-immunité pourrait jouer un rôle dans la phase chronique de la maladie [37].
Histologie
- Le mot dermatite est commode pour regrouper des aspects sémiologiques divers, mais qui ont un trait histopathologique commun [12]. Il est rare cependant, compte tenu de la spécificité de la combinaison des critères sémiologiques et anamnestiques, d'avoir à pratiquer une biopsie pour diagnostiquer une DA. Ce geste a plutôt pour but d'éliminer une autre affection telle qu'un lymphome cutané dans les formes de DA tardives.
- L'aspect histologique comporte une atteinte épidermique prédominante avec un afflux de lymphocytes T (exocytose) qui s'accompagne d'un œdème intercellulaire (spongiose) dans les poussées aiguës réalisant des vésicules microscopiques. Ces vésicules sont exceptionnellement visibles macroscopiquement et c'est leur rupture à la surface de la peau qui détermine le caractère suintant et croûteux des lésions, et constitue un excellent milieu de culture pour les contaminants bactériens. Du fait du grattage, l'épiderme s'épaissit (acanthose), donnant lieu cliniquement au phénomène de lichénification et devient, chez l'enfant et l'adulte, moins susceptible à un suintement issu de vésicules microscopiques. Dans ce cas, les excoriations peuvent cependant déterminer des brèches épidermiques et une exsudation secondaire.
- Le derme superficiel comporte un infiltrat mononucléé périvasculaire. La dilatation des capillaires superficiels est responsable de l'érythème et l'extravasation de protéines plasmatiques de l'œdème cutané (papules œdémateuses). De façon plus caractéristique dans la DA que dans des eczémas de contact, des éosinophiles dégranulés sont objectivables mais uniquement par immunohistochimie (présence de la major basic protein).
ÉPIDÉMIOLOGIE
Votre texte ici
FACTEURS DE RISQUES
Votre texte ici
EXAMEN CLINIQUE
Le phénotype cutané de la DA, bien que très hétérogène, est cepen- dant typique dans la plupart des cas et facilement identifiable [2].
A) Dermatite atopique du nourrisson
1) Aspect clinique
- La DA commence communément dans les premiers mois de vie, généralement entre la 6e et la 12e semaine mais parfois dès le 1er mois.
- Durant ces premières semaines, la plupart des enfants présentent une atteinte initialement «séborrhéique», comportant des squames tenaces du cuir chevelu souvent jaunâtres et grasses. La xérose cuta- née n'est pas toujours cliniquement perceptible et au premier plan.
- Les premières lésions inflammatoires se manifestent sur les joues avec un respect caractéristique de la partie médiane, en particulier la pointe du nez (fig. 5.19). Par la suite, on observe des lésions symétriques sur les convexités des membres. Sur le tronc, les lésions s'arrêtent généralement à la zone protégée par les couches-culottes, suggérant un facteur de protection sur l'expression de la maladie. L'atteinte des plis est parfois notée dès cet âge.
- Dans la 2e année, la xérose devient plus visible et constante. L'aspect des lésions est variable selon la gravité de la DA et le moment de l'examen (poussées ou rémissions). Les lésions aiguës sont suintantes puis croûteuses, et souvent impétiginisées. Elles sont mal limitées dans la plupart des cas. Cependant, les lésions plus chroniques peuvent prendre un aspect nummulaire (bien limité en pièce de monnaie) au tronc chez le nourrisson, et touchent sou- vent le mamelon et le dos mais aussi les convexités des mains et des pieds. Des aspects figurés, comportant des éléments circinés à guérison centrale, s'observent plus rarement. Dans les formes mineures, les lésions sont peu inflammatoires et palpables sous forme de rugosité cutanée des convexités.
- Les éléments de description les plus utiles pour établir un score lésionnel d'intensité chez le nourrisson sont : l'érythème, l'œdème (papules œdémateuses), les excoriations qui témoignent objective- ment du prurit, et le suintement associé aux croûtes qui témoigne de l'acuité des poussées vésiculeuses. Le prurit est souvent net et responsable de troubles du sommeil dès les premiers mois. Le grat- tage manuel est généralement précédé de mouvements équivalents dès le 2e mois (frottement des joues contre les draps et les vête- ments, agitation et trémoussement des membres et du tronc). Les lichénifications ne commencent à apparaître que dans l'enfance, mais parfois plus tôt dans la 2e année chez les enfants noirs ou asiatiques.
2) Diagnostic différentiel
- Il inclut la gale et l'acropustulose infantile, l'histiocytose langerhansienne, la dermatite séborrhéique et le psoriasis, des dermatoses transitoires comme les éruptions sudorales, certains prurigos ectoparasitaires, le syndrome de Gianotti-Crosti à forme papulovésiculeuse, la kératose pilaire, la dermatite de friction, et l'érythème périflexural asymétrique de l'enfant dans les formes d'évolution prolongée.
- Un examen physique complet incluant l'inspection des muqueuses, la palpation des aires ganglionnaires, la palpation abdominale et l'auscultation pulmonaire est impératif pour ne pas porter par excès un diagnostic de DA devant toute dermatose «eczématiforme».
- La notion de chronicité et d'évolution à rechute est importante pour le diagnostic : les formes débutantes sont d'interprétation difficile. En cas de doute, une biopsie sera effectuée en particulier pour éliminer une histiocytose langerhansienne, affection rare mais souvent diagnostiquée avec retard malgré des lésions cutanées spécifiques.
- En cas de point d'appel supplémentaire : infections cutanées et/ou profondes répétées, anomalie de la croissance, purpura, fièvre inexpliquée, des examens complémentaires immunologiques seront nécessaires à la recherche d'une DA ou d'un tableau eczématiforme révélateur d'un syndrome génétique impliquant surtout le système immunitaire ou la barrière cutanée (encadré 5.4). Le gène du syndrome de Wiskott-Aldrich a été cloné et son produit, WASp, intervient dans la motilité, la polarisation et la prolifération de lymphocytes T et des plaquettes. Les mutations de SPINK5 qui causent à l'état homozygote le syndrome de Netherton ont été associées à l'état hétérozygote à la dermatite atopique. Des manifestations eczématiformes ont été décrites au cours d'autres déficits immunitaires primaires (cf. chapitre 19-8).
B) Dermatite atopique de l'enfant (après 2 ans)
Au-delà de 2 ans, quand il coexiste avec la dermatite atopique, l'asthme patent (ou les équivalents asthmatiques, sous forme de toux sèche nocturne, gêne respiratoire avec sifflement expiratoire – wheezing – au froid, à l'effort, au rire ou lors d'épisodes infectieux ORL ou respi- ratoires) devient souvent plus gênant pour l'enfant que l'eczéma.
1) Aspect clinique
- Les lésions cutanées d'eczéma sont volontiers plus localisées aux plis (cou, coudes, genoux), ou comportent des «zones bas- tion» (mains et poignets, chevilles, mamelon, rhagades sous-auriculaires). Elles subsistent de façon chronique et, parfois, isolée (fig. 5.20). Des poussées saisonnières sont notées le plus souvent en automne et en hiver. Certains enfants restent handicapés par des poussées plus généralisées qui peuvent revêtir un aspect de prurigo aux membres.
- Dans les formes graves, une atteinte inversée pour l'âge peut encore toucher les faces d'extension des membres en particulier aux coudes et aux genoux. La lichénification prédomine sur l'érythème et l'œdème.
- Les signes mineurs comme la pigmentation infraorbitaire, les plis sous-palpébraux (signe de Dennie-Morgan) sont plus nets (fig. 5.21).
- La sécheresse cutanée (xérose) est un élément plus constant que chez le nourrisson et pose fréquemment le problème d'une ichtyose vulgaire transmise en dominance associée d'après les enquêtes génétiques dans 20 à 50 % des cas des séries européennes. Ce trait est fréquemment retrouvé chez un des parents, associant parfois une kératose pilaire (aspect râpeux noté sur la face externe des bras et des cuisses), un état squameux en petites écailles des jambes, et des paumes sèches avec une accentuation des plis (hyperlinéarité palmaire). L'amélioration de cette xérose est constante en été et nécessite des soins émollients redoublés en hiver.
- Aux pieds, l'aspect de pulpite sèche et fissuraire est fréquent chez l'enfant et, parfois, isolé. Au visage et sur les faces d'extension des bras, mais aussi parfois de façon plus diffuse, des eczématides sèches achromiantes (pityriasis alba) constituent un motif de consultation esthétique, en particulier après l'été en raison du contraste pigmentaire transitoire. De façon plus fréquente chez l'enfant noir, l'accentuation folliculaire des lésions est marquée en particulier au tronc (dermatite atopique folliculaire ou eczéma périfolliculaire).
- D'autres éléments sémiologiques traduisent des altérations fonctionnelles du tégument : pâleur faciale, dermographisme blanc (fig. 5.22) (raie blanche de vasoconstriction après grattage), crises de sudation labiles.
2) Diagnostic différentiel
- Il est d'autant plus restreint que la notion de chronicité avec évolution à rechutes est bien établie. Outre la difficulté déjà notée de distinguer une xérose associée à la DA d'une ichtyose vulgaire dominante, les formes localisées ou mineures soulèvent la question de leur rattachement à la DA : dermatite périorale, dermatite plantaire juvénile, dysidrose, chéilite, vulvite, eczéma pénoscrotal.
- Le diagnostic d'eczéma de contact et, parfois, de psoriasis doit être évoqué et les tests allergologiques de contact, éventuellement la biopsie, sont utiles pour faire progresser l'enquête diagnostique. La possibilité d'une intrication avec une autre dermatose doit être soulevée dans certains cas : psoriasis concomitant ou consécutif chez plus de 16 % des patients [6], lichen plan sous forme d'une poussée prurigineuse inhabituelle à différencier d'une lichénification banale, véritable vitiligo qui peut épouser les zones de topographie de la DA.
C) Dermatite atopique chez l'adolescent et l'adulte
- Après une période de rémission, la DA peut manifester une période de recrudescence à l'adolescence, souvent à l'occasion de conflits psychoaffectifs ou de stress.
- La DA peut aussi débuter de novo à cet âge ou à l'âge adulte. Hormis la xérose qui sera toujours retrouvée, les lésions inflammatoires seront situées typiquement à la face et au cou (head and neck dermatitis souvent associée à une sensibilisation aux levures du genre Malassezia) ainsi que dans les plis de flexion des coudes et genoux avec aspect de lichénification dominant. Une dermatite atopique affectant les mains est très fréquemment retrouvée. Des aspects nummulaires accompagnés de prurit intense peuvent coexister et présentent fréquemment des poussées saisonnières (printemps et automne).
- Ce début tardif à l'âge adulte, particulièrement chez les patients âgés de plus de 60 ans, doit faire effectuer des examens complémentaires et une biopsie avec étude en immunofluorescence directe, pour éliminer une autre affection notamment un lymphome cutané, une dermatite herpétiforme, une phase initiale d'une pemphigoïde bulleuse, voire un syndrome paranéoplasique.
- Une gale, un eczéma de contact ou une réaction à des allergènes ingérés comme le nickel doivent être exclus cliniquement.
- Parmi les aspects symptomatiques, les formes graves peuvent se manifester à l'extrême sous un aspect érythrodermique, ou plus communément sous forme de prurigo lichénifié (type Besnier) prédominant aux membres.
EXAMENS COMPLÉMENTAIRES
Votre texte ici
DIAGNOSTICS DIFFÉRENTIELS
Votre texte ici
ÉTIOLOGIE
Votre texte ici
COMPLICATIONS
A) Infections
Dans toutes les périodes d'activité de la maladie, les surinfections bactériennes (impétiginisation) seront plus fréquentes chez les enfants et les complications virales chez les adultes. Curieusement, les complications fongiques sont plus rares.
- Le staphylocoque doré colonise habituellement la peau de l'atopique aussi bien en peau lésée qu'en zones cliniquement non inflammatoires. On ne sait pas si la colonisation staphylococcique précède ou suit l'apparition de l'eczéma mais elle a un retentissement sur l'entretien de la réaction inflammatoire par des mécanismes immunologiques et non immunologiques. Elle semble secondaire à l'anomalie génétique de la barrière épidermique chez l'atopique accompagnée d'un déficit de la défense immunitaire innée et acquise. En effet, le traitement dermocorticoïde seul permet de diminuer la colonisation staphylococcique [38]. Il a été montré que, contrairement au psoriasis, la production en peau lésée de certains peptides antimicrobiens, actifs contre le staphylocoque doré, était diminuée [39]. Le seuil d'impétiginisation clinique est difficile à apprécier en particulier dans les formes aiguës exsudatives. La présence de lésions vésiculobulleuses inhabituelles fera évoquer le diagnostic de surinfection et prescrire un traitement antiseptique pour éviter une infection systémique. Des complications bactériennes sous-cutanées (ostéomyélites des phalanges distales, bursites olécrâniennes et prétibiales) ont été décrites à titre exceptionnel.
- L'herpès (HSV-1 essentiellement) est responsable de poussées aiguës parfois dramatiques nécessitant une hospitalisation. Un déficit en production de cathélicidine et une prédisposition génétique sont en cause [40]. Une modification rapide de l'aspect des lésions et/ou la présence de vésiculopustules varioliformes, en association avec de la fièvre, doivent suggérer cette complication et faire mettre en œuvre un traitement antiviral en urgence, pour éviter un tableau de pustulose varioliforme de Kaposi- Juliusberg (fig. 5.23). Cette complication était autrefois décrite lors de la vaccination antivariolique, et est actuellement d'étiologie herpétique quasi exclusive. Ce tableau peut compliquer une primo- infection typiquement associée à une gingivostomatite, ou bien un herpès récurrent. Des infections herpétiques torpides sur placards lichénifiés ont été signalées.
- La varicelle n'a pas de gravité particulière, contrairement à certaines idées reçues.
- Le molluscum contagiosum est fréquemment disséminé chez l'enfant atteint de DA. Typiquement, il y a une prépondérance sur les lésions de DA témoignant du rôle de l'auto-inoculation par grattage.
- Les verrues vulgaires ne semblent pas être plus fréquentes chez les atopiques.
- Les infections fongiques sont rarement impliquées dans les surinfections cutanées chez l'enfant. Il a été signalé à titre exceptionnel des dermatophyties rebelles chez l'adulte atopique (syndrome de Jones).
B) Autres complications
1) Retard de croissance.
- Il peut être associé dans les DA sévères. Il impose une surveillance de routine des paramètres auxologiques chez ces enfants. Compte tenu de la prévalence de la DA, il est nécessaire d'éliminer les causes habituelles de retard staturopondéral avant d'attribuer les anomalies à la DA (retard de croissance intra-utérin, déficit en hormone de croissance, maladie cœliaque, mucoviscidose, etc.). Il faut se méfier des faux positifs des tests de dépistage de mucoviscidose chez le nourrisson atopique [41]. Les retards de croissance sans étiologie commune retrouvée se corrigent souvent de façon spectaculaire quand la DA est traitée efficacement, ce qui est en faveur d'un rôle majeur des troubles du sommeil. Le rôle des dermocorticoïdes dans le retard de croissance n'est en revanche pas établi.
2) Complications ophtalmologiques.
- La kératoconjonctivite allergique est la plus fréquente ; elle peut être aggravée par le port de lentilles de contact, et nécessite une prise en charge spécialisée. Le kératocône, la cataracte et le détachement rétinien sont beaucoup plus rares et connus dans le contexte de l'atopie et plus particulièrement dans les formes sévères de DA dans certaines populations asiatiques. Le rôle des corticoïdes locaux ou systémiques dans la cataracte atopique est controversé.
3) Eczémas de contact.
- À l'inverse du dogme fréquemment propagé, compte tenu du déficit de la barrière épidermique, de l'inflammation latente et de l'importance des soins locaux dans cette affection, il existe un risque important de sensibilisation de contact au long cours contre des haptènes particuliers chez les sujets atopiques [42, 43]. L'eczéma de contact allergique doit donc faire partie du diagnostic différentiel dans certaines poussées atypiques. Il est par conséquent nécessaire d'évoquer cette hypothèse et de tester les patients qui répondent mal aux traitements anti-inflammatoires topiques. Ces données obligent à adopter une attitude préventive dans l'utilisation des topiques potentiellement à risque (conservateurs, parfums, néomycine, etc.), et des métaux, nickel en particulier (percement d'oreilles, bijoux de fantaisie, piercing chez l'adolescent). Par ailleurs, l'orientation professionnelle doit tenir compte de ce paramètre pour éviter les eczémas des mains en particulier.
PRISE EN CHARGE THÉRAPEUTIQUE
Votre texte ici
ÉVOLUTION/PRONOSTIC
Votre texte ici
PRÉVENTION
Votre texte ici
SURVEILLANCE
Votre texte ici
CAS PARTICULIERS
Votre texte ici
THÉRAPIES FUTURES
Votre texte ici
