Hépatoblastome

INTRODUCTION/GÉNÉRALITÉ
- L'hépatoblastome (HB) est la tumeur hépatique maligne pédiatrique la plus fréquente même si elle ne représente que 2 % de l'ensemble des tumeurs malignes de l'enfant.
- L'histoire clinique, l'existence de facteurs de risque (prématurité, tabagisme maternel), le taux sérique de l'alphafœtoprotéine rapporté à l'âge et l'aspect radiologique sont des éléments importants du diagnostic.
HISTORIQUE
Votre texte ici
PHYSIOPATHOLOGIE
Votre texte ici
ÉPIDÉMIOLOGIE
- Son incidence est en voie d'augmentation.1
- Il atteint surtout l'enfant de moins de 3 ans.
FACTEURS DE RISQUES
Votre texte ici
EXAMEN CLINIQUE
- Augmentation du volume de l'abdomen avec hépatomégalie ou tumeur palpable ± troubles du transit.
- Syndrome abdominal aigu par rupture tumorale ou hémorragie intra-abdominale.
- Le diagnostic est rarement évoqué devant une pseudo-puberté précoce (sécrétion anormale d'HCG) ou une ostéoporose généralisée fracturaire.
- La fièvre, des douleurs, un ictère, une altération de l'état général sont plus volontiers décrits dans les carcinomes hépatocellulaires.
EXAMENS COMPLÉMENTAIRES
A) Biologie
- Alphafœtoprotéine sérique à interpréter en fonction de l'âge, sensible mais peu spécifique. Augmente en cas de régénération de tissu hépatique quelle que soit la cause. Si la sécrétion est tumorale, le taux sérique médian est augmenté dans 90 % des cas, à un seuil supérieur à 1,1 × 104 ng/mL. L'évolution du taux d'AFP est un facteur pronostique important ; une décroissance précoce supérieure à 1 log durant la phase de traitement préopératoire est un indicateur de survie sans évènement.
- Bilan hépatique (ASAT [aspartate-aminotransférase], ALAT [alanine-amino- transférase], γGT [gamma-glutamyl-transférase], bilirubine) : normal.
- Thrombocytose supérieure à 500000/mL par hyperproduction de thrombo- poiëtine.
- Plus rarement, sécrétion de β-HCG.
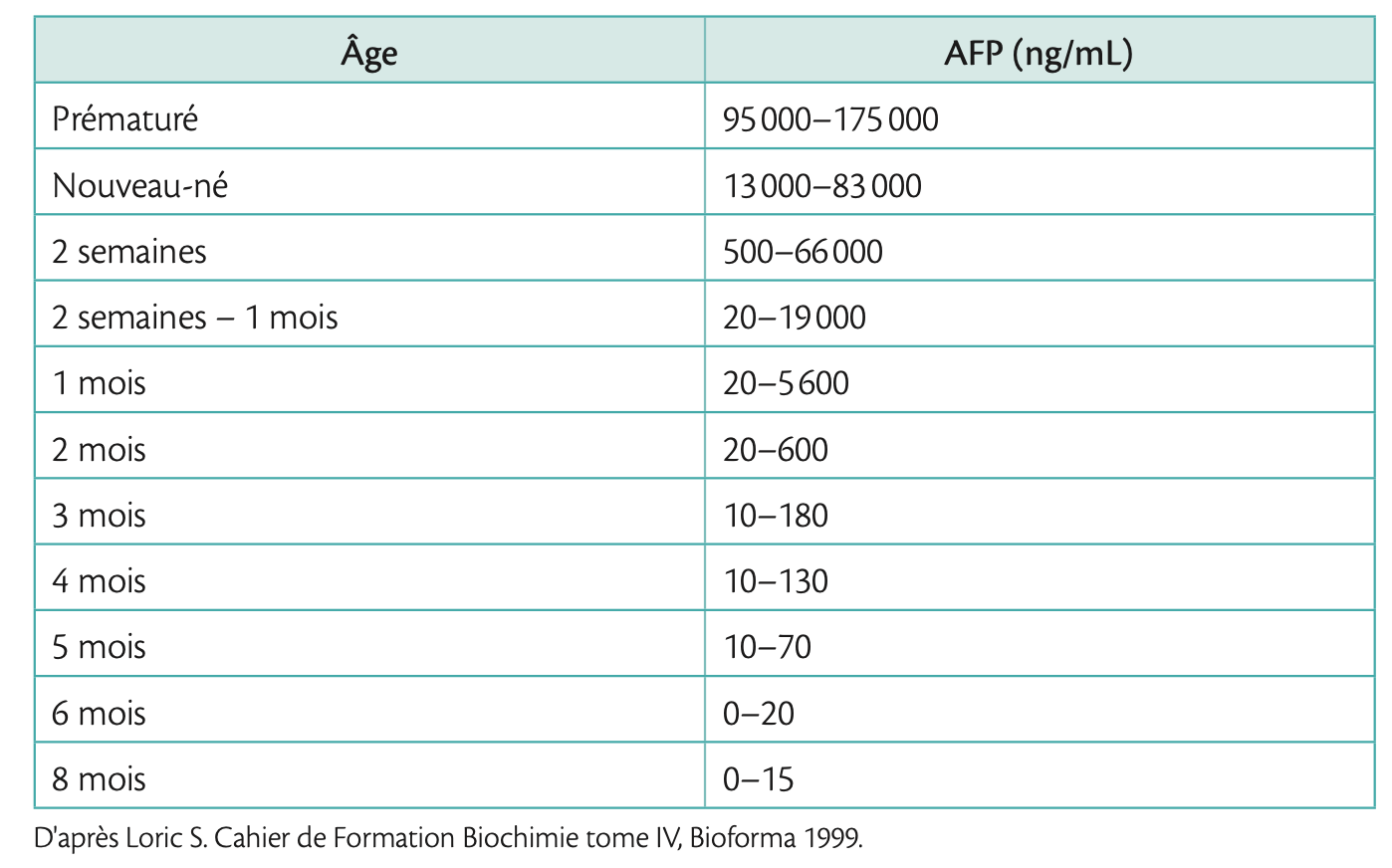
Concentrations sériques physiologiques de l'alphafœtoprotéine (AFP) en fonction de l'âge.
B) Imagerie
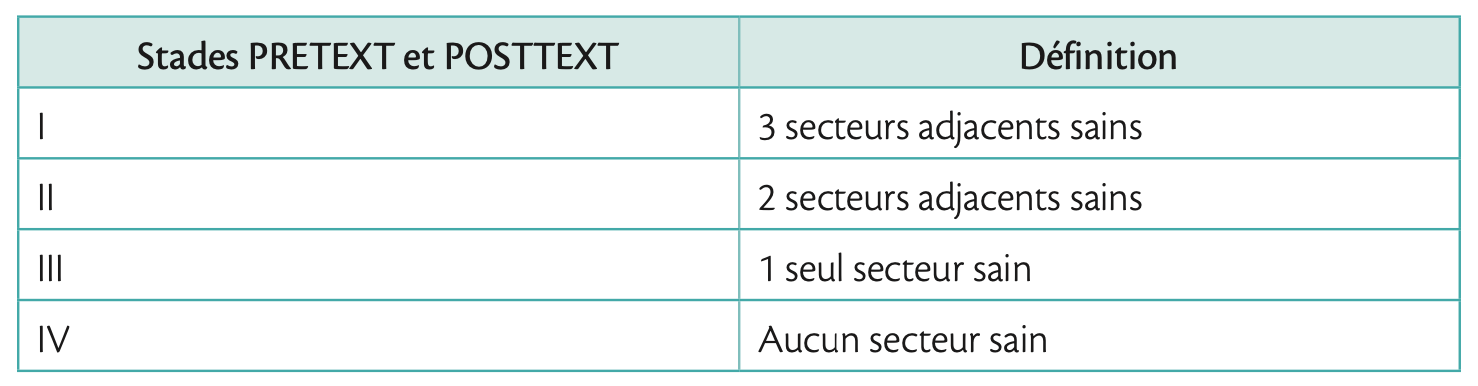
Système de classification préopératoire : l'un des objectifs du bilan radiologique initial (échographie + TDM ± IRM) est de classer la tumeur selon le stade «PRETEXT» soit Pre-Treatment Extent of Disease qui reflète l'extension de la tumeur dans le foie avant la chimiothérapie préopératoire. Il permet ainsi de juger de l'opérabilité et de rechercher des localisations métastatiques. Il est fortement conseillé de demander la relecture centralisée. Cette classification repose sur le nombre de secteurs atteints.
Il existe quatre secteurs qui regroupent chacun deux segments :
- le secteur latéral gauche (segments 2 et 3) ;
- le secteur médian gauche (segments 4a et 4b) ;
- le secteur antérieur droit (segments 5 et 8) ;
- et le secteur postérieur droit (segments 6 et 7).
Ce système individualise quatre groupes (I–IV) en fonction du nombre de sections hépatiques saines et décrit l'extension en dehors du foie avec les lettres suivantes :
- «V 1, 2, 3» en cas d'extension à la veine cave et/ou aux veines sus-hépatiques ;
- «P 1, 2» en cas d'extension au système porte ;
- «E 1, 2» en cas de maladie intra-abdominale extra-hépatique ;
- «C 1» en cas d'atteinte du lobe caudé (segment 1) ;
- et «M 1» en cas de métastases à distance.
Confirmation du diagnostic
- Biopsie hépatique à l'aiguille par méthode co-axiale (5 carottes mesurant chacune au moins 10 × 3 mm) en foie tumoral et en foie sain.1
- Analyse de la pièce opératoire.
DIAGNOSTICS DIFFÉRENTIELS
- Hamartome mésenchymateux de forme solide (en particulier chez l'enfant de moins d'un an avec possibilité de sécrétion d'AFP), tumeur vasculaire (héman- giome infantile, hémangioendothéliome épithélioïde ou angiosarcome), tumeur épithélio-stromale calcifiante en nids, sarcome indifférencié du foie ou carcinome hépatocellulaire de type fibrolamellaire (taux d'AFP normal) chez l'enfant de plus de 5 ans.
- Chez l'enfant plus âgé, en cas de taux sérique élevé d'AFP, discuter le diagnos- tic de carcinome hépatocellulaire (CHC) de type commun, de tumeur germinale maligne extragonadique (tumeur du sac vitellin) envahissant le foie et le péritoine ou de pancréatoblastome étendu au foie.
ÉTIOLOGIE
Votre texte ici
COMPLICATIONS
Votre texte ici
PRISE EN CHARGE THÉRAPEUTIQUE
A) Principes généraux de traitement
- Le traitement médical repose sur l'utilisation des sels de platine ± des anthracyclines, et est donc soumis à une surveillance étroite de l'ototoxicité et de la néphrotoxicité. Le traitement chirurgical doit être réalisé par une équipe spéciali- sée, éventuellement suprarégionale et programmé dès le diagnostic en vue d'une éventuelle transplantation.
B) Patients de risque standard
- Ce sont les patients avec une tumeur localisée (PRETEXT 1, 2 ou 3) sans autre facteur de risque.
- Les recommandations internationales sont issues du protocole SIOPEL 3 : 4 cycles préopératoires de cisplatine (CDDP) 80 mg/m2 sur 24 heures en monothérapie 1 suivis d'une résection chirurgicale, puis 2 cycles de chimiothérapie postopératoire.
- Les cycles sont réalisés tous les 15 jours avec une évaluation prévue tous les 2 cycles et un dosage d'AFP toutes les semaines.
- Dans ce groupe de patients, l'EFS à 3 ans est à 90 % et l'OS à 93 %.1
C) Patients de haut risque : PRETEXT IV sans métastases
- Ce groupe concerne toutes les tumeurs qui n'ont ni les critères de risque standard ni de très haut risque, soit, en pratique, les PRETEXT IV non métastatiques et les patients de 8 ans et plus sans métastase.
- Le traitement est plus intensif avec la séquence «superPlado» du protocole SIOPEL 3.1
- Dans ce groupe le but est d'obtenir les meilleures conditions pour une chirurgie de type R0 avec si besoin une transplantation. La chimiothérapie superPlado comporte du CDDP (80 mg/ m2 24 h) à J1, 29, 57, 85 préopératoire, puis à J15 postopératoire en alternance avec une association de carboplatine 500 mg/m2 sur 1 h – doxorubicine 60 mg/m2 sur 48 h à J15, 43, 71 préopératoire, puis à J1, 29 postopératoire.
- L'EFS à 3 ans est à 76 %.
D) Patients de très haut risque
- Ces patients métastatiques (en général aux poumons) ou avec un taux très bas d'AFP (< 100 ng/mL) sont aujourd'hui traités selon le protocole SIOPEL 4.
- Le traitement consiste en 3 cycles A1-A3 de chimiothérapie préopératoire comprenant du cisplatine 80 mg/m2/j en IV/24 h à J1, puis du cisplatine 70 mg/m2/j en IV/24 h à J8, 15, 29, 36, 43, 57 et 64, et de la doxorubicine 30 mg/m2/j IV/24 h à J8, 9, 36, 37, 57, et 58.
- Ce schéma est suivi d'une chirurgie d'exérèse y compris des métastases ou d'une transplantation si besoin, puis de la poursuite d'une chimiothérapie post- opératoire par un cycle C : doxorubicine 20 mg/m2/j IV/24 h à J1, 2, 22, 23, 43 et 44, et carboplatine visant une aire sous la courbe (AUC) de 6,6 mg/mL/min/j à J1, 22, et 43.
- Les patients qui ne peuvent pas être opérés après les cycles A peuvent recevoir le cycle B : doxorubicine 25 mg/m2/j IV/24 h à J1-3 et J22-24, et carboplatine AUC 10,6 mg/mL/min/j en IV/1 h à J 1 et J22).
- Avec ce protocole de traitement, l'EFS et la survie globale à 3 ans ont augmenté respectivement à 76 et 83 %.1
E) Prise en charge des rechutes
- Rechutes rares après l'obtention d'une rémission complète : 10 % des cas.
- Échecs liés à une progression sous traitement de 1re ligne en particulier pour les patients métastatiques ou inopérables.
- Délai moyen de rechute : 12 mois.
- Traitement : association possible de chimiothérapie et de chirurgie dans 42 % des cas. L'EFS et la survie globale à 3 ans sont de 34 et 43 % respectivement.1
ÉVOLUTION/PRONOSTIC
A) Facteurs de mauvais pronostic
- Taux d'AFP < 100 ng/mL.
- Âge ≥ 8 ans.
- Atteinte vasculaire (V3 ou P2).
- Envahissement extrahépatique.
- Forme métastatique, le plus souvent au poumon (lésion d'au moins 1 cm ou plusieurs dont au moins une est ≥ 5 mm).
- Histologie défavorable : SCU (petites cellules indifférenciées), tumeur rhabdoïde (prise en charge différente).
PRÉVENTION
Votre texte ici
SURVEILLANCE
Votre texte ici
CAS PARTICULIERS
Votre texte ici
THÉRAPIES FUTURES
- Thérapies ciblées envisagées grâce à l'identification de plusieurs voies de signalisation (WNT/bêtacaténine, NOTCH, de l'insulin growth factor 2), de l'activation de MYC et de différentes cascades de signalisation.
- De nouveaux traitements ou associations sont en cours d'évaluation, comme le sorafénib, (un inhibiteur multikinase, utilisé dans les carcinomes hépatocellulaires de l'adulte) ou les inhibiteurs de mTOR qui pourraient jouer un rôle dans le traitement des patients notamment après transplantation hépatique.
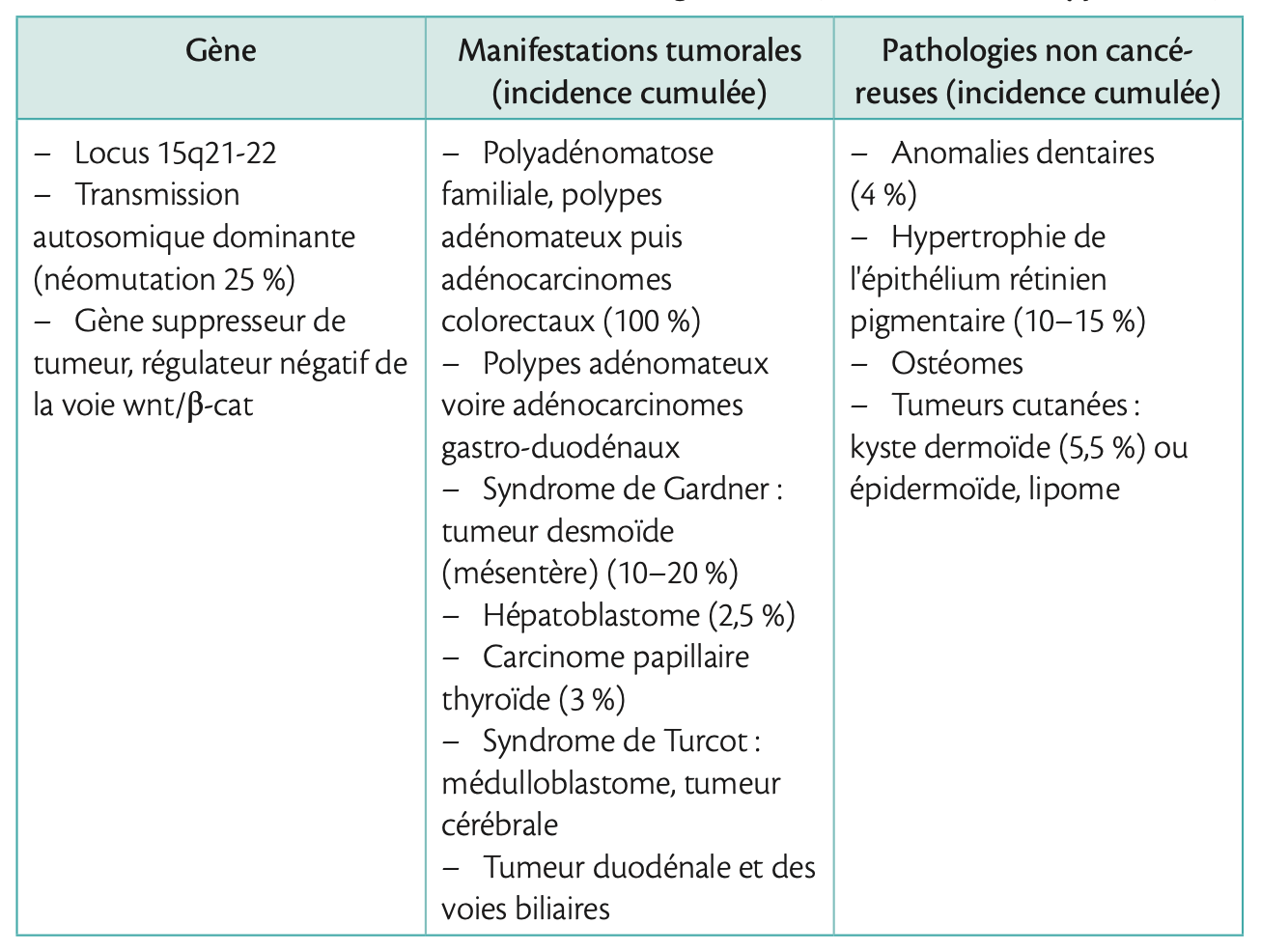
- L'association à une mutation du gène APC (tableau ci-dessous) dans 10 % des cas doit amener à une surveillance spécifique.
- La relecture radiologique par des experts nationaux et la prise en charge dans des centres chirurgicaux référents doit aussi permettre l'amélioration du pronostic de ces jeunes patients.