Ascite

INTRODUCTION/GÉNÉRALITÉ
- L’ascite est définie comme un épanchement liquidien libre dans la cavité péritonéale et non sanglant.
- L'examen clinique (incluant l'anamnèse), l'analyse du liquide d'ascite et l'échographie abdominale sont les 3 éléments sur lesquels s'appuie le diagnostic de la cause de l'ascite.
- L’ascite se manifeste le plus souvent par une augmentation du volume de l'abdomen associée à une prise de poids.
- La mise en évidence de liquide d'ascite par la ponction de la cavité abdominale est réalisée au lit du malade lorsque l'ascite est détectable cliniquement ou après un repérage échographique si elle est indétectable, et permet d'avoir un diagnostic formel.
- La cirrhose est la cause d’ascite la plus fréquente, responsable de près de 90 % des causes d’ascite (l'ascite est une complication fréquente de la cirrhose avancée et aussi un signe de gravité.).1
- Cependant, la présence d’une cirrhose n’est pas une condition exclusive et une ascite peut apparaître dans d’autres situations pathologiques dont le diagnostic et la stratégie thérapeutique sont moins bien codifiés.
- L’ascite peut apparaître au cours d'une maladie déjà connue pouvant se compliquer d'ascite ou être inaugurale de la maladie.
HISTORIQUE
Votre texte ici
PHYSIOPATHOLOGIE
A) situation normale :
-
Du liquide péritonéal est toujours présent bien qu’en très petite quantité, chez le sujet normal.
-
Il est principalement issu du liquide interstitiel hépatique, passant à travers la capsule du foie.
-
Le liquide interstitiel (et donc la lymphe) hépatique est riche en protéines car les capillaires sinusoïdes sont fenêtrés.
-
Les lymphatiques sous-péritonéaux, principalement dans les régions diaphragmatiques, ont pour fonction de drainer ce liquide physiologique
B) situation pathologique :
Trois mécanismes sont à l'origine de la formation de l’ascite : 1
- la rupture intrapéritonéale d’un conduit liquidien.
- une gêne à la résorption du liquide péritonéal.
- un excès de production du liquide péritonéal.
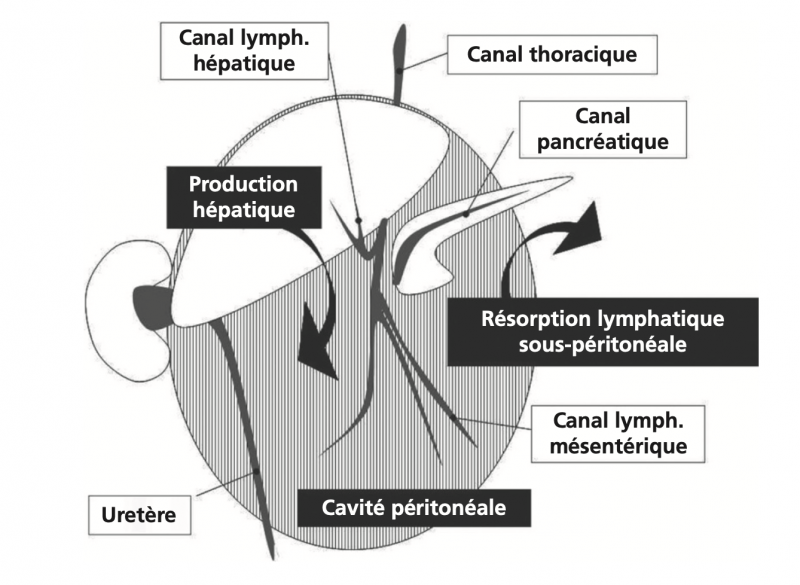
Conduits liquidiens dont la rupture peut causer une ascite.
1) rupture intrapéritonéale d'un conduit liquidien
Ce mécanisme ne rend compte que d'une minorité des ascites rencontrées en pratique. Dans ce cas, l'afflux de liquide est supérieur aux capacités de résorption péritonéale. La rupture peut porter sur un canal lymphatique mésentérique ou hépatique, un canal excréteur du pancréas, ou un uretère.
a) Rupture d’un canal lymphatique mésentérique
Ces canaux drainant la lymphe intestinale sont riches en chylomicrons (et donc en triglycérides) après un repas. Ils sont donc la source d’une ascite chyleuse, d’aspect lactescent (différent d’un aspect opalescent), dont le liquide est plus riche en triglycérides que le plasma. Les principaux mécanismes de rupture d’un canal lymphatique mésentérique sont :
- les traumatismes chirurgicaux (principalement lors de l’abord transpéritonéal de l’aorte ou du rein ou lors de la duodéno-pancréatectomie)
- l’hyperpression lymphatique résultant d’un obstacle sur la circulation lymphatique abdominale ou thoracique (lymphome, métastases ganglionnaires, radiothérapie abdominale, péritonite encapsulante, obstruction du canal thoracique, thrombose de la veine sous clavière gauche)
- la maladie de Waldenström qui induit une hyperviscosité de la lymphe.
-
la cirrhose (qui produit une augmentation du débit lymphatique mésentérique en raison de l'hypertension
portale)
- l’insuffisance cardiaque droite (qui augmente le débit lymphatique et diminue le drainage du canal thoracique en augmentant la pression veineuse centrale).
b) Rupture d’un canal lymphatique hépatique
- Elle résulte principalement d’une plaie chirurgicale d’un lymphatique du pédicule hépatique notamment lorsque, au départ, le débit lymphatique hépatique est augmenté par une insuffisance cardiaque droite ou une cirrhose.
- Le liquide d’ascite issu d’une brèche des canaux lymphatiques hépatiques est riche en protides (> 30 g/L) mais pas en chylomicrons.
c) Rupture d’un canal excréteur du pancréas
- Elle résulte d’une nécrose (après une pancréatite aiguë nécrosante) ou d’une hyperpression d’un canal pancréatique (au cours de la pancréatite chronique). Le liquide est riche en enzymes pancréatiques (lipase).
d) Rupture d’un uretère
Elle résulte d’un traumatisme de l’uretère (principalement chirurgical), ou d’une nécrose de sa paroi (après chirurgie sur la région ou par vascularite). Le liquide est plus riche en créatinine que le plasma.
2) Gêne à la résorption du liquide péritonéal.
Elle est la conséquence d'une obstruction des canaux lymphatiques sous-péritonéaux. Ce mécanisme rend compte d'une part importante des ascites rencontrées en clinique. Cette obstruction peut être secondaire à :
a) Une carcinose péritonéale (fréquente) :
- En cas d’ascite maligne, la physiopathologie de l’ascite est multifactorielle avec une augmentation de la perméabilité vasculaire et une obstruction du drainage lymphatique.1 Cette augmentation de la perméabilité capillaire est favorisée par certaines cytokines comme le VEGF.
- Les cancers de l'appareil digestif (à l'exception du carcinome hépatocellulaire) et le cancer de l'ovaire sont les principales causes de carcinose péritonéale.
- Un syndrome d'obstruction intestinale incomplète est fréquent et doit être cherché.
-
Le liquide d'ascite est souvent riche en protéines (> 25 g/L) et en cellules. Le taux de leucocytes peut être élevé (> 250/mm3).
-
L'examen cytologique montre inconstamment des cellules tumorales.
-
L'utilisation d'anticorps monoclonaux dirigés contre différents marqueurs tumoraux peut permettre de différencier des cellules cancéreuses et non cancéreuses.
-
Un épaississement localisé ou étendu du péritoine pariétal ou viscéral doit être cherché par les examens d'imagerie
b) Mésothéliome péritonéal (très rare, amiante) :
- C’est une cause très rare d’ascite.
- Le diagnostic doit être envisagé même en l’absence d’asbestose évidente.
- Le liquide d’ascite est souvent riche en protéines (> 25 g/L) et en cellules. Le taux de leucocytes peut être élevé (> 250/mm3).
- L’examen cytologique montre inconstamment des cellules tumorales.
- Un épaississement localisé ou étendu du péritoine pariétal doit être cherché par les examens d'imagerie de façon à en effectuer un prélèvement pour examen histologique.
c) Tuberculose péritonéale :
- L’ascite est une manifestation cardinale de la tuberculose péritonéale qui peut être associée à une tuberculose digestive ou d’un autre organe. En revanche, elle n’est que rarement associée à une tuberculose hépatique.
- Le liquide est riche en protide (> 25 g/L) et en leucocytes (> 1 000/mm3) avec lymphocytes > 70%. Toutefois, toutes ces caractéristiques peuvent manquer.
- La recherche de BK par l'examen direct est habituellement négative. La culture est rarement positive et le résultat exige d'attendre plusieurs semaines. Le dosage de l'enzyme adénosine-désaminase dans l'ascite peut s'avérer utile.
-
Le diagnostic est fait par la biopsie du péritoine sous cœlioscopie sur d'éventuelles granulations péritonéales avec mise en évidence de granulomes tuberculeux et mise en culture révélant du BK. La recherche de BK par une méthode PCR (Polymerase Chain Reaction) permet d'avoir un diagnostic plus rapide que la culture.
d) Lymphome péritonéal (très rare) ou une tumeur maligne du péritoine
3) excès de production du liquide péritonéal (contexte d'hyperhydratation extra-cellulaire)
Ce mécanisme rend compte de la plupart des ascites rencontrées en clinique. Il s'applique :
-
à la cirrhose (et au syndrome de Budd-Chiari) ;
-
à l'insuffisance cardiaque droite et à la péricardite constrictive
-
au syndrome néphrotique.
Un excès de production du liquide péritonéal ne survient que dans un contexte d'hyperhydratation extracellulaire, et donc de réabsorption rénale excessive de sodium et d'eau. C'est aussi pourquoi l'ascite est souvent (mais non constamment) associée à un œdème mou déclive (œdème des membres inférieurs chez le sujet ambulant, œdème des lombes chez le sujet alité).
Le liquide interstitiel en excès se localise :
-
soit de façon prédominante à la cavité péritonéale parce que la pression interstitielle y est sélectivement augmentée en raison d'une hypertension portale par bloc intrahépatique (cirrhose) ou sus-hépatique (syndrome de Budd-Chiari).
-
soit également dans la cavité péritonéale et dans l'ensemble du secteur interstitiel, parce que la pression interstitielle y est globalement augmentée en raison d'une élévation de la pression veineuse centrale transmise en amont au territoire portal (insuffisance cardiaque droite et péricardite constrictive), ou d'une diminution globale de pression oncotique plasmatique dans le cas du syndrome néphrotique.
Le mécanisme entraînant une réabsorption rénale excessive de sodium et d'eau est toujours une stimulation des baro et volorécepteurs assurant la régulation de la pression artérielle et du volume sanguin circulant. Cette stimulation induit :
-
l'activation excessive des systèmes vasoconstricteurs, antidiurétiques et antinatriurétiques,
entre autres :
-
système rénine-angiotensine-aldostérone,
-
système sympathique,
-
hormone antidiurétique (appelée aussi vasopressine);
-
-
l'inhibition des systèmes natriurétiques (entre autres, peptide natriurétique atrial) au cours de la cirrhose et du syndrome néphrotique, ou leur augmentation insuffisante au cours de l'insuffisance cardiaque.
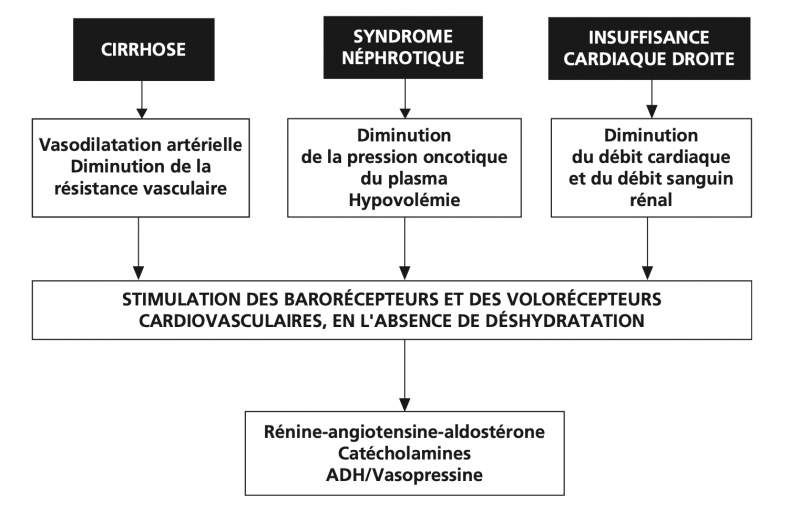
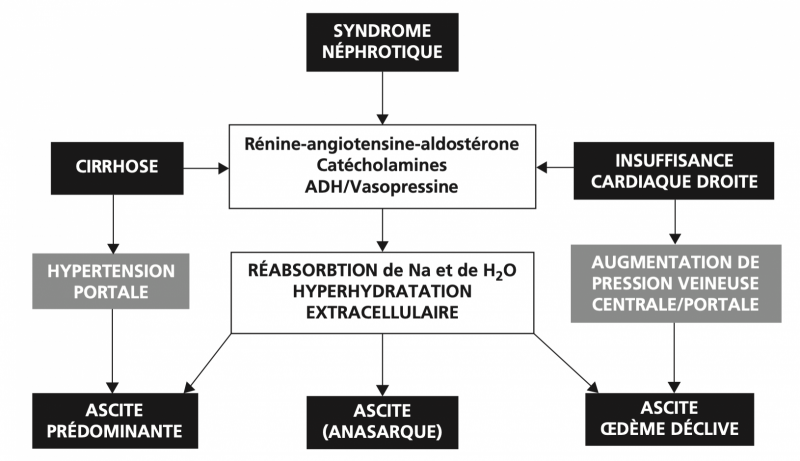
Les anomalies qui induisent l'hyperstimulation des baro et volorécepteurs diffèrent selon le contexte :
-
au cours de la cirrhose, il se produit une vasodilatation majeure des artérioles mésentériques. Il en résulte une diminution de la résistance vasculaire systémique et de la pression artérielle. Outre la réabsorption excessive de sodium et d'eau, la compensation inclut une augmentation du débit cardiaque.
-
au cours de l'insuffisance cardiaque droite, la diminution du débit cardiaque induit une baisse de la pression artérielle et une hypoperfusion rénale.
-
au cours du syndrome néphrotique, une diminution du volume circulant est induite par le passage de liquide vers le secteur interstitiel en raison de la baisse de la pression oncotique. Il s'y ajoute des mécanismes intrarénaux directement liés à l'atteinte rénale.
a) Ascite de la cirrhose :
- Habituellement, il y a un facteur déclenchant ou favorisant : infection bactérienne (pulmonaire, cutanée, urinaire, septicémie), hémorragie digestive, poussée de la maladie causale.
- Un œdème des membres inférieurs est fréquent en cas d'ascite tendue (comprimant la veine cave inférieure), plus rare en son absence. En l'absence d'ascite tendue, une insuffisance veineuse associée doit être cherchée. L'insuffisance rénale est souvent associée à la présence d'une ascite volumineuse et témoigne de la gravité de l'hypertension portale.
- Une complication très grave de la cirrhose est la péritonite bactérienne spontanée (ou infection spontanée du liquide d'ascite) secondaire à une translocation bactérienne intestinale ou à un ensemencement du liquide par voie directe ou par voie hématogène.
-
Le liquide d'ascite non infecté au cours de la cirrhose est pauvre en leucocytes et en protéines (< 25 g/L). Cela s'explique par le fait que le liquide d'ascite est filtré à travers les capillaires sinusoïdes, remaniés par la fibrose hépatique (capillarisation des sinusoïdes avec perte de leur fenestration) qui les rend moins perméables à l'albumine.
-
Le diagnostic d'infection d'ascite est posé lorsque le taux de polynucléaires neutrophiles est supérieur à 250/mm3, qu'il existe ou non des germes. Les germes (généralement des bacilles à Gram négatif de la flore digestive) sont exceptionnellement mis en évidence par l'examen direct, et inconstamment par les cultures.
b) Ascite du syndrome de Budd-Chiari
- L'ascite est une manifestation majeure du syndrome de Budd-Chiari (obstruction des veines hépatiques), qui est généralement dû à une thrombose.
- L'œdème des membres inférieurs est en partie dû à la compression de la veine cave inférieure par le gros foie et par l'ascite.
- L'ascite est riche en protéines (> 25 g/L) et pauvre en leucocytes pour des raisons analogues à celles indiquées pour l'insuffisance cardiaque.
c) Ascite de l'insuffisance cardiaque
- L'ascite est une manifestation de l'insuffisance cardiaque congestive droite ou globale avancée. Elle est généralement associée à un œdème déclive.
- L'ascite est riche en protéines (> 25 g/L) et pauvre en leucocytes.
- Cela s'explique par le fait que le liquide d'ascite est filtré à travers les capillaires sinusoïdes, dilatés par l'hypertension veineuse mais par ailleurs normaux (fenestration préservée), donc largement perméables aux protéines.
d) Ascite du syndrome néphrotique
- L'ascite est une manifestation inconstante du syndrome néphrotique. Elle est associée à une anasarque.
- L'ascite est pauvre en leucocytes et pauvre en protéines (< 25 g/L) en raison de l'hypoalbuminémie.
ÉPIDÉMIOLOGIE
Votre texte ici
EXAMEN CLINIQUE
Les données de l'examen clinique peuvent, à elles seules, faire le diagnostic de l'ascite et de sa cause. Il faut garder à l'esprit que la cirrhose, l'insuffisance cardiaque et la carcinose péritonéale sont les principales causes d'ascite dans notre pays.
A) Interrogatoire
- Histoire de la maladie : début des symptômes, mode d'installation, facteur déclenchant, signes associés...
- A visée étiologique :
- Les facteurs de risque, les causes et les signes de cirrhose (VHC, VHB, toxicomanie, alcoolisme chronique, syndrome métabolique...) et statut VIH.
- Les facteurs de risque et les signes de maladie cardiaque et de maladie bronchopulmonaire (particulièrement les signes d’insuffisance cardiaque droite).
- Les antécédents, les facteurs de risque et les signes de cancers (surtout de l’appareil digestif ou génital), de lymphome ou de maladie du pancréas
- Les antécédents, notion de contage et les signes de tuberculose
- Les facteurs de risque, les causes et les signes de syndrome néphrotique.
- Les antécédents de chirurgie ou de traumatisme abdominaux.
- Une exposition à l’amiante et la notion d’asbestose.1
- Retentissement : dyspnée, abdomen tendu et douloureux, hernie récemment apparue.
B) Examen physique
1) Ascite de faible abondance (< 1,5L)
- L'ascite est souvent asymptomatique et ne le sera décelé que par l'échographie et/ou une ponction exploratrice.
- L’installation de l’ascite est parfois précédée d'un météorisme abdominal.
- Chez certains sujets, elle peut déjà entraîner la distension d'une hernie crurale, inguinale ou ombilicale, antérieurement connue ou méconnue.
- Dans certains cas l'installation de l'ascite s'accompagne de quelques douleurs abdominales.
- L'examen clinique peut retrouver une prise de poids récente inexpliquée
2) Ascite de moyenne ou grande abondance abondance (> 1,5L)
Le diagnostic d'ascite est très fortement suggéré lorsque s'associent, chez un sujet atteint d'une maladie connue pour causer une ascite :
-
une augmentation de volume de l'abdomen.
-
une matité abdominale déclive, mobilisable, à limite supérieure horizontale dessinant une courbe concave en haut (anatomiquement) sur le sujet en décubitus dorsal.
a) Inspection :
- Plus l'ascite est abondante, plus la distension de l'abdomen devient alors évidente.
- L'ombilic est souvent éversé.
- Les muscles grands-droits de l'abdomen sont plus ou moins écartés (diastasis)
b) Palpation et percussion
- Il est généralement impossible de palper le foie et la rate.
- Signe du glaçon : si l'abdomen n'est pas trop tendu, et s'il existe une splénomégalie ou une hépatomégalie : la dépression brusque de la paroi refoule l'organe qui donne ensuite un choc en retour (à la manière d'un glaçon qu'on enfonce dans l'eau et qui remonte à la surface).
- Signe du flot : En appuyant de part et d'autre sur l'abdomen, on perçoit bien le mouvement du liquide. L'équivalent du signe du flot peut être recherché en effectuant une chiquenaude sur un flanc qui sera transmise à l'autre flanc.
- On constate une matité des flancs avec un tympanisme de la région péri-ombilical en décubitus dorsal.. Si le malade est placé en décubitus latéral, la matité s'exagère dans le flanc où le liquide s'accumule et diminue ou disparaît dans l'autre (matité déclive). La matité déclive caractéristique de l’ascite n’apparaît cliniquement que pour un épanchement péritonéal d’au moins 1,5 litre mais cela dépend aussi de la constitution des patients.1 1 1 En cas d'ascite cloisonnée, la percussion retrouve une matité fixe
3) Complications
- Fonction ventilatoire et examen pulmonaire complet : Une mauvaise tolérance respiratoire (dyspnée) peut être liée à l'ascite elle-même (compression du diaphragme) mais doit aussi faire rechercher un épanchement pleural associé généralement localisé à droite ou une autre complication : pneumopathie aiguë, tuberculose, embolie pulmonaire...
- Lorsque l’ascite est abondante, elle peut être associée à un tableau d’anasarque avec œdèmes des membres inférieurs, scrotale et épanchements pleuraux. Les œdèmes des membres inférieurs sont très fréquemment associés à l'ascite du cirrhotique (on parle d'ailleurs de décompensation œdémato-ascitique) et apparaissent souvent quelques jours ou semaines avant l'ascite; ils sont liés à l'hypo-albuminémie et à la compression de la veine cave inférieure par le foie ou l'ascite.
- Hernie ombilicale et ses complications : rupture et étranglement/ Eventration
- Température, signes de sepsis.
4) Etiologie
- En faveur d'une cirrhose : signes d'hypertension portale, d'insuffisance hépato-cellulaire et de décompensation.
- Signes d'insuffisance ventriculaire droite.
- Aires ganglionnaires.
EXAMENS COMPLÉMENTAIRES
A) Examens sanguins et urinaires
Ils incluent :
-
protéinurie des 24 heures et électrophorèse des protéines (syndrome néphrotique) ;
-
hémogramme, électrophorèse des protéines, albuminémie, taux de prothrombine, bilirubinémie (cirrhose)
-
proBNP ou BNP, uniquement lorsque les signes cliniques et échographiques d'insuffisance cardiaque sont discutables.
Leur second intérêt est de préciser le fonctionnement rénal, souvent perturbé quelle que soit la cause de l'ascite :
-
sodium et potassium, sanguins et urinaires
-
créatinine plasmatique et urinaire.
B) Imagerie
Il faut toujours faire une imagerie abdominale lors d'une 1ère poussée d'ascite.
1) Échographie-doppler abdominale
a) Diagnostic-prélèvement
- Permet le diagnostic d’une ascite de faible abondance dès 100 mL.
- Permet de diriger une ponction d’ascite en cas d’ascite de faible abondance (peut être fait dans le même temps), cloisonnée ou que l’anatomie du malade n’est pas favorable.
- Permet d’éliminer un diagnostic différentiel : tumeur pelvienne, globe vésical, autres collections abdominales.
b) Recherche des arguments pour une étiologie
- Recherche de signes de cirrhose et complications : Dysmorphie hépatique, signes d'hypertension portale, thrombose portale, carcinome hépatocellulaire.
- Anomalie de la morphologie pancréatique, image de pseudo-kyste
- carcinose ou mésothéliome : épaississement pariétal d’une tumeur péritonéale (nodules péritonéaux)
- Tumeur de l’ovaire ou de l’appareil digestif,
adénopathies intra ab
dominales.
- Obstruction des veines hépatiques d’un syndrome de Budd-Chiari.
- Dilatation des veines hépatiques et de la veine cave inférieure d’une insuffisance cardiaque droite ou d’une péricardite constrictive.
2) TDM/IRM
- Tomodensitométrie et IRM n’ont d’intérêt que dans les cas où l’échographie est peu contributive ou en cas d'ascite cloisonnée.
- Des coupes thoraciques permettent de rechercher une atteinte extra-digestive comme une tuberculose ou une sarcoïdose.
- Elles sont particulièrement utiles pour la mise en évidence :
- des tumeurs de l’appareil digestif ou de l’ovaire
- des tumeurs du péritoine
- des affections pancréatiques.
Dans tous ces cas, les examens permettent de préciser l’accessibilité des tumeurs détectées à une biopsie dirigée.1
3) L'échographie cardiaque
- Elle est nécessaire en cas de cardiopathie.
- En cas d'ascite liée à une cardiopathie, les veines hépatiques sont toujours dilatées.
C) Ponction d'ascite (paracentèse) diagnostique (± Ponction évacuatrice si ascite mal tolérée ou ascite réfractaire.)
La ponction d’ascite quelle qu’en soit la méthode (ponction à l’aveugle ou bien écho-guidée) est l’élément clef permettant une orientation diagnostique. La ponction est sans danger lorsque les règles sont respectées. Les analyses sont peu coûteuses, largement disponibles en routine, et donnent souvent des résultats spécifiques. Leur sensibilité n'est cependant pas parfaite. Autrement dit, elles échouent à fournir la clé du diagnostic dans bon nombre de cas (faux négatifs).
1) Indication
Une paracentèse de diagnostic doit être réalisée :
- chez tous les patients avec une première poussée d’ascite de stade 2 ou 3. (Niveau A1).
- chez tous les patients hospitalisés suite à l’aggravation d’une ascite ou la complication d’une cirrhose (Niveau A1) afin d’exclure une PBS (péritonite bactérienne spontanée).
- chez tous les patients cirrhotiques avec un état de choc, de la fièvre ou d’autres signes d’inflammation systémique ou symptômes gastro-intestinaux, ainsi que chez les patients avec une aggravation des fonctions hépatique et/ou rénale. (Niveau A1)1
2) Contre indication
- Doute diagnostique : réaliser une échographie abdominale préalable indispensable dans ce cas, en demandant à l'échographiste de repérer l'ascite si celle-ci est effectivement peu abondante ou cloisonnée voire de réaliser une ponction sous échographie.
-
Vessie distendue : en cas de rétention urinaire, le patient doit être sondé au préalable.1
-
Splénomégalie s'étendant jusqu'en FIG.
- Les troubles de l’hémostase habituels dans la cirrhose ne contre-indiquent pas la ponction (TP ≥ 40 %, plaquettes ≥ 40 000/mL, absence de coagulation intravasculaire disséminée) et n’indiquent pas la transfusion prophylactique de plaquettes ou de plasma.1 1
3) Réalisation
La paracentèse doit se faire selon les règles suivantes :
- après avoir expliqué au patient la procédure, ce que l’on en attend, et ses désagréments.
- après avoir vérifié que la rate n’occupe pas la fosse iliaque gauche (splénomégalie importante), par la palpation ou la revue des examens d’imagerie disponibles.
- Le patient est en décubitus dorsal +/- latéral G , le tronc surélevé de 30-45° pour permettre au liquide d’ascite de se concentrer dans les parties inférieures de l’abdomen.
-
Une anesthésie locale avec un patch d'Emla® 5% à poser
une heure avant le geste est parfois souhaitée par le patient
- La ponction se fait en un point situé à la jonction du tiers externe et du tiers moyen de la ligne joignant l’épine iliaque antéro-supérieure gauche et l’ombilic, et en pleine matité (pas de ponction à droite car le colon droit est plus superficiel = risque d'effraction digestive et de péritonite et souvent hépatomégalie dans la cirrhose).
- Après nettoyage et désinfection de la peau sur une surface large, en respectant les précautions universelles et les règles de l’asepsie.
- Au moyen d’une aiguille ou d’un petit cathéter monté sur un mandrin, branchés sur une seringue permettant de maintenir une légère aspiration.
- L'aiguille est introduit perpendiculaire au plan cutané en évitant les grosses collatérales veineuses visibles sur les flancs, continue cette trajectoire à travers les tissus sous-cutanés jusque dans la cavité péritonéale (irruption du liquide dans le corps de la seringue) sans excéder un trajet d'environ 5 cm.
- Ne jamais réintroduire le guide métallique dans le dispositif de ponction (risque de scinder le cathéter et de laisser une partie de celui-ci dans la cavité abdominale).
- Effectuer sur des échantillons du liquide prélevé des analyses cytologiques, microbiologiques, et biochimiques appropriées.1
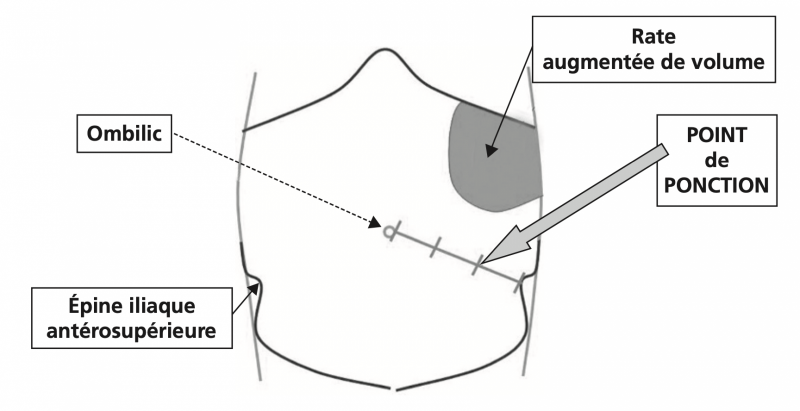
En pleine matité, à la jonction du tiers externe et du tiers moyen de la ligne joignant épine iliaque antérosupérieure et ombilic.
4) Analyse du liquide d'ascite
- Le péritoine est une barrière qui va réguler les échanges en fonction de la pression hydrostatique et de la pression oncotique des protéines. La composition du liquide d’ascite est donc fonction de la pression veineuse dans le territoire portal mais également lymphatique ainsi que par la capacité de sécrétion ou de résorption du tissu péritonéal lui-même.1 L’analyse du liquide d’ascite donne ainsi une orientation générale et des pistes étiologiques.
- Les analyses du premier prélèvement d'ascite chez un malade donné doivent être complètes.
- Sauf situation particulière, les analyses ultérieures devraient être limitées à un examen cyto-bactériologique de routine.
a) Analyse macroscopique
-
Citrin (habituel) : liquide jaune citron, fluide, ne coagulant pas
-
Trouble : en cas d'infection
-
Hémorragique : en cas d'origine néoplasique
-
Chyleux : en cas de compression du système lymphatique.
b) Analyse microscopique
- Biochimie :
- Afin de déterminer le taux de protides et l’albumine (et éventuellement le dosage des enzymes pancréatiques (lipase), ou triglycérides).
- Il est important de mesurer la concentration protidique totale dans l’ascite car les patients dont la concentration protidique dans l’ascite est inférieure à 15 g/L ont un risque augmenté de développer une péritonite bactérienne spontanée (Niveau A1) et peuvent bénéficier d’une prophylaxie antibiotique (Niveau A1).1
- La différence entre la concentration d'albumine de l'ascite et celle du plasma («gradient d'albumine») permet une estimation indirecte de la pression portale. Son utilité est limitée à des cas rares, mais lorsqu'il est supérieur à 11 g/L, il est quasi spécifique d'ascite due à l'hypertension portale.1
- La lipasémie et la triglycéridémie doivent être déterminées simultanément pour comparaison des concentrations dans l'ascite et dans le plasma.
- Bactériologie :
- Un tube standard (pot à ECBU) avec examen direct grâce à la coloration de May-Grünwald-Giemsa
- et mise en culture systématique sur flacons d'hémocultures aérobies et anaérobies ensemencés avec du liquide d’ascite permettant la mise en évidence plus fréquente d’un germe en cas d’infection.
-
Le compte des polynucléaires neutrophiles et la culture du liquide ascitique (par inoculation dans des bouteilles de cultures sanguines au chevet) doivent être réalisés afin d’exclure toute péritonite bactérienne (Niveau A1).
- Cytologie :
A côté de ces explorations« standards» que l'on doit effectuer devant toute première poussée d'ascite, on peut demander d'autres examens en fonction des hypothèses diagnostiques initiales. Quelques exemples :
- Il faut obligatoirement déterminer la concentration en protéines du liquide d’ascite qui est mise en perspective avec la concentration en albumine du sérum, permettant de définir le gradient protéique sérum-ascite.1 On considère qu’une ascite est pauvre en protides pour des valeurs inférieures à 25 g/L qui historiquement permettaient de différencier les transsudats des exsudats. Le gradient albumine sérique-albumine dans l’ascite est plus discriminant et on considère que lorsque ce gradient est > 11g/L, il s’agit dans la majorité des cas d’une ascite secondaire à une hypertension portale et plus rarement à une dénutrition protéique sévère. À l’inverse lorsque ce gradient est < 11 g/L une hypertension portale est peu probable et il s’agit dans la majorité des cas d’une tuberculose, d’une carcinose ou d’une autre cause.1 1
- Des analyses biochimiques complémentaires sont utiles dans certaines situations :1 1
- En cas d’ascite d’aspect laiteux, l’élévation du taux des triglycérides dans le liquide permet de confirmer le caractère chyleux de l’ascite.
- L’augmentation dans l’ascite du taux de cholestérol avec un seuil de 1,8 mmol/l ou des LDH par rapport à la concentration sérique est fréquente en cas de néoplasie avec une sensibilité de 90 % mais avec une mauvaise spécificité.1
- Le dosage des enzymes pancréatiques (lipase) si suspicion de rupture d'un canal pancréatique
- Le dosage d'acide hyaluronique/mésothéline est élevé dans l'ascite en cas de mésothéliome péritonéale.
- Le dosage de l’adénosine désaminase,1 lorsque son taux est élevé (> 21 à 30 UI/L) dans le liquide d’ascite, est un élément d’orientation vers une tuberculose péritonéale. La sensibilité de ce marqueur serait de 90 à 100 % avec une spécificité de 80 à 97 %. Cependant, en cas de cirrhose, la sensibilité de l’augmentation de l’adénosine désaminase n’est que de 30 %.1
- L’analyse de marqueurs tumoraux (ACE, α-fœto-protéine, CA 19/9, CA 125) dans l’ascite n’ont pas une sensibilité ou de spécificité suffisante pour pouvoir être recommandée.1
5) Complications
a) Evènements indésirables (EI) :
-
Echec de la ponction
-
Douleur post-ponction.
-
Sortie accidentelle du cathéter court
-
Hématome de paroi <1% (pas de mesure préventive efficace) : complication la plus fréquente
-
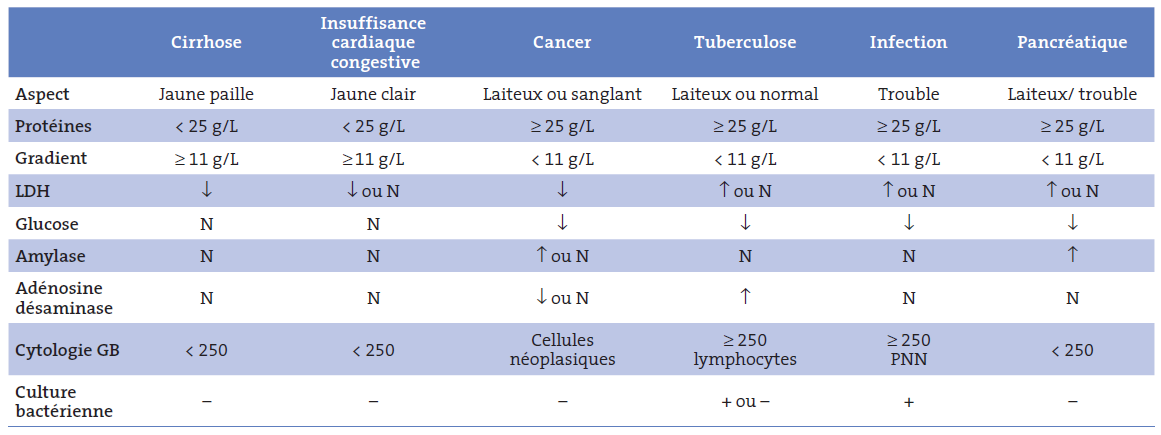
Fuite de liquide hors de la paroi abdominale post paracentèse : La fuite d’ascite par l’orifice de ponction, plus fréquente en cas d’œdème pariétal, pourrait être prévenue par la technique (trajet en baïonnette lors de la ponction, éloignant le point d’entrée cutanée du point d’entrée péritonéal), et doit être traitée sans attendre (suture, pansement compressif, décubitus latéral opposé) pour éviter les risques de déplétion volémique et d’infection (la simple pose d’une « poche » adhésive est à proscrire).
b) Evènements indésirables (EI) graves :
-
Perforation intestinale, hémopéritoine (Ponction d’une veine superficielle de la paroi abdominale, de varices mésentériques ou plaie de rate) surviennent sans doute plus souvent (1,5 %)1 que ce qui était généralement écrit (< 1 cas sur 1 000).1
-
Etranglement herniaire (prévenue par une réduction de la hernie avant et pendant la ponction)
D) Études hémodynamiques
- Elles ne sont utiles que dans les cas rares où examen clinique, examens du liquide d'ascite et échographie n'ont pas permis d'affirmer ni d'écarter une atteinte cardiaque ou une cirrhose.
- Elles consistent en un cathétérisme de la veine jugulaire interne pour mesure des pressions veineuse centrale, veineuse hépatique (libre et bloquée), auriculaire droite, ventriculaire droite et artérielle pulmonaire (libre et bloquée), ainsi qu'une détermination du débit cardiaque. Cette approche permet également d'effectuer une biopsie hépatique transveineuse.
On peut ainsi attribuer l'ascite :
-
à une cirrhose quand le gradient de pression veineuse hépatique (pression bloquée – pression libre) est
> 10 mmHg;
-
à une insuffisance cardiaque droite ou à une péricardite constrictive lorsque la pression dans l'oreillette droite est > 12 mmHg. On peut aussi préciser le type d'atteinte cardiaque éventuelle, et notamment une péricardite constrictive dont le diagnostic peut échapper à l'échographie cardiaque.
-
à un autre mécanisme lorsque le gradient de pression veineuse hépatique et la pression dans l'oreillette droite sont normaux.
E) Cœlioscopie, endoscopie et histopathologie
1) Cœlioscopie (ou laparoscopie)
- Elle permet d'examiner le péritoine et la surface du foie, et de biopsier des lésions péritonéales éventuelles ou de faire une ponction-biopsie hépatique.
- Elle est contre-indiquée par un état précaire, une laparotomie antérieure, des troubles de l'hémostase non corrigés.
2) Biopsies du péritoine ou de lésions abdominales
Elles ne doivent être effectuées que lorsque l'examen cytologique du liquide d'ascite est non concluant, et que les examens d'imagerie ou les examens hémodynamiques ont permis d'exclure les causes communes (cirrhose et insuffisance cardiaque).
Elles peuvent être effectuées sous cœlioscopie, ou par voie percutanée, guidée par l'échographie :
-
sur une zone anormale du péritoine, une adénopathie ou une autre lésion ;
-
sur une zone de péritoine apparaissant normale en l'absence de lésion focale.
Le rendement des biopsies péritonéales dirigées est excellent pour la carcinose péritonéale, le mésothéliome et la tuberculose. Elles n'ont aucune place dans le diagnostic des ascites les plus communes (cirrhose et insuffisance cardiaque).
3) Endoscopie digestive
- Sa place est limitée à la recherche ou à la caractérisation d'une tumeur digestive en cas de carcinose péritonéale, et à la recherche de signes d'hypertension portale en cas de suspicion de cirrhose.
DIAGNOSTICS DIFFÉRENTIELS
Parce que la constitution d’une ascite s’accompagne fréquemment d’un météorisme, il n’est pas toujours facile de reconnaître une ascite peu abondante chez un patient à l’abdomen distendu et tympanique.
A) Causes d'augmentation du volume de l'abdomen
- Obésité.
-
Grossesse
- Stase stercorale colique
- Occlusion intestinale aiguë mais tableau clinique très différent et tympanisme
- Tumeur pelvienne (ovaire)
- Globe vésical (dysurie, matité sous-ombilicale médiane convexe vers le haut)
B) Causes d'épanchement péritonéal
- Epanchement purulent = péritonite purulente
- Hémopéritoine post-traumatique, spontané (rupture tumorale d'un carcinome hépatocellulaire) ou Iatrogène (ponction-biopsie hépatique, postopératoire). Le liquide de ponction peut être rendu sanglant par la traversée accidentelle d’un vaisseau sanguin de la paroi. Le diagnostic d’hémopéritoine peut être corrigé par une ponction ultérieure montrant un liquide clair. À l’inverse, il peut être confirmé si un examen d’imagerie abdominale non-invasive montre des caillots dans le péritoine. Un hématocrite du liquide de ponction < 1 % permet d’écarter le diagnostic d’hémopéritoine. La distinction est parfois difficile mais le contexte apporte le plus souvent des arguments décisifs (notion de traumatisme ou de lésion intra-abdominale pouvant être la source d’un saignement).1
ÉTIOLOGIE
A partir des renseignements obtenues par l'examen clinique (et notamment les données anamnestiques) , les données des examens sanguins de routine, l'analyse complète du liquide d'ascite et l'échographie abdominale, l'orientation étiologique est souvent évidente.
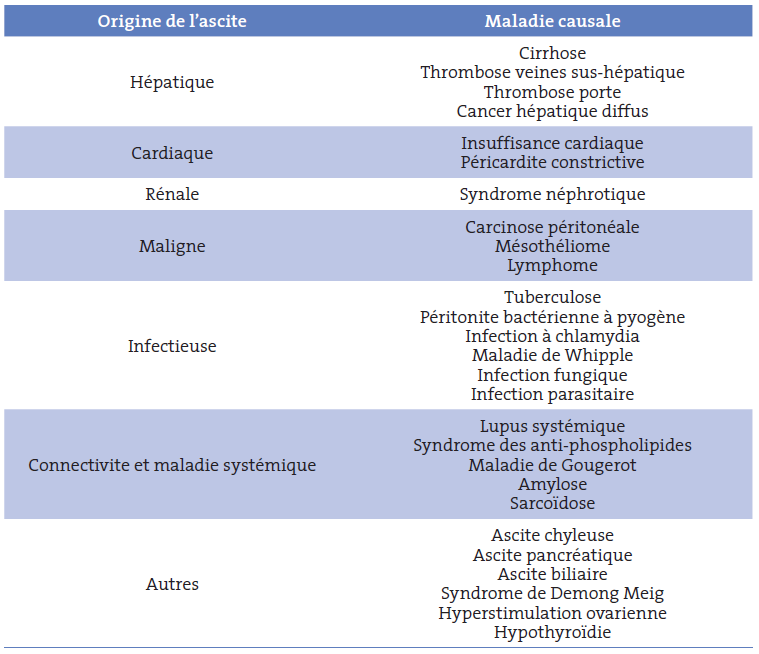
A) Démarche diagnostique commençant par la recherche des 3 principales causes d'ascite
Il faut garder à l'esprit que : la cirrhose, l'insuffisance cardiaque droite et la carcinose péritonéale sont les 3 principales causes d'ascite.
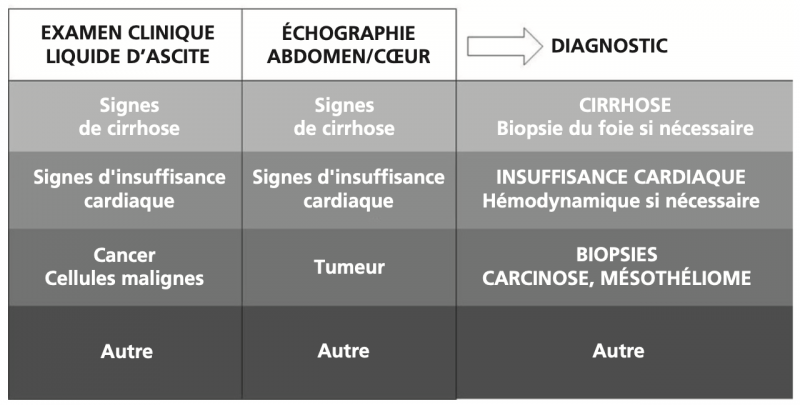
1) Ascite cirrhotique
Lorsqu'une ascite est due à une cirrhose, les arguments cliniques, biologiques ou échographiques de cirrhose sont généralement présents sans qu'il soit nécessaire de recourir à des examens invasifs comme une biopsie hépatique ou une étude hémodynamique.
Le cas échéant, le diagnostic d'ascite cirrhotique peut être posé lorsque :
- les caractéristiques du liquide sont compatibles (protéines <25 g/L ou gradient d'albumine >11 g/L, absence de lipase et de triglycérides, lymphocytes <700/mm3, polynucléaires neutrophiles < 250/mm3), sans cellule anormale.
-
les veines hépatiques ne sont pas dilatées.
-
il n'y a pas de protéinurie importante (> 3 g/24 h).
Cas particulier important : s'il y a des signes de cirrhose et si le taux de polynucléaires neutrophiles est supérieur à 250/mm3, le diagnostic d'infection du liquide d'ascite (péritonite bactérienne spontanée) doit être posé. En cas d'ascite hémorragique, il faut corriger le taux de neutrophiles dans l'ascite en soustrayant 1 neutrophile pour 250 globules rouges retrouvés dans l'ascite. Une fois établi le diagnostic d'ascite cirrhotique, il faut chercher un facteur déclenchant de la poussée d'ascite (causes de décompensation) et évaluer la fonction rénale et la natrémie.
2) Insuffisance cardiaque
Si les veines hépatiques sont dilatées, le diagnostic d'ascite cardiaque peut être posé :
-
s'il n'y a pas de signes de cirrhose (notamment, s'il n'y a pas de circulation collatérale portosystémique évidente à l'examen clinique ou échographique, voire endoscopique).
-
si le liquide d'ascite est riche en protides (> 25 g/L) et pauvre en leucocytes.
-
s'il n'y a pas de protéinurie importante (> 3 g/24 h).
L'échographie cardiaque permet de confirmer le diagnostic par une caractérisation de la cardiopathie sous-jacente.
3) Carcinose péritonéales
-
Il s'agit d'un envahissement métastatique du péritoine prenant généralement la forme de nodules tumoraux multiples.
-
En cas d’ascite maligne, la physiopathologie de l’ascite est multifactorielle avec une augmentation de la perméabilité vasculaire et une obstruction du drainage lymphatique.1 Cette augmentation de la perméabilité capillaire est favorisée par certaines cytokines comme le VEGF.
-
Les cancers primitifs les plus fréquemment à l'origine de carcinose sont gynécologiques (ovarien++ et utérin) mais aussi digestifs (colorectal +++, estomac ou pancréatique.1 Plus rarement : cancer du sein, cancer du poumon. À la différence des cancers solides, les ascites lymphomateuses sont plus rares.
-
La carcinose peut apparaître de façon synchrone (10-15 % des cas en cas de cancer colorectal) ou métachrone (10-35 % des cas) par rapport au primitif.
-
Les 2 manifestations cliniques possibles de la carcinose péritonéale sont l'ascite et le syndrome occlusif (l'ascite est due à un suintement et/ou saignement des nodules tumoraux dans le péritoine).
-
Le diagnostic d'ascite maligne est facile quand des cellules malignes sont mises en évidence par l'examen cytologique du liquide ou quand les examens morphologiques (TDM) montrent des tumeurs péritonéales ou intra-abdominales (notamment ovariennes et digestives).
-
La ponction doit être de volume suffisant pour pouvoir permettre une analyse immuno-histochimique d’éventuelles cellules carcinomateuses. L’étude immuno-histochimique permet de caractériser les cellules carcinomateuses en n’hésitant pas à multiplier les ponctions d’ascite en cas de prélèvement initial négatif. L’analyse cytologique à la recherche de cellules carcinomateuses a une sensibilité qui est variable de 50 % à 97 % en fonction des équipes.1
- Une cœlioscopie diagnostique avec biopsies péritonéales n’est réalisée qu’en deuxième intention si le diagnostic reste incertain.
- Gradient albumine sérum-ascite bas < 11 g/L.
- En cas de carcinose péritonéale, le traitement est le plus souvent chimiothérapique avec ou sans chimiothérapie hyperthermique intra péritonéale. De nouvelles stratégies thérapeutiques utilisant l’immunothérapie sont maintenant disponibles en cancérologie et doivent être intégrées dans la stratégie thérapeutique. C’est le cas du catumaxomab qui est un anticorps monoclonal hybride de rat/souris dirigé spécifiquement contre la molécule d’adhésion cellulaire épithéliale (EpCAM) et l’antigène CD3. L’antigène EpCAM est surexprimé dans la plupart des carcinomes. Le CD3 est exprimé sur les lymphocytes T matures au sein du récepteur du lymphocyte T. Le Catumaxomab induit une réaction immunologique concertée contre les cellules tumorales, faisant intervenir différents mécanismes d’action tels que l’activation des lymphocytes T, la cytotoxicité à médiation cellulaire dépendant des anticorps ou du complément et la phagocytose. Ceci aboutit à la destruction des cellules tumorales.1 L’utilisation du catumaxomab est indiquée pour le traitement intrapéritonéal de l’ascite maligne chez les patients atteints de carcinomes EpCAM-positifs lorsque le traitement standard n’est pas disponible ou lorsque celui-ci n’est plus utilisable. Les résultats des essais de phase II/III, en particulier dans les carcinoses péritonéales au cours des cancers de l’estomac ou ovariens, ont démontré une efficacité statistiquement significative sur la durée de survie sans ponction, qui était quatre fois supérieure à celle du groupe témoin.1 1 L’administration du catumaxomab est réalisée en quatre perfusions intrapéritonéales. La balance bénéfice/risque de ce traitement reste discutée. La combinaison d’une immunothérapie par catumaxomab avec la chirurgie ou la chimiothérapie systémique nécessite d’être évaluée.1 1
B) Démarche diagnostique permettant l'identification de causes rares d'ascite faciles à établir.
- Trois causes rares d'ascite sont faciles à reconnaître : ascite pancréatique, ascite chyleuse et syndrome néphrotique. Quand elles ont été écartées, il reste à affirmer ou à éliminer une tuberculose péritonéale et une tumeur péritonéale.
- La détermination de la protéinurie des 24 heures, de la lipase et des triglycérides dans le liquide d'ascite permet d'établir facilement les diagnostics respectifs de syndrome néphrotique, d'ascite pancréatique et d'ascite chyleuse. Il reste encore à en préciser la cause.
- Lorsque ces diagnostics ne peuvent être établis, il faut chercher une tumeur maligne et une tuberculose par des biopsies péritonéales dirigées soit sur une anomalie mise en évidence par une imagerie non invasive, soit par une cœlioscopie.
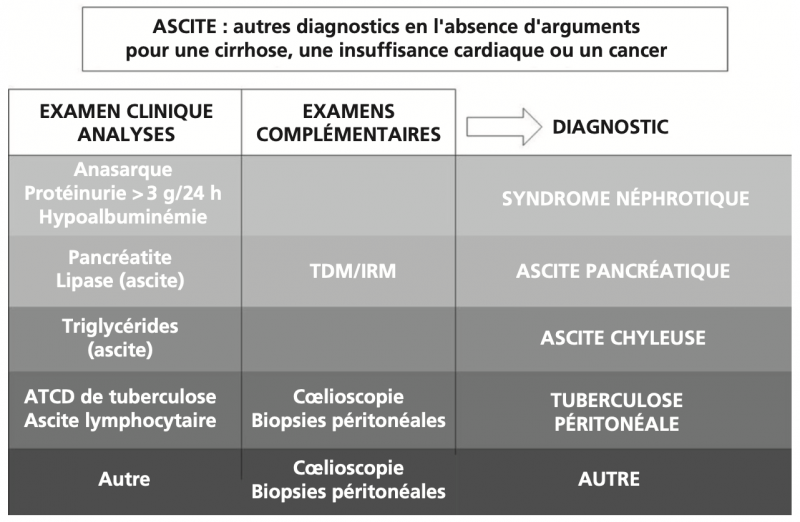
1) Ascite pancréatique
- Généralement liée à la rupture d'un canal pancréatique ou d'un pseudokyste dans le péritoine chez un patient ayant une pancréatite chronique.
- Le diagnostic de l'origine pancréatique du liquide est aidé par : L'imagerie abdominale (scanner +++).
- Le dosage de l'amylase et de la lipase dans le liquide d'ascite, dont les taux sont 5 à 20 fois supérieurs aux taux plasmatiques.
2) Ascite chyleuse
- Elle est suspectée par l’aspect macroscopique blanchâtre ou laiteux du liquide d’ascite riche en protides.1
- Il s’agit d’une ascite riche en triglycérides avec une concentration dans l’ascite > 2 g/L.
- La première cause est liée à un traumatisme chirurgical du canal lymphatique, en particulier en chirurgie urologique ou vasculaire abdominale.1
- Plus rarement, il s’agit d’une atteinte ganglionnaire d’un lymphome (adénopathies tumorales primitives) responsable d'une obstruction lymphatique et exceptionnellement d’une maladie congénitale par dysplasie des canaux lymphatiques ou par une infection parasitaire à filaires après un séjour en zone d’endémie.
- Les ascites chyleuses nécessitent la mise en place de mesures nutritionnelles avec l’utilisation de triglycérides à chaîne moyenne et hyper protidique alors qu’une reprise chirurgicale est proposée en cas d’ascite chyleuse post-opératoire. Un traitement par Somatostatine a montré une certaine efficacité pour des ascites chyleuses post-opératoires.1
3) Syndrome néphrotique
-
L’ascite s’inscrit dans le cadre de l’anasarque. L’ascite est souvent pauvre en protides (fuite rénale de protéines), avec un gradient d’albumine sérum-ascite inférieur à 11 g/L.
Le syndrome néphrotique peut être dépisté facilement par la bandelette urinaire systématique devant toute ascite. Il est défini par une protéinurie supérieure à 3 g/L, associée à une hypoalbuminémie inférieure à 30 g/L.
-
Il correspond à une fuite protéique majeure causée par une altération du glomérule rénal et peut être primitif (le plus souvent chez l’enfant) ou secondaire.
C) Étiologie des ascites non cirrhotiques
1) Gradient albumine sérum-ascite bas < 11 g/L
a) Carcinose péritonéale
b) Mésothéliome péritonéale
- Une tumeur primitive péritonéale comme le mésothéliome est exceptionnelle avec une rentabilité diagnostique de la ponction d’ascite qui est moins bonne (< 40 %) que celle des carcinoses péritonéales sur cancer solide.
-
Le principal facteur favorisant est l'exposition aux fibres d'amiante, de très mauvais pronostic.
-
Généralement révélé par de l'ascite et/ou des douleurs abdominales dans un contexte d'altération de l'état général.
- Le scanner oriente le diagnostic.
- L’augmentation de la mésothéline dans le liquide d’ascite a une sensibilité de 67 % et ne remplace pas l’analyse anatomopathologique.
- En cas de suspicion de mésothéliome, il faut avoir recours à la chirurgie cœlioscopique pour réaliser des biopsies péritonéales permettant un diagnostic de certitude.1
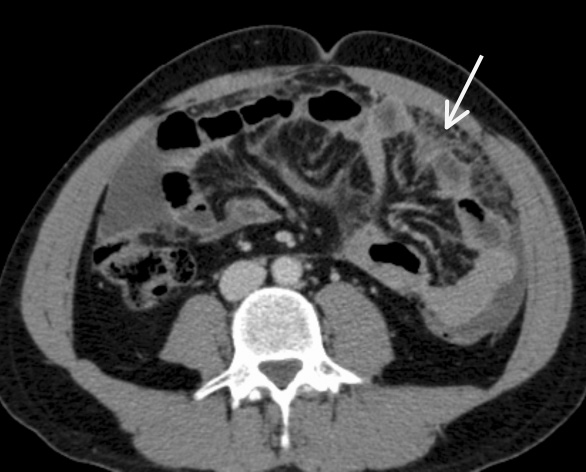
(collection Pr Otal, Radiologie CHU Rangueil Toulouse)
c) Tuberculose péritonéale
- Il s’agit d’un liquide riche en lymphocytes et avec un taux de protéine dans l’ascite > 25 g et un gradient albumine sérum-ascite est < 11 g/L.
-
La tuberculose péritonéale correspond à une localisation extra-pulmonaire de la tuberculose. Le terrain et les facteurs de risque sont les mêmes que pour la tuberculose pulmonaire.
- Le diagnostic est évoqué sur le contexte épidémiologique : un contact ou un séjour en zone d’endémie tuberculeuse.
-
La symptomatologie est liée à l'atteinte péritonéale d'une part (douleurs abdominales, ascite, troubles du transit) et d'autre part aux signes généraux (altération de l'état général, fébricule, sueurs nocturnes ...) et/ou aux autres localisations de l'infection (toux, dyspnée, crachats hémoptoïques...)
- Seulement 38 % des patients ont une tuberculose pulmonaire [8]. L’IDR ou le quantiféron ne sont positifs que dans 50 % à 80 % des cas.1
- Le diagnostic est confirmé par la recherche à l’examen direct, en culture et par PCR de la mycobactérie.
- À l’examen direct, la mycobactérie est mise en évidence dans moins de 6 % des cas alors que la culture sur milieu de Löwenstein n’est positive que chez 20 à 35 % des malades.1
- Le diagnostic par PCR a l’avantage de pouvoir être réalisé sur un volume faible avec un résultat plus rapide mais là-aussi avec une sensibilité insuffisante de 60 à 80 %.
- La valeur prédictive de la positivité du Quantiféron dans le liquide d’ascite pourrait être intéressante mais reste non validée.1
- En cas de négativité des examens microbiologiques avec une forte suspicion clinique, le diagnostic est fait par un abord chirurgical cœlioscopique mettant en évidence sur le péritoine les granulomes avec nécrose caséeuse dont la sensibilité est excellente > 95 %.1
- En cas d’ascite tuberculeuse, un traitement de 6 mois est nécessaire en débutant par une quadrithérapie de 2 mois. Il faudra vérifier la sensibilité phénotypique de la souche en culture à l’isoniazide. Pour éviter, une fibrose péritonéale secondaire, une corticothérapie de quelques semaines est introduite dans les tuberculoses pulmonaires florides.1
d) Hypertension portale par bloc sus-hépatique
+ Syndrome de Budd-Chiari (thrombose des veines sus-hépatiques).1
- Il se rencontre essentiellement chez des patients présentant un syndrome myéloprolifératif, des troubles de l’hémostase ou des maladies systémiques.
- L’ascite est l’expression clinique la plus fréquente (83 %) et la concentration de protides dans le liquide d’ascite est supérieure à 25 g/L.
- Le syndrome de Budd-chiari doit faire réaliser un bilan d’une thrombophilie constitutionnelle ou acquise.
- Au cours du syndrome de Budd-chiari, le traitement anticoagulant ou du facteur de thrombophilie associé est nécessaire et peut être complété par la mise en place d’un shunt porto-sus-hépatique par voie Trans jugulaire (TIPS) .1 1 Le traitement du foie cardiaque sera le plus souvent médical sauf en cas de péricardite constrictive où il sera chirurgical.
+ Insuffisance cardiaque droite :
- Comme pour le syndrome de Budd-Chiari, l’ascite est majoritairement riche en protides, les capillaires sinusoïdes étant perméables aux protides habituellement (contrairement à la cirrhose).
- La présentation clinique est celle d’une insuffisance cardiaque droite ou globale.
- Un « foie cardiaque » biologique (baisse du TP, cytolyse) est souvent présent, pouvant à tort orienter vers une pathologie hépatique (si la pathologie cardiaque est inconnue).
- Certaines des causes d’insuffisance cardiaque droite aiguë sont des urgences vitales (tamponnade, péricardite chronique constrictive, embolie pulmonaire massive), devant entraîner la réalisation d’une échographie cardiaque en urgence permettant ensuite une prise en charge spécialisée adaptée.
e) Maladie dysimminutaire
- Les connectivites peuvent s’associer à une ascite qui est en général riche en protides et secondaire à une sérite par vascularite péritonéale en particulier pour le lupus systémique.1
- Une connectivite est à différencier d’une atteinte péritonéale d’un syndrome hyperéosinophilique ou le taux d’éosinophiles sanguins est très élevé avec une ascite également riche en éosinophiles.
- En cas de syndrome néphrotique au cours d’un lupus ou d’une amylose, l’ascite s’intègre dans une anasarque liée à une hypoalbuminémie majeure avec protéinurie élevée.
f) Maladie gélatineuse du péritoine.
- Il s’agit d’une entité rare (prévalence : 1/1 million), correspondant à une prolifération intrapéritonéale de tumeurs de malignité variable.
- Elle se caractérise par une ascite mucineuse récidivante, insidieuse, liée dans 90 % des cas à une tumeur mucosécrétante, le plus souvent appendiculaire;
- Elle est également décrite dans des tumeurs ovariennes. Le terme de gélatineux correspond à l’aspect de l’ascite ; elle est également nommée pseudomyxome péritonéal.
- Le tableau clinique est pauvre, dominé par une altération de l’état général associée à de l’ascite.
- La présentation anatomopathologique est celle d’un adénocarcinome de bas grade.
- Le traitement, repose sur la combinaison d’un traitement médical (chimiothérapie spécifique intrapéritonéale [CHIP]) et d’un traitement chirurgical (péritonectomie).1
2) Gradient albumine sérum-ascite élevé > 11 g/L
En-dehors de la cirrhose, il s’agit souvent d’un bloc intrahépatique.
a) Maladies vasculaires du foie :
- Il s’agit le plus souvent d’une maladie vasculaire du foie avec une hypertension portale non cirrhotique.1
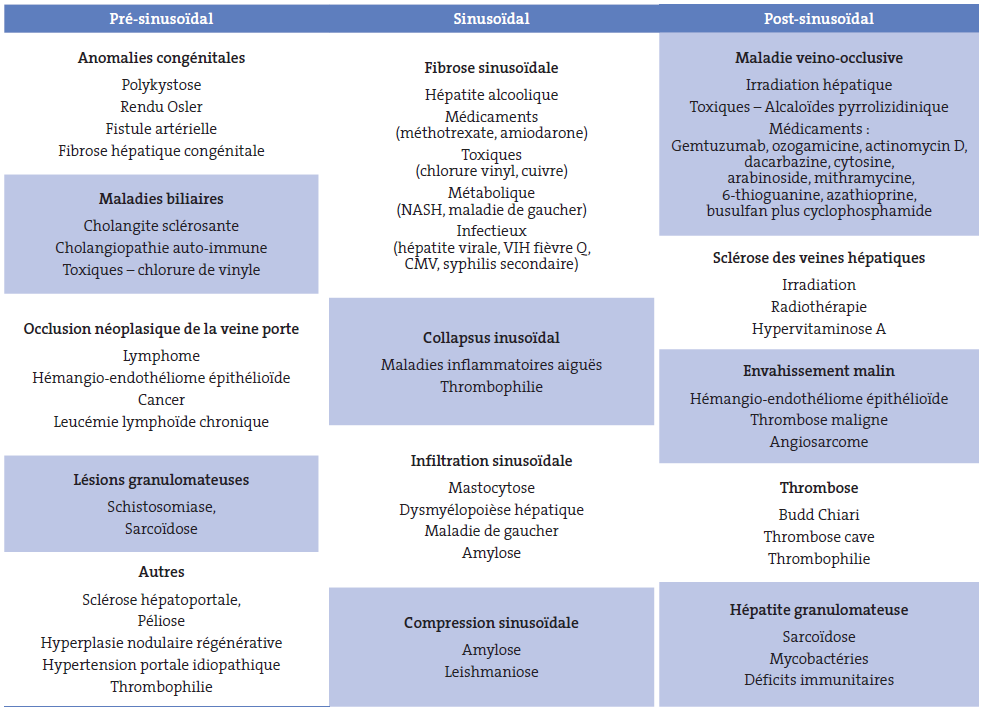
- L’hypertension portale non cirrhotique inclut des maladies vasculaires diverses dont la classification dépend du siège de l’augmentation des résistances vasculaires qui peut être sinusoïdale, pré-sinusoïdale ou plus rarement post-sinusoïdale.
- L’imagerie par scanner peut donner un élément d’orientation en précisant le caractère homogène ou nodulaire du foie et la perméabilité des veines sus hépatiques ou du tronc porte.
-
Le diagnostic d’hypertension portale non cirrhotique repose sur les critères de Schouten et al.1 associant les points suivants : splénomégalie et hypersplénisme, varices œsophagiennes, ascite, augmentation du gradient porto-sus-hépatique, circulation collatérale, exclusion de la cirrhose sur la biopsie hépatique, exclusion des autres causes de maladie hépatique (virale stéato-hépatite, hépatite auto-immune, hémochromatose, maladie de Wilson ou cirrhose biliaire primitive), exclusion des autres causes d’hypertension portale non cirrhotique (fibrose hépatique congénitale, la sarcoïdose ou la bilharziose), perméabilité des veines sus hépatiques et de la veine porte par imagerie de type écho-doppler ou scanner.
-
Les complications de l’hypertension portale non cirrhotique sont dominées par les hémorragies digestives par rupture de varices alors que l’ascite n’est présente que dans 10 à 34 % des cas.1 -
Le diagnostic est porté par l’étude hémodynamique et surtout par la biopsie hépatique. Le diagnostic anatomopathologique est souvent difficile et nécessite un prélèvement de taille suffisante.1 Le dialogue avec l’anatomopathologiste est très important et permet de préciser l’atteinte vasculaire et la présence éventuelle d’une hyperplasie nodulaire régénérative avec transformation nodulaire du parenchyme hépatique en l’absence de fibrose extensive péri-nodulaire.
Dans le cas de l’hypertension portale non cirrhotique, la prise en charge est plus difficile avec le traitement de la cause lorsqu’elle a été identifiée. En particulier l’arrêt du médicament s’il s’agit d’une toxicité médicamenteuse ou le traitement de la connectivite par exemple sont indispensables. La mise en place d’un shunt porto sus hépatique par voie transjugulaire en cas d’ascite réfractaire aux diurétiques a une efficacité inconstante avec peu de cas publiés.1
b) Infiltration néoplasique du foie
- L’envahissement du foie par des métastases peut favoriser l’apparition d’une ascite, d’une part par un envahissement des capillaires sinusoïdes favorisant une augmentation de la pression d’amont et permettant le passage du liquide interstitiel à travers la paroi formant une ascite souvent riche en protides, et d’autre part par l’insuffisance hépatique liée à l’infiltration néoplasique, et l’hypoalbuminémie qui en résulte (ascite alors pauvre en protides).
COMPLICATIONS
Les complications mécaniques peuvent se rencontrer quelle que soit la cause de l'ascite, mais les autres complications surviennent généralement sur une ascite d'origine cirrhotique.
A) Complications mecaniques
- Troubles respiratoires par compression phrénique et/ou épanchement pleural associé qui est localisé généralement du côté droit. Le mécanisme de formation de l'hydrothorax est lié à un transfert unidirectionnel de l'ascite abdominale vers la cavité pleurale à travers des brèches diaphragmatiques.
- L'augmentation de pression abdominale peut être responsable de la formation de hernies inguinales ou ombilicales, sources potentielles des habituelles complications d'étranglement herniaire ou d'occlusion intestinale aiguë.
-
Les hernies ombilicales peuvent, en outre, se compliquer de rupture en cas d'ascite tendue et/ou de fragilité cutanée, nécessitant alors un traitement chirurgical en urgence. Le diagnostic de rupture est évident, et d'autant plus grave qu'elle témoigne d'une insuffisance hépatique avancée (qui explique l'atrophie de la paroi cutanée en regard de la hernie).
B) Infection spontanée du liquide d'ascite (ILA) = Péritonite bactérienne spontanée (PBS)1
1) Epidémiologie
- La PBS est une infection bactérienne très courante chez les patients cirrhotiques avec ascite [10,105–107], le plus souvent par translocation de bactéries d'origine intestinale.
-
L'infection d'ascite est une complication grave, potentiellement mortelle. En outre, l'infection du liquide d'ascite témoigne toujours d'une cirrhose grave.
-
Lorsqu’elle fut décrite pour la première fois, sa mortalité excédait les 90 % mais grâce au diagnostic précoce et au traitement, elle a été réduite à environ 20 % [6,108]. -
Tous les patients cirrhotiques avec ascite sont à risque de développer une PBS, dont la prévalence est de 1,5– 3,5 % chez les patients ambulatoires [109,110] et environ 10 % chez les patients hospitalisés [109]. La moitié des épisodes de PBS sont présents au moment de l’admission alors que les autres sont contractés durant l’hospitalisation [10].
2) Symptomatologie
Les patients avec PBS peuvent présenter l’un des signes suivants [10,109,111], mais Il est important de rappeler que la PBS peut être asymptomatique, surtout chez les patients ambulatoires [109,110] :
- Symptômes locaux et/ou signes de péritonite : douleurs abdominales, vomissements, diarrhée, iléus.
- Signes d’inflammation systémique : hyper ou hypothermie, frissons, tachycardie, et/ou tachypnée, polynucléose neutrophile ou augmentation des globules blancs chez un sujet leucopénique, augmentation de la CRP.
- Une encéphalopathie hépatique;
- Un état de choc
- une hémorragie digestive
- Aggravation de la fonction hépatique ou rénale (Insuffisance rénale aiguë)
3) Paracentèse diagnostique
- Une paracentèse diagnostique doit être réalisée chez tous les patients cirrhotiques avec ascite au moment de l’admission afin d’exclure une PBS.
- Une paracentèse diagnostique doit également être effectuée chez les patients avec des saignements gastro-intestinaux, un état de choc, de la fièvre ou d’autres signes d’inflammation systé- mique ou symptômes gastro-intestinaux, ainsi que chez les patients avec une aggravation des fonctions hépatique et/ou rénale, et d’encéphalopathie hépatique (Niveau A1).
- Le diagnostic de PBS repose sur un compte de neutrophiles dans le liquide d’ascite > 250/mm3, déterminé au microscope (Niveau A1). Le nombre de neutrophiles dans le liquide d’ascite est obtenu ainsi : le liquide d’ascite est centrifugé; un frottis est coloré au Giemsa et une numération cellulaire totale et différentielle est réalisée avec un microscope optique. Cela peut être fait en moins de 4 h. [10,107,108,112]. À ce jour, les données sont insuffisantes pour recommander l’utilisation de compteurs cellulaires automatiques ou de bandelettes réactives pour le diagnostic rapide de la PBS.
-
La culture du liquide d’ascite est souvent négative même si elle est effectuée dans des flacons d’hémoculture et n’est pas nécessaire au diagnostic de PBS, mais reste importante pour adapter le traitement antibiotique (Niveau A1). Les cultures sanguines doivent être effectuées, avant l’initiation d’un traitement antibiotique, chez tous les patients où une PBS est suspectée (Niveau A1). Lorsqu’une culture est positive (~40 % des cas), les pathogènes les plus courants sont les bactéries Gram négatifs (BGN), habituellement Escherichia coli et les cocci Gram positifs (principalement streptocoques et entérocoques) [10,105–108]. Une étude récente a montré que 30 % des BGN isolés sont résistants aux fluoroquinolones et que 30 % sont résistants au triméthoprime–sulfaméthoxazole [106]. 70 % des BGN résistants aux fluoroquinolones sont également ré- sistants au triméthoprime–sulfaméthoxazole [106]. Le risque de PBS due aux BGN résistants aux quinolones est plus élevé chez les patients sous norfloxacine que chez les patients naïfs [106]. Le taux de BGN résistants à la céphalosporine est faible chez les patients avec PBS indépendamment d’un traitement prophylactique par norfloxacine [106]. Les patients sous norfloxacine prophylactique peuvent développer une PBS à cocci Gram positifs [10,106– 108].
-
Certains patients peuvent avoir un compte de neutrophiles inférieur à 250/mm3 mais avec une culture du liquide d’ascite positive. Cette pathologie est appelée bactérascite. Si le patient montre des signes d’inflammation systémique ou d’infection, il doit être traité par antibiotique (Niveau A1). Autrement, le patient doit subir une seconde paracentèse quand le résultat de la culture revient positif. Les patients chez qui un deuxième compte de neutrophiles dans l’ascite est > 250/mm3 doivent être traités comme une PBS, et les patients restants (neutrophiles < 250/mm3) doivent être surveillés (Niveau B1).
-
L'infection spontanée du liquide d'ascite est monomicrobienne. Lorsque plusieurs espèces microbiennes sont mises en évidence dans le liquide d'ascite, il faut s'inquiéter d'une perforation du tube digestif et chercher un pneumopéritoine.
4) Traitement
- Dès le diagnostic fait par le compte des polynucléaires dans le liquide d'ascite > 250/mm3, un traitement antibiotique probabiliste doit être initié (Niveau A1).
- Vu que les micro-organismes les plus fréquemment à l’origine de PBS sont les bactéries aérobies à Gram négatives, comme le E. coli, ce sont les céphalosporines de troisième génération qui doivent être proposés comme traitement antibiotique de première ligne (Niveau A1). Il existe des alternatives comme l’amoxicilline/l’acide clavulanique et les quinolones comme la ciprofloxacine ou l’ofloxacine. L’utilisation de quinolones ne doit cependant pas être considérée chez les patients sous traitement prophylactique contre la PBS, dans des zones où il y a une forte prévalence en bactéries résistantes aux quinolones, ou de PBS due à des infections nosocomiales (Niveau B1). L'antibiogramme permettra d'ajuster ultérieurement le traitement antibiotique.
- La PBS est résolutive sous l’effet des antibiotiques chez environ 90 % des patients. La résolution de la PBS doit être prouvée en démontrant une diminution du compte de neutrophiles dans le liquide d’ascite < 250/mm3 et des cultures du liquide d’ascite stériles, si elle était positive au moment du diagnostic (Niveau A1). L'efficacité de l'antibiothérapie est contrôlée par nouvelle ponction exploratrice après 48 heures de traitement.
- Un échec des antibiotiques doit être suspecté en cas d’aggravation des signes cliniques et des symptômes et/ou sans diminution marquée ou d’augmentation du compte de neutrophiles dans le liquide d’ascite, par rapport aux comptes effectués au moment du diagnostic. Un tel échec est habituellement dû à des bactéries résistantes ou à une péritonite bactérienne secondaire. Une fois que la péritonite bactérienne secondaire est exclue, il faut changer les anti- biotiques en tenant compte de la susceptibilité in-vitro d’organismes isolés, ou passer à des agents empiriques à large spectre (Niveau A1).
- surveillance de l'état circulatoire et de l'état de conscience pour dépister précocement les signes d'un choc septique ou d'une encéphalopathie ;
-
Un SHR se développe chez environ 30 % des patients avec PBS traités par antibiotiques seuls, et est associé à une faible survie. L’administration d’albumine (1,5 g/ kg au diagnostic et 1g/kg au jour 3) diminue la fréquence du SHR et améliore la survie (Niveau A1).
-
Tous les patients avec une PBS sont traités avec des antibiotiques à large spectre et de l’albumine en intraveineuse (Niveau A2).
Une suspicion d’ILA nécessite une prise en charge hospitalière et la mise en place d’une antibiothérapie probabiliste.
Après un premier épisode, une antibioprophylaxie secondaire est nécessaire. Le déremboursement récent de la norfloxacine a conduit à de nouvelles recommandations en faveur de la ciprofloxacine 500 mg/j, du cotrimoxazole ou de la rifaximine, lorsque le patient a un antécédent d’encéphalopathie hépatique.
Une prophylaxie primaire de l’ILA est également justifiée chez les patients ayant une cirrhose avec Child C et liquide d’ascite pauvre en protides (< 15 g/L). elle est stoppée dès que l’ascite disparaît.
- Infection secondaire du liquide d'ascite (rare) par diffusion d'un foyer infectieux intra-abdominal ou par perforation d'un organe creux.
C) Autres
- Ascite réfractaire (cf. Cirrhose).
- Syndrome hépatorénal (cf. Cirrhose).
PRISE EN CHARGE THÉRAPEUTIQUE
Vu le lien entre réduction de la survie et développement d’ascite de stade 2 ou 3, chez les patients cirrhotiques, une greffe hépatique doit être envisagée comme une option thérapeutique potentielle (Niveau B1).
PRÉVENTION
Votre texte ici
SURVEILLANCE
Votre texte ici
CAS PARTICULIERS
Votre texte ici
THÉRAPIES FUTURES
Votre texte ici
`
