État de mal épileptique (EME)

INTRODUCTION/GÉNÉRALITÉ
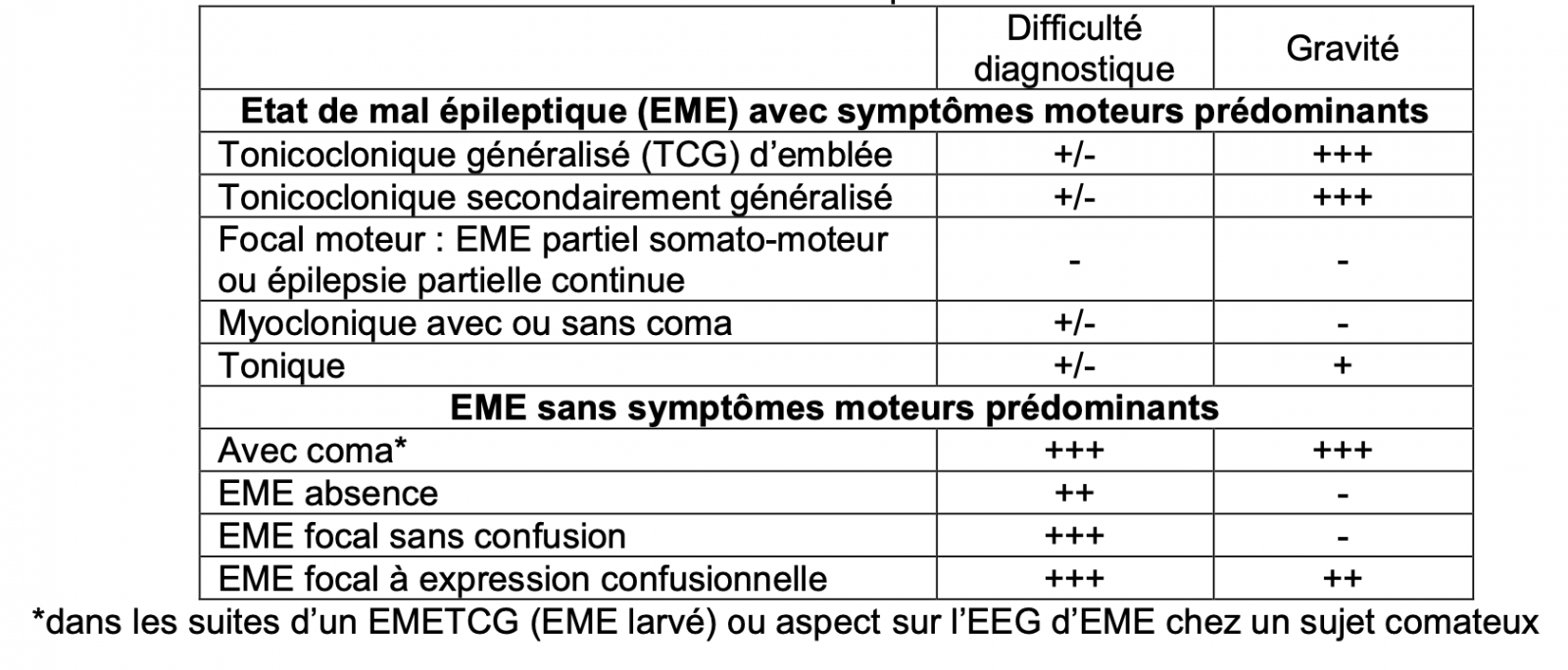
Les EME peuvent être classés selon deux critères cliniques : 1
- Prédominance ou non de manifestations motrices
- Altération ou non de la conscience
A) L’état de mal épileptique tonico-clinique généralisé (EMETCG) :
- Il est défini de façon opérationnelle par une crise généralisée dont les manifestations motrices se prolongent au-delà de cinq minutes ou par des crises (≥ 2) qui se répètent à des intervalles brefs sans reprise de conscience intercritique (non réponse à des ordres simples).1 1 1
- L’EMETCG doit être distingué des crises TCG en série entre lesquelles on constate une reprise de conscience, définie comme la capacité à répondre à des ordres simples. Cette situation constitue une menace d’EMETCG.
- Dans le cadre de l’EMETCG, la persistance isolée d’un coma ou de crises avec reprise de conscience après deux lignes de traitement ne suffit pas au diagnostic d’EME réfractaire.
B) Les EME se présentent aussi sous des aspects moins inquiétants (EME partiels moteurs...), ou trompeurs, sans manifestations cliniques convulsives (aphasiques, visuels...).
- Les EME focaux (moteurs ou non) avec troubles de conscience sont définis de façon opérationnelle par une crise qui se prolonge au-delà de 10 minutes ou par des crises qui se répètent (≥ 2) à des intervalles brefs sans reprise de conscience intercritique.
- Les EME focaux (moteurs ou non) sans altération de conscience peuvent être définis comme une crise qui se prolonge au-delà de 10 à 15 minutes.
- Un EME absence se définit de façon opérationnelle par une crise qui se prolonge au-delà de 10 à 15 minutes.
- Les EME myocloniques, cloniques et toniques, souvent récidivants, constatés la plupart du temps dans le cadre d’encéphalopathies épileptiques ayant débuté dans l’enfance, peuvent être définis comme une crise qui se prolonge au-delà de 10 à 15 minutes.
-
L’EME réfractaire est défini par la persistance de l’EME clinique ou électrique malgré deux lignes thérapeutiques différentes et bien conduites de médicaments antiépileptiques recommandés (posologies optimales et délais d’action).1 1 Le caractère réfractaire de l'EMETCG ne se définit en aucune façon par le recours à des agents anesthésiques prescrits :
-
dans le cadre d’une intubation pour détresse respiratoire
- en raison de la cause du coma (traumatisme crânien grave...)
- pour faciliter le transport en extrahospitalier
-
- L’EMETCG super-réfractaire est défini par un EME persistant ou récidivant après 24 heures d’un coma thérapeutique bien conduit.1
- L’EMETCG larvé, rare, est l’expression clinique très tardive d’un EMETCG non ou insuffisamment traité. Son diagnostic repose sur l’EEG.1 Un aspect EEG d’EME peut se rencontrer chez un patient dans le coma dans des contextes cliniques divers dont l’analyse doit être rigoureuse car impliquant des prises en charge parfois très différentes en particulier en ce qui concerne l’opportunité et l’intensité du traitement.
HISTORIQUE
Votre texte ici
PHYSIOPATHOLOGIE
Votre texte ici
ÉPIDÉMIOLOGIE
- Il s’agit d’une urgence médicale.
- L’incidence des états de mal épileptiques, difficile à estimer, serait de l’ordre de 6 à 40 nouveaux patients pour 100 000 individus par an.1
- Environ la moitié des états de mal épileptiques surviennent chez des patients souffrant d’épilepsie connue.
- Une autre moitié des EME sont inauguraux et dits « de novo » 1 soit le plus souvent dans le cadre d’une atteinte structurelle ou fonctionnelle cérébrale aiguë, soit en tant que première manifestation d’une maladie épileptique en particulier consécutive à des séquelles de lésions anciennes (traumatiques, vasculaires...).
- L’EME tonico-clonique généralisé (EMETCG) en est l’expression la plus connue et la plus spectaculaire.
FACTEURS DE RISQUES
Votre texte ici
EXAMEN CLINIQUE
Votre texte ici
EXAMENS COMPLÉMENTAIRES
A) Biologie
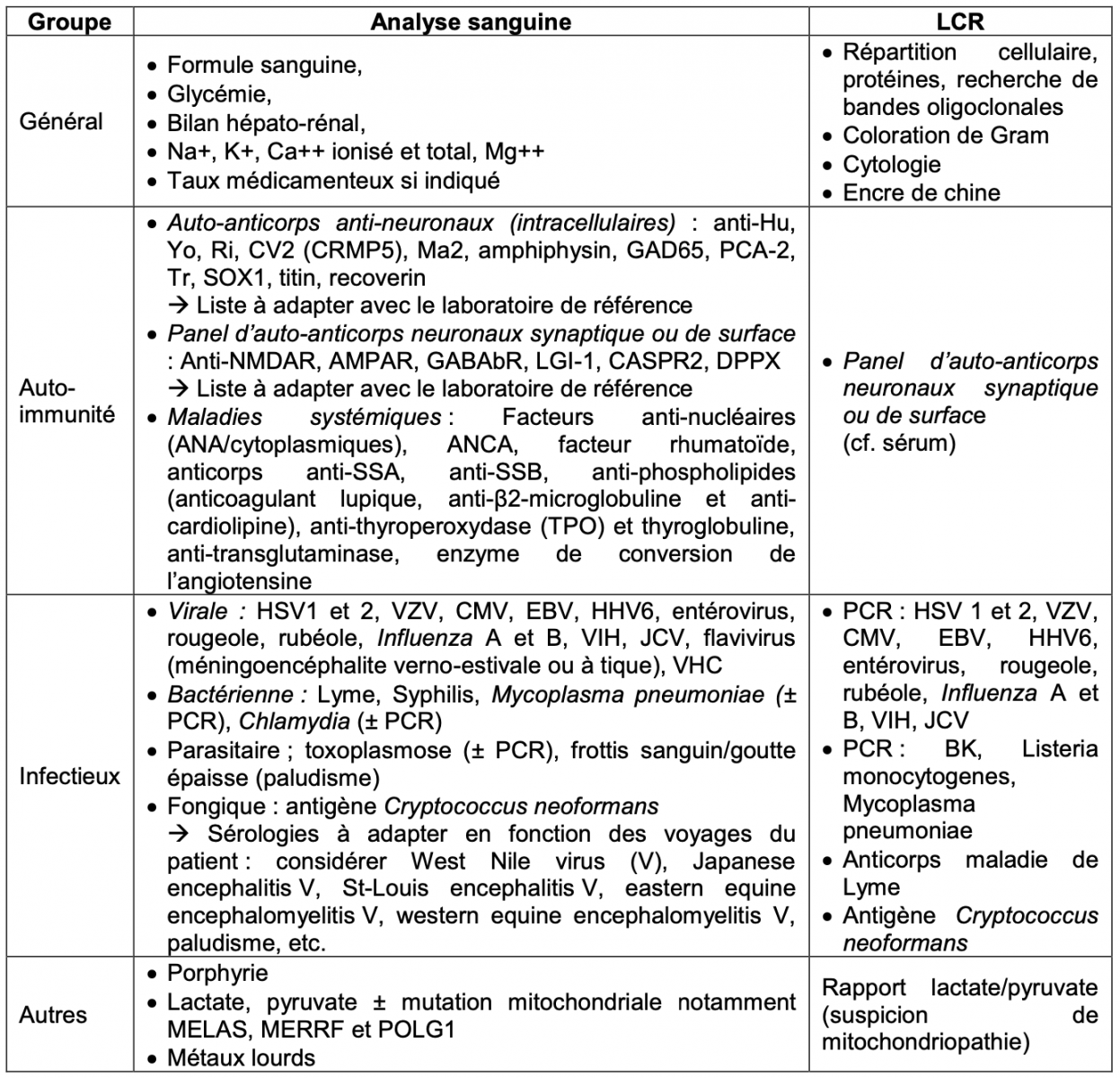
- Les examens biologiques suivants, dans le strict cadre du bilan étiologique, doivent être obtenus dès que possible : glycémie, natrémie, calcémie ionisée ou totale, magnésémie, dosage des antiépileptiques. Selon le contexte, d’autres dosages et une PL peuvent être indiqués.1 1
B) Imagerie cérébrale
- En cas d’EME inaugural la réalisation en urgence d’une imagerie cérébrale (imagerie par résonnance magnétique ou IRM12), à défaut scanner sans et avec injection et comportant des séquences veineuses), dès que l’état du patient est stabilisé, est presque toujours nécessaire, et indispensable si une PL est indiquée.
- Chez le patient souffrant d’épilepsie les indications d’une imagerie en urgence sont larges : traumatisme crânien, premier épisode d’EMETCG, pathologie cérébrale connue susceptible de s’être modifiée, troubles de vigilance, confusion ou céphalées, syndrome méningé, modifications de l’examen neurologique (déficit récent, etc.), état fébrile inexpliqué, antécédents néoplasiques, terrain immunodéprimé...
- L’imagerie cérébrale si elle est indiquée en urgence doit être effectuée dès que possible, éventuellement par le SAMU avant le transfert en réanimation/USC.
- L’IRM doit être privilégiée chaque fois que possible car elle est plus sensible pour établir le diagnostic de certaines étiologies citées ci-dessus.1 Par ailleurs, dans certains cas, elle peut apporter des éléments physiopathologiques tels que la mise en évidence d’une souffrance neuronale per- ou postcritique.1 Il s’agit alors le plus souvent d’hyper-signaux corticaux unilatéraux (notamment del’hippocampe), de la substance blanche adjacente, des ganglions de la base, du thalamus (pulvinar), du corps calleux et du cervelet, visibles en pondération T2 ou Flair, témoignant d’un œdème vasogénique et parfois cytotoxique.1
- L’imagerie peut cependant être différée voire jugée non nécessaire si l’état clinique est strictement revenu à l’état antérieur, si :
- le diagnostic étiologique ne fait aucun doute (cause métabolique indiscutable et EME d’emblée généralisé),
- la cause déclenchante de l’EME est claire chez un patient souffrant d’épilepsie,
- les données de l’imagerie n’ont aucune incidence thérapeutique.
C) Ponction lombaire
- En cas de forte présomption de méningo-encéphalite ou de méningite infectieuse un traitement anti-infectieux probabiliste est immédiatement mis en route. Une PL sera réalisée en urgence, après l’imagerie et en l’absence d’autre contre- indication, chez tous les patients suspects d’infection du SNC ou immunodéprimés.
Une PL doit être effectuée si aucune étiologie de l’EME n’est clairement identifiée après une première évaluation (clinique, biologie et imagerie). La PL doit être répétée en cas de :
- Encéphalite suspectée, le LCR pouvant être normal à la phase très précoce : les infections du SNC expliquent 3 à 6% des EME de novo.1 Leur prise en charge thérapeutique est une urgence justifiant la réalisation d’une PL dans la prise en charge initiale au moindre doute diagnostique. L’absence d’anomalies du LCR, a fortiori lorsque la PL a été réalisée précocement, n’exclut pas formellement une encéphalite infectieuse (HSV-1 par exemple),1 notamment chez l’immunodéprimé, ou d’autres causes (néoplasique, paranéoplasique, dysimmunitaire).1 1
- Pléiocytose isolée modérée (< 25 éléments/μL) constatée sur la première PL : L'interprétation des résultats cytologiques et biologiques de l'analyse du LCR peut être sujette à débat, notamment en présence d’une pléïocytose modérée. En effet, des modifications cytologiques (pléïocytose) et biologiques (augmentation de la concentration du lactate et du quotient albumine LCR/ sérum) du LCR sont parfois décrites en phase post critique en l’absence de toute pathologie infectieuse ou vasculaire. Néanmoins, cette pléïocytose reste alors modérée (< 25 éléments/μl), peu fréquente (6% des patients), précoce (< 24 heures), elle n'est influencée ni par la durée ni par le type de crise. Son interprétation doit de toute façon rester prudente pour ne pas méconnaître une infection débutante.1
- Recherche étiologique : auto-immune, néoplasique... :1 1 Les pathologies dysimmunitaires ou paranéoplasiques représentent un pourcentage plus confidentiel de causes d’EME,1 mais doivent néanmoins être rapidement évoquées lorsque le bilan initial reste non contributif.1
D) Electroencéphalogramme
1) Devant un état de mal épiléptique tonico- clonique convulsif généralisé
- Tout établissement de santé susceptible de prendre en charge des patients en EME devrait disposer d’un accès rapide à un EEG dans les plus brefs délais.
L’EEG doit être effectué chaque fois que possible en urgence :
- S’il n’y a pas d’amélioration de la vigilance lorsque les convulsions cessent :
- L’EEG n’est pas nécessaire à la phase convulsive d’un EME généralisé convulsif. En revanche, il doit être réalisé rapidement après la phase convulsive dans le but de s’assurer de l’absence de crises résiduelles ou d’EME non convulsif (après un EMETCG avec récupération de la vigilance, un EEG standard de 20 minutes au minimum doit être réalisé rapidement)
- Dans ce but, il doit être effectué en urgence s’il n’y a pas d’amélioration progressive de la vigilance. En effet, la persistance d’un EME non convulsif après l’arrêt des convulsions a été rapporté comme doublant la mortalité 1 et cet état justifie donc l’intensification du traitement. Le retard de diagnostic des EME non convulsifs augmente la mortalité.1
- En cas de doute diagnostique avec une encéphalopathie ou des manifestations psychogènes non épileptiques : dans certains cas, l’EEG peut montrer des aspects évocateurs d’encéphalopathie (métabolique, toxique, post-anoxique ...) orientant le diagnostic étiologique.
- En cas de suspicion d’EME larvé ou d’EME réfractaire :1 1 la possible évolution d’un EME clinique vers un EME larvé justifie à elle seule le recours à l’EEG systématique en urgence chez tout EMETCG dont l’état de vigilance ne s’améliore pas progressivement dans l’heure qui suit l’arrêt des convulsions.1
- Chez un patient dans le coma et en EME, l’activité épileptique est définie par la présence d’activités rythmiques, non réactives aux stimulations, avec souvent une organisation spatio-temporelle, de façon continue ou se répétant sans retour à l’activité de fond. Des critères précis récents (dits de Salzburg) peuvent aider à qualifier ces tracés.
- L’EEG peut apporter des arguments en faveur de certaines causes d’EME (encéphalite herpétique, encéphalite à anticorps anti-récepteurs NMDA) et reflète le niveau de sédation.
- L’EEG avec enregistrement vidéo et EMG permet de confirmer le caractère psychogène non épileptique des symptômes notamment s’il est normal en dehors des manifestations motrices. Pendant celles-ci, les artéfacts rendent l’interprétation du tracé délicate.
- La collaboration entre réanimateurs et neurophysiologistes doit être fortement encouragée, au mieux 24 heures sur 24 heures, compte tenu de la difficulté d’interprétation correcte de l’EEG en réanimation. Il faut notamment éviter de diagnostiquer à tort comme EME des tracés EEG d’encéphalopathie.
Un EEG prolongé, dans l’idéal continu d’au moins 24 heures, doit être ensuite entrepris dans la mesure du possible :
- Pour le suivi thérapeutique de l’EMETCG réfractaire
- Si les troubles de vigilance persistent plus d’une heure après l’arrêt des convulsions (hors sédation)
- En cas de constatation d’un tracé EEG d’EME
- En cas de survenue de nouvelles crises
- Un monitoring EEG continu sur scope comportant peu de dérivations (quatre minimum, au mieux neuf électrodes - quatre de chaque côté et une électrode centrale médiane), peut être utilisé dans la surveillance d’un EME généralisé si un enregistrement par EEG continu n’est pas disponible. Il ne dispense en aucun cas de la réalisation d’un enregistrement EEG standard car il ne fournit que des informations parcellaires.1
- L'index bispectral (BIS) ne doit pas être utilisé pour guider le traitement d’un EME.
2) Dans les autres états de mal épileptiques
- Un EEG sera effectué le plus tôt possible devant un syndrome confusionnel d’étiologie non évidente ou qui persiste après une crise d’épilepsie afin d’éliminer un EME généralisé ou focal non convulsif à expression confusionnelle.
- Un EEG est indiqué devant des manifestations neurologiques centrales très diverses de début brusque dont l’origine n’apparaît pas clairement ou dont l’étiologie est susceptible de se compliquer d’un EME.
- L’EEG, indispensable au diagnostic d’EME non convulsif, montre des activités paroxystiques rythmiques non réactives aux différentes stimulations. Dans les EME généralisés, ces activités sont bilatérales et prédominent souvent en antérieur. Dans les EME focaux, ces activités sont focales, ou asymétriques, ou plus ou moins diffuses. Il existe des critères (Salzbourg) qui aident au diagnostic EEG.
- Dans l’EME généralisé non convulsif (EME absence), l’EEG devra être effectué au plus tôt pour affirmer le diagnostic. En cas d’impossibilité de réalisation rapide, une injection de BZD peut être effectuée avant l’obtention de l’EEG à la recherche d’une amélioration clinique.
-
Pour les EME absence ou focaux à expression confusionnelle, la normalisation du tracé quelques secondes ou minutes après l'injection IV d'une BZD affirme le diagnostic d’EME non convulsif si elle s'accompagne d’une nette amélioration de la symptomatologie confusionnelle. La négativité de ce test n’élimine pas le diagnostic.
-
Le recours à un monitoring vidéo-EEG continu est à considérer dans les EME
réfractaires notamment à expression confusionnelle.
-
Le recours à un monitoring vidéo-EEG continu est à considérer dans la surveillance de certaines encéphalopathies et encéphalites, pour y rechercher
d’authentiques crises voire un EME.
E) Bilan approfondi
Devant un EME réfractaire et a fortiori super-réfractaire inaugural « de novo » qui reste inexpliqué un bilan approfondi sera réalisé très rapidement, à la recherche notamment d’une cause dysimmunitaire, paranéoplasique ou non, ou infectieuse.
DIAGNOSTICS DIFFÉRENTIELS
A) De l'état de mal épiléptique tonico- clonique convulsif généralisé
1) Les crises tonico-cloniques généralisées en série
- Elles n’entrent pas dans le cadre des EME mais peuvent évoluer vers un EMETCG.
- La prise en charge de cette menace d’EMETCG revêt le même degré d’urgence, recourant aux benzodiazépines et si besoin à un ou plusieurs antiépileptiques de deuxième ligne.
2) Un coma post EMETCG avéré
- sans manifestations motrices peut être consécutif à la cause de l’EME, à l’expression d’un EME que l’on ne peut authentifier que sur l’EEG, au caractère sédatif des médicaments administrés. Cette situation justifie un EEG en urgence.
- accompagné de manifestations motrices discrètes évoquant un EME larvé impose un EEG en urgence.
3) Manifestations psychogènes non épileptiques :
- La possibilité de manifestations psychogènes non épileptiques doit être systématiquement évoquée devant tout EMETCG tout au long de sa prise en charge.
-
Les crises psychogènes non épileptiques sont définies comme des manifestations paroxystiques du comportement moteur et de la conscience faisant évoquer en premier lieu une crise épileptique.
-
Elles comportent des atypies incompatibles avec l’anatomie et la physiologie, sans modification concomitante de l’électrogenèse.
-
Elles surviennent en général chez l’adolescent ou l’adulte jeune, mais peuvent survenir chez l’enfant.1 1 1
-
Ces crises comportent des manifestations motrices spectaculaires, pouvant concerner les quatre membres et se prolonger plusieurs minutes, désordonnées, rythmées ou reptatoires avec parfois opisthotonos.
-
Ces mouvements peuvent être facilités ou déclenchés par la suggestion.
-
Il existe une polypnée sans cyanose.
-
Les yeux restent fermés avec parfois résistance lors des tentatives pour soulever les paupières et fuite des globes oculaires vers le haut.1
-
Il n’est pas rare de constater des pleurs post critiques.
-
Ces crises ne sont pas stéréotypées.
-
-
L’EEG normal ou surchargé d’artéfacts myographiques et dépourvu d’anomalies paroxystiques permet d’affirmer le diagnostic.
-
On retrouve souvent la notion d’hospitalisations multiples avec EEG normal.
-
Ces états de mal non épileptiques ne répondent pas aux traitements épileptiques et risquent d’être étiquetés EME réfractaires entrainant une escalade thérapeutique délétère.1 1 1 1 1
-
Des intrications avec d’authentiques crises épileptiques (10 à 20% des patients) sont possibles.1
4) Autres diagnostics différentiel
- Dans le cadre de l’encéphalopathie anoxo-ischémique, les myoclonies constatées sont parfois d’origine épileptique et rarement l’expression d’un EME.1
- Les myoclonies avec ou sans trouble de la vigilance des encéphalopathies toxiques et métaboliques (insuffisance rénale, insuffisance hépatique, etc) ne sont pas la plupart du temps de nature épileptique. L’EEG montre souvent un tracé d’encéphalopathie, comportant typiquement des ondes triphasiques, et peut poser des problèmes diagnostiques avec un EME.1 1 1
- L’analyse sémiologique attentive, le contexte et parfois l’EEG permettront d’éliminer les mouvements anormaux associés aux encéphalites à anticorps anti- récepteurs NMDA, les myoclonies de la maladie de Creutzfeldt-Jakob, les mouvements observés dans certains AVC du tronc basilaire, des accès d’hypertonie, des syncopes itératives avec myoclonies, les frissons...1 1 1
- L’EEG peut montrer des aspects qui peuvent faire porter à tort le diagnostic d’EME chez un patient cérébrolésé qui se trouve dans un coma non précédé de convulsions.
B) Des autres états de mal épileptiques
- Devant un EME partiel moteur, myoclonique, tonique, il convient d’éliminer :
- des tremblements, myoclonies, chorées, dystonies, dyskinésies, spasmes musculaires ou pyramidaux; les myoclonies non-épileptiques peuvent notamment survenir dans le cadre d’encéphalopathies (métaboliques, post- anoxiques, médicamenteuses, toxiques) ou d’encéphalites (anticorps anti-récepteurs NMDA) ;
- des mouvements psychogènes et même de simples frissons.
- De nombreux mouvements non épileptiques peuvent être supprimés ou atténués par des BZD ou d’autres antiépileptiques.
-
Devant un EME sans manifestation motrice prédominante, à expression confusionnelle ou non, la symptomatologie variée (auditive, visuelle, dysesthésique, aphasique, olfactive, gustative, psychique, végétative, comportementale avec ou sans automatismes...) peut amener à discuter de nombreux diagnostics, notamment migraines, accident ischémique transitoire, troubles psychiatriques.
-
L’analyse sémiologique, la vidéo-EEG et l’IRM cérébrale apporteront des arguments en faveur d’une origine épileptique.
ÉTIOLOGIE
- La cause de l’EME doit être identifiée et si elle est curable, traitée le plus tôt possible dans l’espoir de faciliter le contrôle de l’EME et le cas échéant d’améliorer le pronostic du patient.
- L’enquête étiologique est guidée par l’anamnèse, l'existence ou non d’antécédents d’épilepsie, le caractère focal ou généralisé (d’emblée ou secondairement) des crises, l’examen clinique complet en particulier neurologique, des examens biologiques, l’EEG, l’imagerie et éventuellement une ponction lombaire (PL). Un EME peut répondre à plusieurs étiologies.
A) Chez un épileptique connu
En cas d’EME survenant chez un patient souffrant d’épilepsie, et en dehors d’une suspicion de pathologie cérébrale aiguë surajoutée, les étiologies principales à évoquer systématiquement sont :
- l’arrêt ou l’inadaptation du traitement de fond
- un trouble métabolique aigu
- une infection hors système nerveux central (SNC)
- un sevrage ou une intoxication énolique ou par psychotropes
- une intoxication aiguë par des médicaments ou substances épileptogènes
- une évolution de l’éventuelle pathologie sous-jacente.
B) EME inaugural ou de novo
- En cas d’EME inaugural ou de novo, avec ou sans atteinte cérébrale préexistante connue, il faut éliminer une atteinte cérébrale structurelle aiguë évolutive curable vasculaire, infectieuse, traumatique, tumorale, inflammatoire, sans omettre de rechercher et traiter une cause métabolique, toxique ou médicamenteuse.
C) Chez l'enfant
- Chez l’enfant et l’adolescent, un sevrage ou une intoxication alcoolique ou aux psychotropes sont exceptionnels. Un épisode infectieux, en particulier fébrile, peut entraîner chez ces patients souffrant d’épilepsie des crises plus longues qu’habituellement et dans de rares cas un véritable EME.1
- Chez l’enfant, un EME inaugural peut être observé dans le cas de convulsions fébriles se prolongeant suffisamment pour évoluer vers un EME.
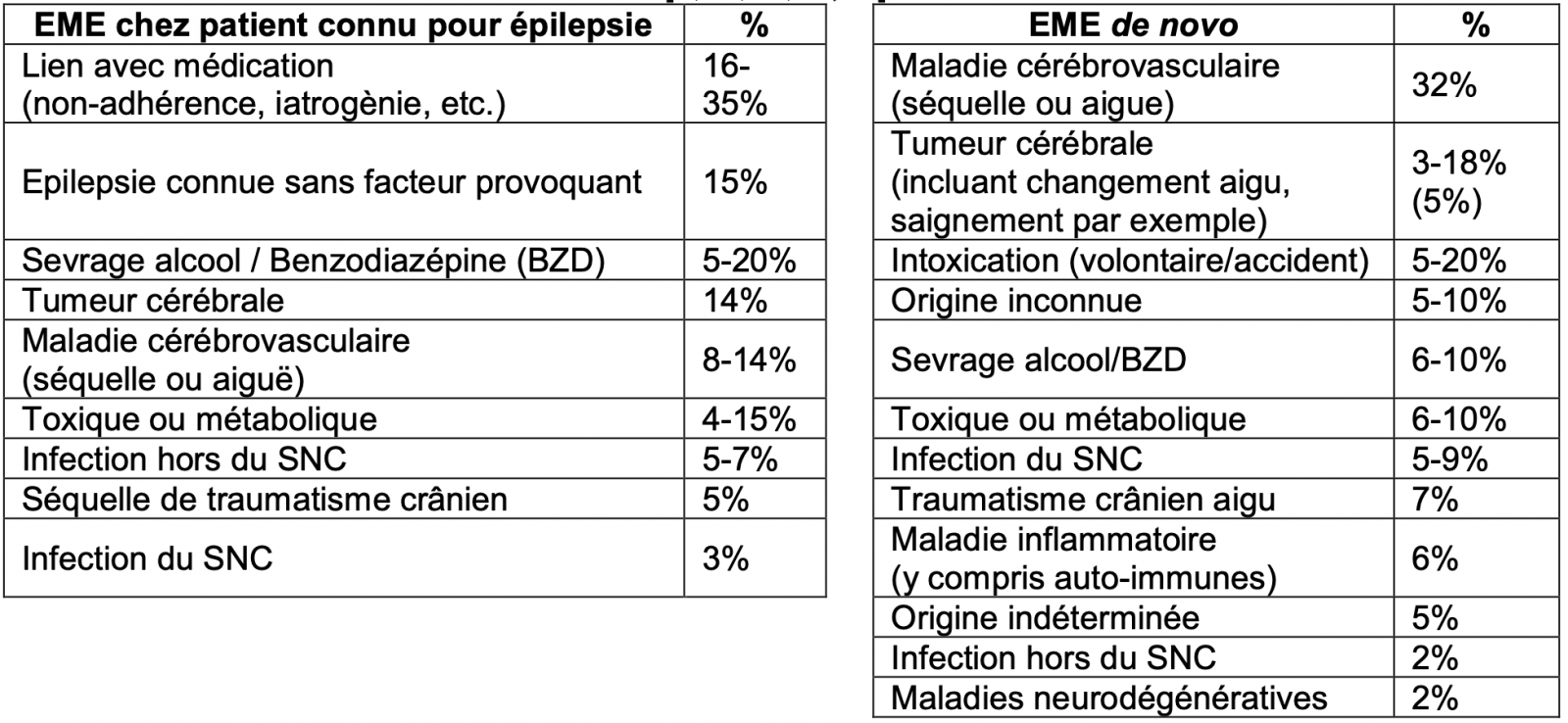
Etiologies les plus fréquentes des états de mal épileptique (EME) de l’adulte : 1 1 1 1 1
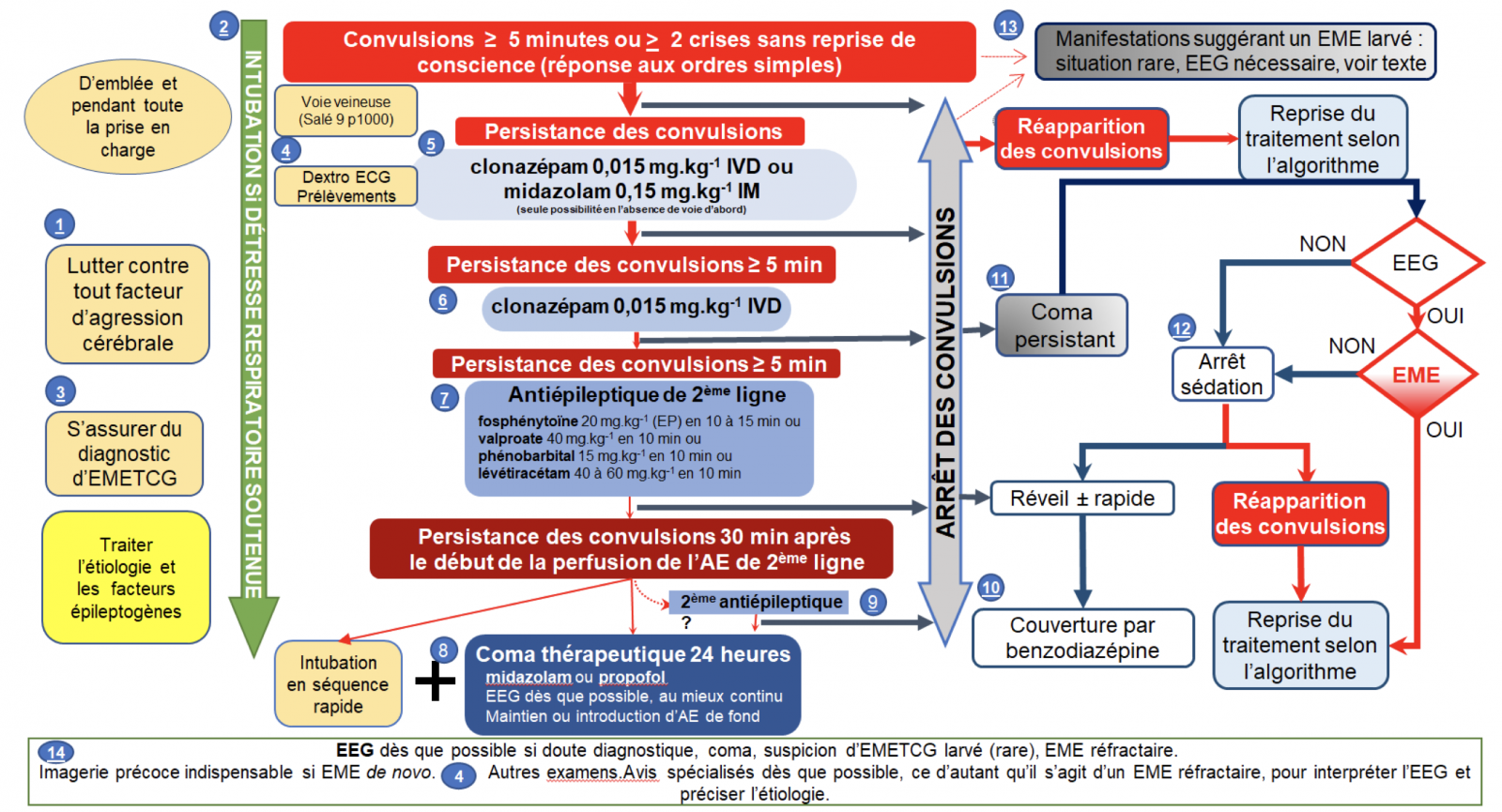
PRISE EN CHARGE THÉRAPEUTIQUE de l'EMETCG
A) Prise en charge non spécifique
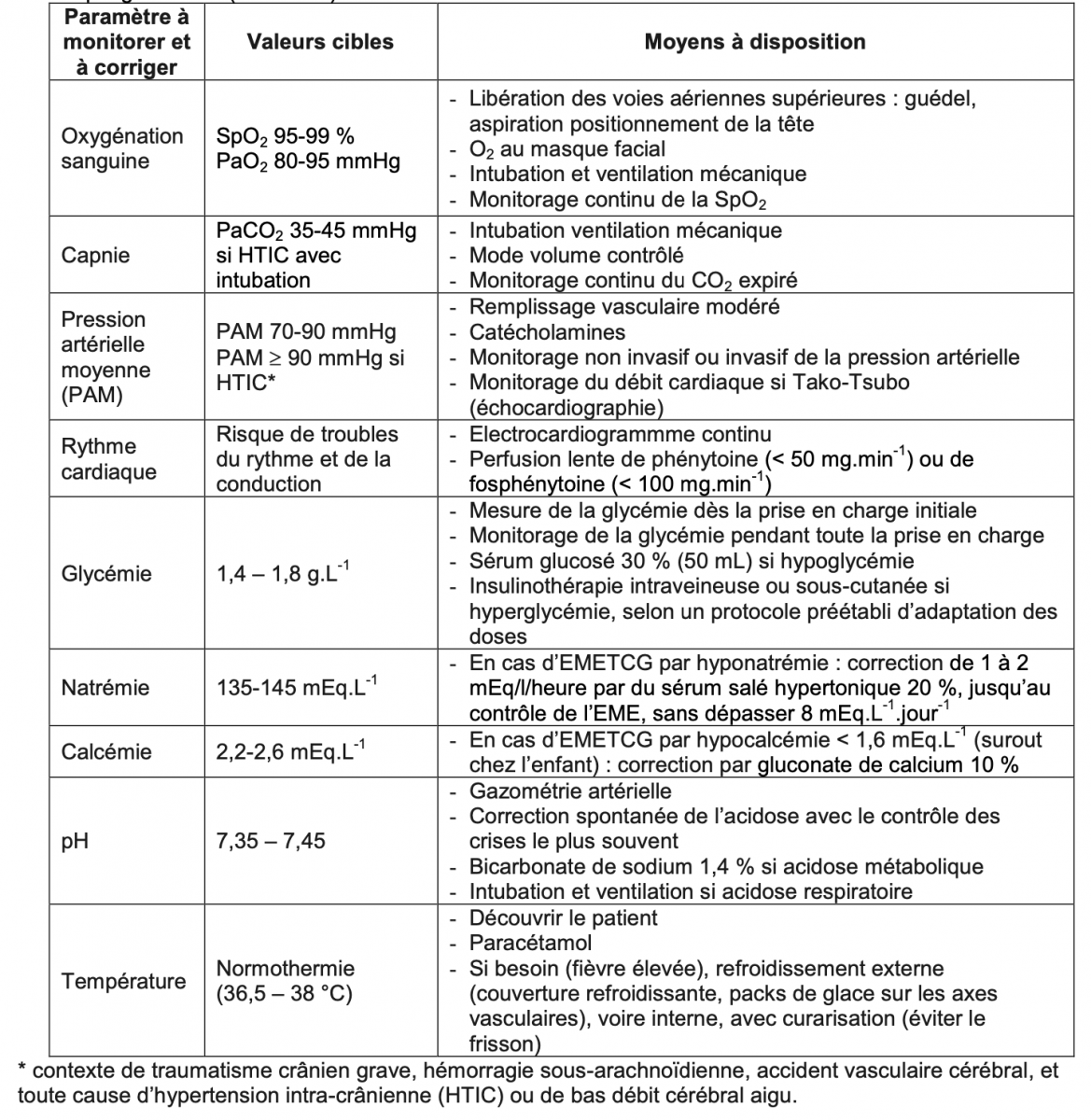
1) Paramètres systémiques à monitorer et à corriger lors d’un état de mal épileptique tonico- clonique généralisé (EMETCG) de l’adulte.
- Dès la phase préhospitalière de prise en charge d’un patient en EMETCG, il est nécessaire de prévenir et de lutter contre les facteurs d’agression cérébrale : hypotension artérielle, hypocapnie, hypoxémie, hypoglycémie, hyponatrémie, hyperthermie, hypocalcémie, hyperoxie, hypercapnie franche, certaines hypertensions artérielles, troubles du rythme et de la conduction, hyperglycémie.1
- Dans ce contexte, le soluté de base conseillé chez l’adulte est le sérum salé à 0,9% et chez l’enfant un soluté sucré isotonique avec adjonction d’ions.
- L’administration de 100 à 500 mg de thiamine s’impose au moindre doute de carence en vitamine B1 (éthylisme, dénutrition, femme enceinte, etc.) en particulier si une perfusion de sérum glucosé hypertonique est nécessaire pour la correction d’une hypoglycémie.
2) Indications et non d’indication de l’intubation trachéale :
- Il ne semble pas justifié d’intuber un patient présentant un coma persistant après l’arrêt des crises tant que la tolérance respiratoire est bonne et qu’il n’y a pas d’argument pour une agression cérébrale aiguë (traumatisme crânien grave, etc.).
- L’intubation d’un patient en EMETCG n’est indiquée qu’en cas de détresse respiratoire soutenue (au-delà des quelques minutes de respiration stertoreuse postcritique) et en cas d’échec (persistance des convulsions) des traitements de première et de deuxième ligne bien conduits. L’étiologie de l’EME peut imposer en elle- même une intubation : traumatisme crânien grave, hémorragie sous arachnoïdienne, HTIC sévère.1

B) Prise en charge spécifique
1) Traitement par BZD
- Il faut utiliser des BZD comme traitement de première ligne.1
- Il faut probablement utiliser en IV direct 0,015 mg/kg de clonazépam (soit 1 mg pour 70 kg ; maximum 1,5 mg) ou en intra-musculaire (IM) 0,15 mg/kg de midazolam (soit 10 mg pour 70 kg).1 1
- Chez l’adulte, en l’absence de voie d’abord veineuse rapidement disponible, il faut recourir au midazolam IM (0,15 mg/kg soit 10 mg IM pour un adulte de 70 kg).1
- Chez l’enfant en l’absence de voie IV rapidement disponible, il est conseillé d’administrer par voie rectale (IR) 0,5 mg/kg de diazépam (maximum 10 mg) ou par voie buccale (VB) 0,3 mg/kg de midazolam (maximum 10 mg).1
- Il faut probablement répéter l’injection de la BZD, à l’exception du midazolam, en cas de persistance clinique de l'EMETCG cinq minutes après la première injection. Si l’état respiratoire s’est dégradé, il est prudent de n’administrer qu’une demi-dose.1 1 1 1 1
2) Traitement antiépileptique
- En cas de persistance clinique de l'EMETCG cinq minutes après la deuxième injection de BZD il faut administrer en IV un autre médicament antiépileptique en deuxième ligne.1
On peut utiliser chez l’adulte (selon le terrain, les éventuels traitements antiépileptiques antérieurs, l’étiologie, les habitudes des prescripteurs) soit :1
- Valproate de sodium : 40 mg/kg en 15 minutes, sans dépasser 3 g (préférer un autre traitement de deuxième ligne chez les femmes en âge de procréer)
- Fosphénytoïne à la dose de 20 mg/kg en dose équivalent phénytoïne, à un débit maximum de 100 à 150 mg/min, ou phénytoïne à la dose de 20 mg/kg à un débit maximum de 50 mg/min (si âge > 65 ans : 15 mg/kg et débit réduit), sous scope, contre-indiqué en cas de troubles du rythme et de la conduction et à manier prudemment en cas d’antécédents cardiaques.
- Phénobarbital : 15 mg/kg, débit de à 50 à 100 mg/min, plus sédatif
- Lévétiracétam : 30 à 60 mg/kg en 10 minutes, sans dépasser 4 g.
Toute la dose prescrite de ces antiépileptiques doit être administrée, même si les convulsions s’arrêtent pendant l’injection.
Chez l’enfant il existe deux particularités :
- Le valproate de sodium est peu utilisé et doit même être évité lorsque la cause de l’EME n’est pas connue, pouvant aggraver une maladie innée du métabolisme sous-jacent ;
- Avant cinq ans la pharmacocinétique de la fosphénytoïne n’est pas connue, on utilise donc de préférence la phénytoïne.
Si l’EMETCG est contrôlé, le patient étant réveillé, et si la cause n’est pas immédiatement réversible, un traitement antiépileptique de relais doit être débuté dès que possible, initialement associé à une BZD (clonazépam, clobazam).
C) Orientation – filière
- L’hospitalisation en réanimation ou en unité de soins continus (USC) est indiquée en cas de persistance clinique de l’EMETCG, d’altération de la vigilance, pour la prise en charge de certaines étiologies, ou en cas de défaillance d’organe associée (notamment si le patient est ventilé).
- Il est possible d’adresser le patient aux urgences en cas d’amélioration rapide de l’état de conscience et en l’absence de défaillance d’organe associée.
- En cas de crises tonico-cloniques généralisées en série, l’hospitalisation en réanimation/USC est indiquée si les crises persistent malgré l’administration de benzodiazépines et d’un ou plusieurs traitements de deuxième ligne, si une autre défaillance d’organe apparaît ou si l’état de conscience inter-critique se dégrade.1 1
- Le transfert en neurologie est à privilégier dans tous les cas, au décours de la prise en charge. Quand cela est impossible, le patient devra être transféré en médecine. Une consultation neurologique de suivi sera systématiquement programmée.
D) EMETCG réfractaire et super-réfractaire
- Si les convulsions persistent trente minutes après le début de l’administration du traitement de deuxième ligne, on se trouve devant un EMETCG réfractaire. Il faut alors probablement chez l’adulte, après intubation trachéale sous anesthésie en séquence rapide, recourir en troisième ligne à un coma thérapeutique au moyen d’un agent anesthésique IV.
- Chez l’adulte il est possible, à ce stade d’EMETCG réfractaire, de différer le recours à l’anesthésie générale, (aux risques indéniables et à la supériorité non démontrée), en administrant un autre antiépileptique de deuxième ligne, si l’EME évolue depuis moins de 60 minutes et s’il s’agit d’un patient avec épilepsie connue ne présentant pas de facteur d’agression cérébrale manifeste. Cette attitude est recommandée lorsque le recours à la ventilation mécanique est déraisonnable (limitation des thérapeutiques autres que de confort).
- Chez l’enfant, en cas d’EMETCG réfractaire, le recours à un autre antiépileptique de deuxième ligne avant les anesthésiques généraux est la pratique la plus habituelle.
- Lors d’un traitement par agents anesthésiques, il faut probablement chercher à obtenir sur l’EEG une suppression des crises voire un tracé de « burst-suppression » pendant au moins 24 heures, puis réduire progressivement les anesthésiques généraux sur environ 6 heures sous contrôle EEG.
- Lors d’un EMETCG super-réfractaire, les agents anesthésiques utilisés en première intention (midazolam ou propofol) sont repris. En cas de contrôle de l’EME vérifié par l’EEG, au mieux continu, il est conseillé de poursuivre le traitement plus de 24 heures, puis d’arrêter progressivement l’anesthésie générale. En cas d’échec d’emblée ou secondairement, il faut probablement recourir à la kétamine (bolus de 1 à 3 mg/kg puis 0,5 à 5 mg/kg/h) couplée à une BZD ou au thiopental. En cas d’échec il faut poursuivre l’anesthésie et discuter le recours à d’autres thérapeutiques : adjonction d’antiépileptiques, régime cétogène, corticothérapie ± immunothérapie.
- Lors d’un EMETCG réfractaire et a fortiori super-réfractaire, le maintien ou l’instauration d’un traitement antiépileptique de fond est dans tous les cas nécessaire.
- Si les manifestations motrices étiquetées EMETCG se sont spontanément arrêtées, il n’y a pas lieu d’injecter un traitement à visée antiépileptique d’emblée, que le patient soit ou non dans le coma.
- Au décours d’un EMETCG traité, la persistance du coma sans convulsions ne doit pas conduire à l’intensification du traitement antiépileptique sans avoir étayé une éventuelle poursuite de l’EME par l’EEG.
- Chez un patient d’emblée dans le coma, la présence de signes cliniques évocateurs d’un EME larvé (à filmer), peut conduire à l’administration de BZD, voire d’un traitement de deuxième ligne en attendant l’EEG.
- À l’arrivée en réanimation d’un patient ventilé et sédaté, s’il n’existe aucune manifestation convulsive et si l’on ne dispose pas rapidement d’un EEG, il est licite sous certaines conditions d’interrompre la sédation pour évaluer le niveau de vigilance, l’état neurologique, et éventuellement extuber le patient.
- L’attitude thérapeutique à tenir devant la découverte d’un tracé EEG d’EME associé au coma n’est pas codifiée. On recourra au mieux à un contrôle EEG continu et successivement aux traitements de première et seconde ligne. Le recours éventuel à des agents anesthésiques devra s’appuyer sur les conseils de spécialistes. La recherche de la cause associée à ce tracé d’EME est primordiale.
PRISE EN CHARGE THÉRAPEUTIQUE DES autres états de mal épileptiques
A) Orientation – filière 1
L’hospitalisation en réanimation/USC d’un patient présentant un EME avec manifestations motrices (EME partiel moteur, myoclonique, tonique) n’est indiquée qu’en présence de troubles de la vigilance (généralisation de l’EME ou troubles de vigilance liée à l’étiologie ou au traitement) ou si une autre défaillance d’organe apparaît.
L’hospitalisation en réanimation/USC d’un patient présentant un EME sans manifestation motrice prédominante, à expression confusionnelle ou non est indiquée, en fonction du terrain :
- si l’option thérapeutique choisie le nécessite (l’administration de (fos)phénytoïne nécessite une surveillance par scope),
- en raison de troubles de la vigilance,
- si l’étiologie sous-jacente laisse entrevoir une possibilité d’aggravation,
- si des crises tonico-cloniques généralisées viennent émailler le tableau clinique,
- si une autre défaillance d’organe apparaît.
Le transfert en neurologie est à privilégier dans tous les cas. Quand cela est impossible, le patient devra être transféré en médecine. La sortie à domicile ou dans une autre structure, après avis neurologique, est fonction de la cause de l’épilepsie, de son degré de contrôle, du terrain, de l’organisation de l’établissement, des éventuelles affections associées. Une consultation neurologique de suivi sera systématiquement programmée.
B) Prise en charge spécifique 1
Il faut probablement utiliser une BZD comme traitement de première ligne. On peut proposer :
- Le clonazépam selon les mêmes modalités que pour l’EMETCG.
- Le midazolam subjugal (Buccolam®: 10 mg pour un adulte facile et rapide à mettre en œuvre par l’entourage.
- Le diazépam (Valium® intra rectal à la dose de 0,3 à 0,5 mg/kg sans dépasser 10 mg) est chez l’enfant une autre possibilité.
- La prise en charge médicamenteuse en seconde ligne est différente de celle de l’EMETCG. Divers traitements antiépileptiques pourront être utilisés, dès que possible, avec le conseil d’un neurologue, sans que ces instaurations thérapeutiques revêtent le caractère d’extrême urgence propre au traitement de l’EMETCG.
- Le délai entre chaque nouvelle ligne de traitement va dépendre du type d’EME, de son retentissement clinique et son profil évolutif, de l’étiologie sous-jacente, du terrain, des traitements antérieurs, de la pharmacocinétique des divers médicaments et du pronostic associé. Contrairement à la prise en charge de l’EME généralisé convulsif qui est une urgence thérapeutique et impose de minimiser le délai entre chaque ligne de traitement, il n’y a pas de données de la littérature dans les autres EME permettant de préconiser l’administration séquentielle codifiée de nouvelles lignes de traitement. Une attitude moins agressive est donc conseillée dans ces états de mal.1
Les médicaments antiépileptiques utilisables chez l’adulte en seconde ligne sont très nombreux, sous réserve de leurs précautions d’emploi :
- Par voie intraveineuse on dispose de : (fos)phénytoïne, valproate de sodium, lévétiracétam, lacosamide, phénobarbital. À la différence des EMETCG, qui nécessitent une perfusion rapide, le débit d’administration des médicaments peut être ralenti et la posologie modulée en fonction du terrain et de la sémiologie des crises.
- Par voie orale ou par sonde gastrique (si le patient présente des troubles de vigilance ou des troubles de la déglutition), en cas de contre-indication des molécules antiépileptiques précédentes, d’absence de voie intraveineuse disponible, ou d’impossibilité de surveillance dans une USC, on peut recourir à une dose de charge en carbamazépine (sauf si le patient est d’origine asiatique, du fait d’un risque accru d’allergie cutanée), de phénytoïne, perampanel, zonisamide, topiramate, prégabaline, phénobarbital.
- En pédiatrie, les traitements par voie intraveineuse sont la phénytoïne, le phénobarbital et le lévétiracétam ; la fosphénytoïne étant réservée aux enfants de plus de 5 ans. Le valproate est évité par crainte de décompensation d’une maladie métabolique chez les patients dont la cause de l’EME n’est pas identifiée. Par voie orale ou par sonde gastrique, on dispose de la phénytoïne, du zonisamide, du perampanel, du topiramate et du phénobarbital.
- Le recours aux agents anesthésiques qui impose une intubation et une ventilation mécanique n’est envisagé que très rarement car les risques d’une telle approche sont en règle supérieurs au bénéfice escompté.
La très grande diversité des types d’EME impose de connaître certaines spécificités de leur prise en charge :
- dans les EME partiels moteurs, l’escalade thérapeutique doit être progressive : des médicaments antiépileptiques peuvent être administrés par voie intraveineuse, ou orale dès la 2ème ligne de traitement. En cas de généralisation secondaire la prise en charge rejoint celle de l’EMETCG. «L’épilepsie partielle continue» est une forme très particulière d’EME focal, qui ne se généralise pas et est particulièrement pharmacorésistante ; les délais entre les lignes de traitement peuvent donc être prolongés et le recours à une anesthésie générale n’est pas indiqué. Il n’y a pas d’indication à un transfert en réanimation.
- l’EME absence dans le cadre d’une épilepsie généralisée idiopathique, qui s’accompagne souvent de quelques myoclonies, survient volontiers à l’arrêt du traitement ou à la prescription d’un médicament antiépileptique inapproprié (par exemple, carbamazépine, gabapentine, etc.). Il faut, après la prescription de BZD, réintroduire le traitement de fond par voie orale, et, si l’EME perdure, recourir selon les précautions sus-citées et, après avis chez l’enfant, au valproate de sodium IV.
- dans l’EME absence de novo, faisant suite à un sevrage brutal d’une BZD chez un sujet âgé, la réintroduction d’une BZD est souvent suffisante.
- dans les EME non convulsifs à expression confusionnelle, d’origine frontale ou temporale, dont il faut tenter de contrôler la cause, il convient de proposer comme traitement de 2ème ligne un traitement antiépileptique IV comme la (fos)phénytoïne, le lacosamide ou le lévétiracétam, voire le phénobarbital. Si une origine mitochondriale est suspectée, il faudra absolument éviter le valproate de sodium.
- dans les EME myocloniques sans troubles de conscience perceptibles qui surviennent dans le cadre d’une épilepsie généralisée idiopathique les BZD sont très efficaces.
- dans les EME toniques (rencontrés dans les encéphalopathies type Lennox Gastaut), la prescription de BZD doit être prudente car leur effet sédatif peut induire une majoration des crises toniques. Il conviendra de rechercher attentivement un foyer infectieux, souvent associé à ces EME.
ÉVOLUTION/PRONOSTIC
- Le pronostic vital et fonctionnel du patient (séquelles cognitives et épilepsie notamment) est avant tout déterminé par celui de l’étiologie de l’EME. Celle-ci peut gêner le contrôle symptomatique de l’EME si elle n’est pas rapidement et aisément accessible à un traitement et, par ailleurs, toute cause structurelle aiguë a son génie évolutif propre. Identifier et traiter chaque fois que possible la ou les causes d’un EME est donc urgent et primordial. On comprend donc que la part de ce qui, dans le pronostic, est clairement attribuable à l’activité épileptique elle-même est bien difficile à cerner.
De nombreux autres facteurs, dont il est malaisé d’apprécier l’importance relative, peuvent aussi influer sur le pronostic :
- Présentation clinique de l’EME avec ou sans trouble de la vigilance
- Durée : l’EME est d’autant plus difficile à contrôler au fur et à mesure que le temps s’écoule
- Caractère réfractaire ou non de l’EME
- Age, comorbidités
- Non-respect de la prise en charge à ce jour considérée comme optimale : précipitation, non prise en considération de la graduation de l’introduction des antiépileptiques, de leurs posologies et de leurs contre-indications, recours inadapté à un coma thérapeutique, contrôle imprécis des divers facteurs d’agression cérébrale actuellement répertoriés, traitement inapproprié et excessif de tracés électroencéphalographiques (EEG) interprétés à tort comme des EME ou a contrario non prise en compte d’un EME sur l’EEG, enquête étiologique superficielle, non recours à l’avis de médecins habitués à la prise en charge de l’EME surtout s’il est super-réfractaire.
- Effets secondaires éventuels des antiépileptiques et des agents anesthésiques
- Complications inhérentes à la réanimation, telles celles consécutives au recours à la ventilation mécanique ou à la survenue de sepsis.1 1
Parmi les facteurs éventuellement maîtrisables cités dans la liste ci-dessus, certains peuvent avoir un impact d’autant plus péjoratif qu’il existe une agression cérébrale aiguë structurelle sous-jacente.
PRÉVENTION
Votre texte ici
SURVEILLANCE
Votre texte ici
CAS PARTICULIERS
Votre texte ici
THÉRAPIES FUTURES
Votre texte ici
