Angor De Prinzmetal

Mise à jour
09/08/2020
INTRODUCTION/GÉNÉRALITÉ
- L'angor de Prinzmetal ou Prinzmetal (aussi connu comme l'angor inversa, ou spasme coronarien) est un syndrome coronarien aiguë constitué typiquement de l'angine de poitrine (douleur thoracique) au repos. Elle est provoquée par un vasospasme (rétrécissement des artères coronaires provoquées par la contraction du tissu musculaire lisse) plutôt que directement par l'athérosclérose (accumulation de plaque de cholestérol et un durcissement des artères).
HISTORIQUE
- En 1959, Myron Prinzmetal, cardiologue américain, décrit une forme singulière d’angine de poitrine : l’angor vasospastique ou communément appelé angor de Prinzmetal. Cette maladie n’est pas due à une ischémie induite par une sténose athéromateuse, mais résulte d’une vasomotricité anormale. Les mécanismes qui régissent ce trouble restent en partie inexpliqués à ce jour.1
- Le premier spasme coronarien est objectivé chez l'animal dès 1962 et chez l'homme en 1973.1
- Cependant, il avait déjà été décrit deux fois dans les années 1930 par d'autres auteurs.1
PHYSIOPATHOLOGIE
Le mécanisme qui provoque le vasospasme intense, et un rétrécissement significatif sur le plan clinique des artères coronaires est jusqu'ici inconnu.
Il y a trois hypothèses pertinentes :
- Contractilité accrue du muscle lisse vasculaire coronaire en raison de la biodisponibilité de l'oxyde nitrique réduite causée par un défaut dans l'oxyde nitrique synthétase endothéliale, enzyme qui conduit à des anomalies de la fonction endothéliale.1 1 L'acétylcholine est normalement libéré par le système nerveux parasympathique (SNPS) au repos, et provoque la dilatation des artères coronaires.1 Bien que l'acétylcholine induit une vasoconstriction des cellules musculaires lisses vasculaires par un mécanisme direct, l'acétylcholine stimule également les cellules endothéliales pour produire l'oxyde nitrique ( NO). le NO diffuse alors hors des cellules endotheliales, stimulant la relaxation des cellules musculaires lisses voisines. Dans les parois des artères saines, la relaxation indirecte globale induite par l'acétylcholine (via l'oxyde nitrique) à plus d'effet que toute contraction qui est induite. Lorsque l'endothélium est dysfonctionnel, la stimulation par l'acétylcholine échouera à produire, ou produira très peu, l'oxyde nitrique. Ainsi, l'acétylcholine libérée par les SNPS au repos va simplement provoquer la contraction du muscle lisse vasculaire.
- Le Thromboxane A2 qui est un vasoconstricteur libérée par les plaquettes pour aider à la formation de caillots, pourrait également jouer un rôle dans l'angor de Prinzmetal. La lipoprotéine interfère avec la fibrinolyse en compétition avec le plasminogène. L'altération de la fibrinolyse déclenche la formation d'un thrombus, ce qui se traduit également par un vasospasme coronaire dans l'angine de Prinzmetal.1
- Augmentation du nombre de récepteur alpha-adrénergique actif sur les artères coronaires épicardiques conduit au vasospasme coronarien.1
ÉPIDÉMIOLOGIE
- Marginale en occident, plus fréquente en Asie, la prévalence de cette pathologie potentiellement fatale en l’absence de traitement, reste incertaine.1
- Profil du patient à risque : Plutôt une femme, relativement jeune avec peu ou pas de facteurs de risque, mis à part une exposition passive ou active au tabac.
- Les antécédents les plus régulièrement cités sont : la migraine, le syndrome de Raynaud ou l’asthme.
FACTEURS DE RISQUES
Des facteurs déclenchants sont parfois identifiés :
EXAMEN CLINIQUE
- Cyclique, la maladie peut rester longtemps muette et se réveiller subitement.
- Les symptômes apparaissent généralement au repos, de préférence au petit matin et en fin de soirée.
- Polymorphe d’autre part, elle se manifeste par :
- Un angor typique avec sus-décalage du segment ST, soulagée par les dérivées nitrées (trinitrine) ; l’épisode angineux disparaît le plus souvent spontanément en quelques minutes. Les crises sont exceptionnelles à l’effort, mais fréquemment observées en phase de récupération.
- Un angor suivi d’une perte de connaissance (lié à l'intensité de la douleur ou provoquée par un trouble du rythme, avec dans ce cas un risque élevé de mort subite).
- Un infarctus du myocarde (IDM) inaugural, souvent massif.
- Une ischémie silencieuse, induite par un épisode spastique non occlusif. Des enregistrements Holter mettent en évidence des modifications électriques aux heures de manifestations habituelles.1
EXAMENS COMPLÉMENTAIRES
A) Electrocardiogramme (ECG) peut montrer :
- Un sus décalage diffus du segment ST régressant sous Trinitrine (dérivé nitré).
- Des troubles du rythme ventriculaire associées.
B) Coronarographie :
- Elimine un syndrome coronarien aigüe (Thrombose visible).
- Visualise le spasme coronaire parfois présent.
- Recherche une sténose athéromateuse associée.
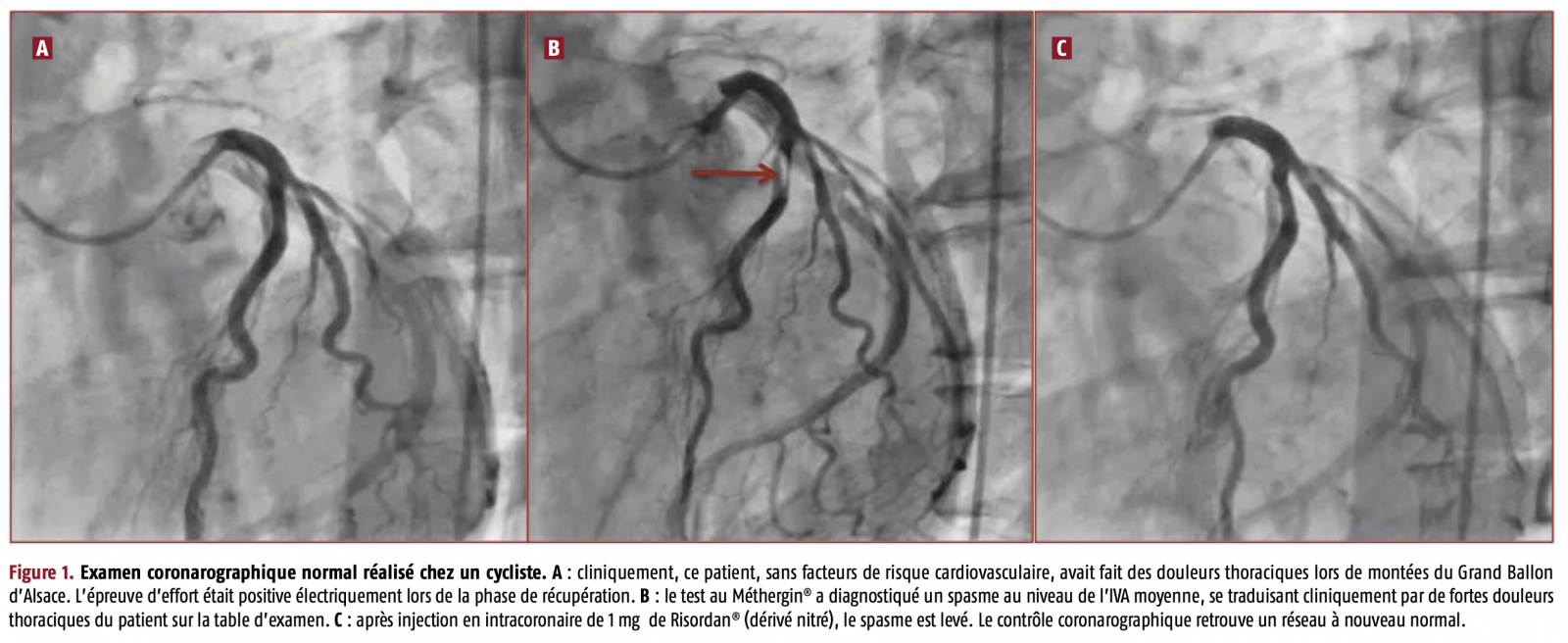
C) Tests de provocation : Test au (Méthergin®) : 1
- Ces tests associent la coronarographie (après élimination d'une sténose significative contre-indiquant le test) à l’injection d’une substance capable de déclencher un spasme chez les patients atteints par la maladie
- Deux tests permettent ce diagnostic : le test à l’acétylcholine (fiiable mais complexe dans sa mise en œuvre) et le test à la méthylergométrine (Méthergin®) (simple à réaliser, sûr et peu onéreux ; il est de loin le test le plus utilisé).
- La méthylergométrine est une molécule aux propriétés vaso-constrictrices, dérivé semi-synthétique d’un alcaloïde de l’ergot du seigle.
- Le test au méthergin® : La sensibilité (vrais positifs) et la spécificité (vrais négatifs) de ce test sont excellentes. Afin d’éviter les faux négatifs, la suspension des traitements vasoactifs s’impose 48 heures avant la coronarographie. Le choix de la voie d’abord n’est pas anodin. La médication indispensable pour maîtriser la propension au spasme de l’artère radiale contraint à préférer la voie fémorale pour éviter les interférences avec le test.
1) Les indications
Il existe différents cas de figure :
- L’indication de la coronarographie posée, le test au Méthergin® est envisagé pour les patients avec un profil et une clinique compatibles avec un angor vasospastique et réalisé si le réseau coronaire est indemne de lésion.
- Un test de provocation n’est pas recommandé en phase aiguë d’un IDM à « coronaires saines », mais décalé de quelques semaines après un bilan étiologique favorable à l’exploration.
- La stratégie est la même pour une mort subite récupérée, le test pourra se faire à distance après une exploration électrophysiologique négative.
- Pour finir, il est éventuellement possible d’évaluer l’efficacité d’un traitement antispastique chez des patients diagnostiqués au préalable.
- Cas particulier : si l’épisode vasospastique a été documenté par un enregistrement ECG montrant un sus-décalage du segment ST suivi d’une normalisation à la disparition de l’angor, une coronarographie normale suffit à poser le diagnostic. C’est le cas le plus simple, mais le moins fréquent.
2) Les contre-indications
- En plus des contre-indications à la coronarographie, le test est contre-indiqué en cas d’infarctus du myocarde (IDM) en phase aiguë, d’une maladie vasculaire périphérique sévère, d’hypertension artérielle sévère, d’allergie ou d’hypersensibilité à la méthylergométrine, de grossesse.
- Il existe un risque de vasoconstriction et/ou d’hypertension en cas d’interactions médicamenteuses (certains antimigraineux ou antibiotiques, par ex.), ce qui pourrait fausser le test ou pire, générer une complication.
3) Complications et effets secondaires
- Ils se manifestent par une poussée hypertensive, des céphalées, une éruption cutanée, un vasospasme périphérique, un trouble de la fréquence cardiaque (bradycardie ou tachycardie), des nausées, des vomissements, un accident vasculaire cérébral, un IDM.
- Remarque : le spasme coronaire, la douleur thoracique ou un sus-décalage du segment ST ne sont pas dans ce cas considérés comme des effets secondaires puisque volontairement induits.
4) Le test en pratique
- Comme pour tout acte invasif, le patient aura donné au préalable son consentement éclairé. La coronarographie, premier temps du test au Méthergin®, est réalisée par voie fémorale de préférence en 4 F pour minorer le risque hémorragique. Si aucune sténose significative n’est décelée, le test sera réalisé.
- Afin de sécuriser l’acte, il est essentiel de prépositionner une sonde au niveau du tronc commun jusqu’au contrôle angiographique et de disposer sur table d’un dérivé nitré (ex : Risordan®) prêt à l’emploi, afin de lever rapidement un spasme coronaire.
- La provocation débute avec une injection intraveineuse lente de 0,4 mg de méthylergométrine (2 ampoules de Méthergin®) suivie d’un temps d’attente (4 minutes) pendant lequel l’équipe restera à l’affût :
- d’une modification électrique à l’ECG
- de la survenue d’une douleur thoracique
- d’une modification de la pression invasive en bout de sonde
- d’une variation de la tension artérielle et/ou de la saturation en oxygène.
- Deux minutes après l’injection du Méthergin®, une nouvelle coronarographie est réalisée avec deux incidences pour la coronaire gauche (OAD 30°/caudale 30° et face/crâniale 30°) et une incidence pour la coronaire droite (face/crâniale 30°). Il n’y a cependant aucun dogme en la matière, le tout étant de dégager rapidement et au mieux les différentes branches en fonction de l’angiographie initiale.
- Au premier spasme visualisé, 1 mg de Risordan® sera immédiatement administré en intracoronaire, suivi d’un contrôle angiographique pour s’assurer du retour à la normale. Une injection de Risordan® est systématique en fin d’exploration même en cas de négativité du test pour parer à un éventuel « effet retard ».
- Remarque : au moindre signe d’ischémie apparaissant entre le moment T0 de l’injection et T0 + 2 minutes, le contrôle angiographique sera immédiat, avec une réversion du vasospasme si nécessaire.
- Pour être reconnu positif, le test doit provoquer la réduction du calibre d’une artère d’au moins 70 %.
- L’atteinte peut être focale ou diffuse, des réactions particulièrement intenses sont possibles avec des spasmes touchant l’intégralité du réseau coronaire.
- Une modification électrique et/ou l’apparition de douleurs (hors réaction extrême) ne sont pas obligatoires, la brièveté du test ne permettant pas toujours aux signes ischémiques de se manifester.
DIAGNOSTICS DIFFÉRENTIELS
Devant un sus-décalage du ST plusieurs diagnostics peuvent se poser :
- Syndrome coronarien aigu avec sus-décalage permanent du ST (SCA ST+) : à éliminer en priorité
- Anévrisme ventriculaire gauche
- Péricardite
- Repolarisation précoce
ÉTIOLOGIE
Votre texte ici
PRISE EN CHARGE THÉRAPEUTIQUE
- Le traitement curatif repose sur les inhibiteurs calciques à tropisme cardiaque, à des posologie élevée, parfois en association.
- Le traitement de la crise repose sur les dérivées nitrées.
- L'utilisation des bêta-bloquants tel que le propranolol est contre-indiqué dans l'angor de Prinzmetal car favoriseraient le spasme coronaire.1
ÉVOLUTION/PRONOSTIC
Votre texte ici
PRÉVENTION
Votre texte ici
SURVEILLANCE
Votre texte ici
CAS PARTICULIERS
Votre texte ici
THÉRAPIES FUTURES
Votre texte ici
